Clear Sky Science · nl
Laserinterstitiële thermotherapie en adjuvante pembrolizumab bij terugkerend hooggradig astrocytoom: een fase 1/geblokkeerde gerandomiseerde fase 2b-studie
Waarom deze hersenkankerstudie ertoe doet
Terugkerend hooggradig astrocytoom, waaronder glioblastoom, behoort tot de dodelijkste hersentumoren; de huidige behandelingen houden de ziekte zelden langdurig onder controle. Deze studie onderzoekt een tweestapsstrategie die eerst warmte van een laser gebruikt om tumorgezwel te vernietigen en de barrières van de hersenen tijdelijk te openen, gevolgd door een immuunmedicijn dat de eigen T‑cellen helpt achtergebleven kankercellen aan te vallen. Voor patiënten en families die met deze diagnose worden geconfronteerd, bekijkt het onderzoek of een minimaal invasieve ingreep een vrijwel niet‑reagerende kanker kan omzetten in een tumor die uiteindelijk op immunotherapie reageert.
Een nieuwe aanpak voor hardnekkige hersentumoren
Patiënten in deze proef hadden allemaal hooggradige astrocytomen die waren teruggekeerd na standaardtherapie, die meestal chirurgie, bestraling en chemotherapie omvat. De onderzoekers concentreerden zich op twee hulpmiddelen. Het eerste, laserinterstitiële thermotherapie (LITT), is een kijkgaatje‑procedure waarbij een dunne sonde onder MRI‑geleiding in de tumor wordt gebracht en gebruikt om kankercellen te verhitten en te doden, terwijl veel van het omliggende hersenweefsel wordt gespaard. Het tweede hulpmiddel is pembrolizumab, een veelgebruikt immunotherapeuticum dat PD‑1 blokkeert, een moleculaire “rem” die vaak voorkomt dat T‑cellen tumoren aanvallen. Eerdere pogingen om dergelijke middelen alleen bij deze hersentumoren te gebruiken waren teleurstellend. Het team vroeg zich daarom af of eerst de laser gebruiken de tumor en het immuunsysteem beter kon voorbereiden op een respons op pembrolizumab. 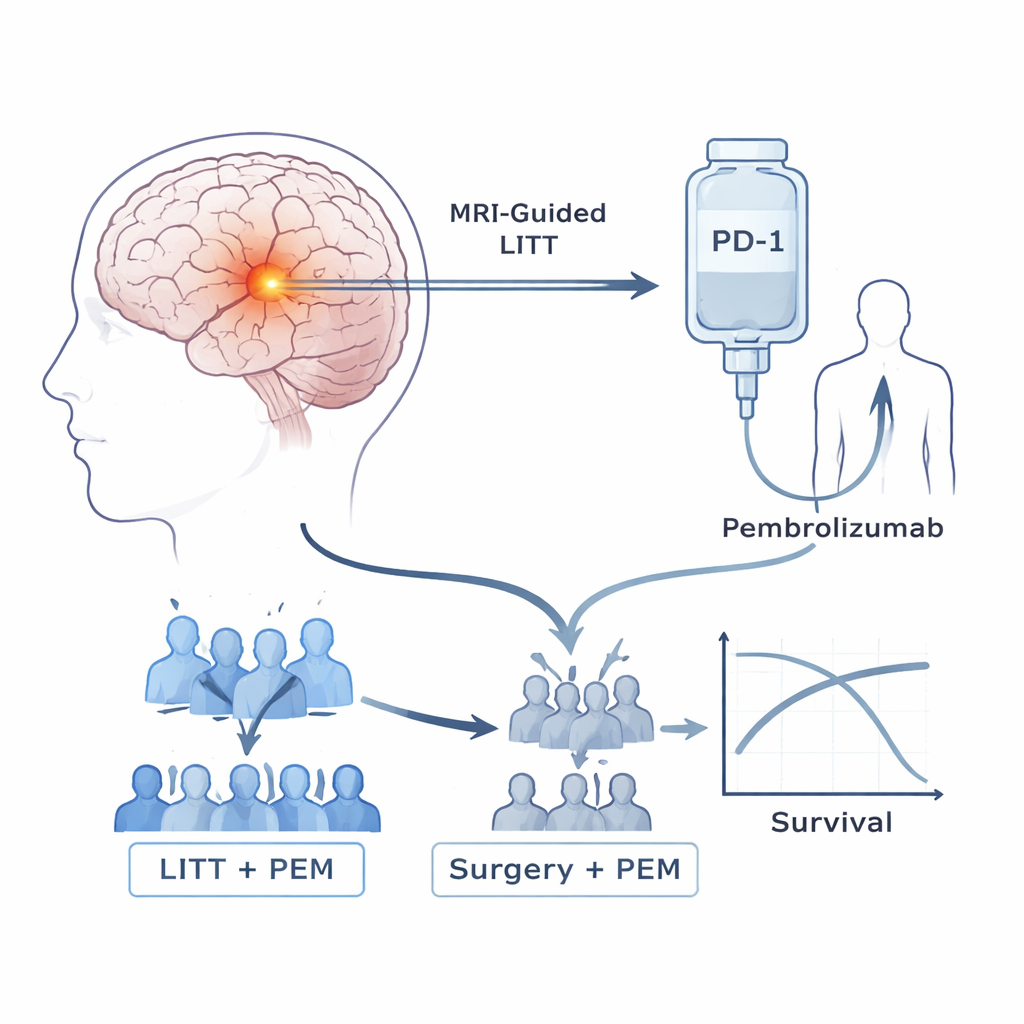
Hoe de klinische proef werd uitgevoerd
De studie begon met een kleine veiligheidsfase, waaruit bleek dat patiënten veilig elke drie weken pembrolizumab konden krijgen na LITT, zonder dosisbegrenzende bijwerkingen. Vervolgens ging men over naar een fase 2b‑onderzoek. Aanvankelijk werden patiënten willekeurig toegewezen aan een van twee groepen: LITT gevolgd door pembrolizumab, of conventionele herhaalde hersenchirurgie zonder laser, gevolgd door pembrolizumab. Naarmate buitenstaanders meer bewijs verzamelden dat chirurgie plus immunotherapie op zichzelf weinig voordeel bood, beoordeelde een onafhankelijk comité de vroege resultaten van deze proef. Zij zagen aanwijzingen dat de niet‑laser groep het relatief slecht deed terwijl de LITT‑groep leek te overleven, waarop ze verdere randomisatie stopzetten en alle latere patiënten de combinatie van laser en medicijn gaven.
Wat er gebeurde met overleving en tumorcontrole
Van de 39 patiënten die de behandeling volgens plan ontvingen, leefden degenen die LITT plus pembrolizumab kregen duidelijk langer dan degenen die chirurgie plus pembrolizumab ondergingen. De mediaan van de totale overleving was ongeveer 11,8 maanden met de gecombineerde LITT‑aanpak, versus 5,2 maanden met alleen chirurgie, en geen van de chirurgiepatiënten leefde nog na 18 maanden vergeleken met 42% van de LITT‑groep. Ook de tijd tot tumorprogressie verbeterde, van 1,6 maanden in de chirurgiegroep tot 4,5 maanden met LITT. Ongeveer 27% van de LITT‑behandelde patiënten had een meetbare tumorreductie en 70% behaalde ten minste tijdelijke ziektecontrole, terwijl alle patiënten die niet‑laserchirurgie plus pembrolizumab kregen progressie ervoeren. De bijwerkingen van de gecombineerde behandeling waren grotendeels mild en hanteerbaar, met enkele gevallen van diarree, spierzwakte en stijging van leverenzymen, maar geen sterfgevallen gerelateerd aan de behandeling.
Wat het immuunsysteem deed
Om te begrijpen waarom de combinatie mogelijk werkte, onderzochten de wetenschappers bloedcellen over tijd nauwkeurig met behulp van single‑cell RNA‑sequencing en tracking van T‑celreceptoren. Na LITT zagen ze dat een specifieke groep innate immuuncellen, zogeheten non‑classical monocyten, in een actievere staat verschoven die verband hield met migratie, ontsteking en interactie met T‑cellen—veranderingen die niet werden gezien na standaardchirurgie. Toen pembrolizumab vervolgens werd gestart, toonden patiënten die langer overleefden sterke golven van CD8‑T‑celactivatie en klonale expansie, wat betekent dat veel identieke T‑cellen die op dezelfde antigenen gericht zijn, zich vermenigvuldigden. Deze T‑cellen ontwikkelden zich vaak naar geheugen‑ en effectorstaten die tumorcellen kunnen herkennen en doden, in plaats van uitgeput en ineffectief te worden. Langdurige overlevenden lieten ook een daling zien van IDO‑1, een molecuul geassocieerd met immuunsuppressie, wat suggereert dat de combinatie meerdere lagen van immuunremming kan verlichten. 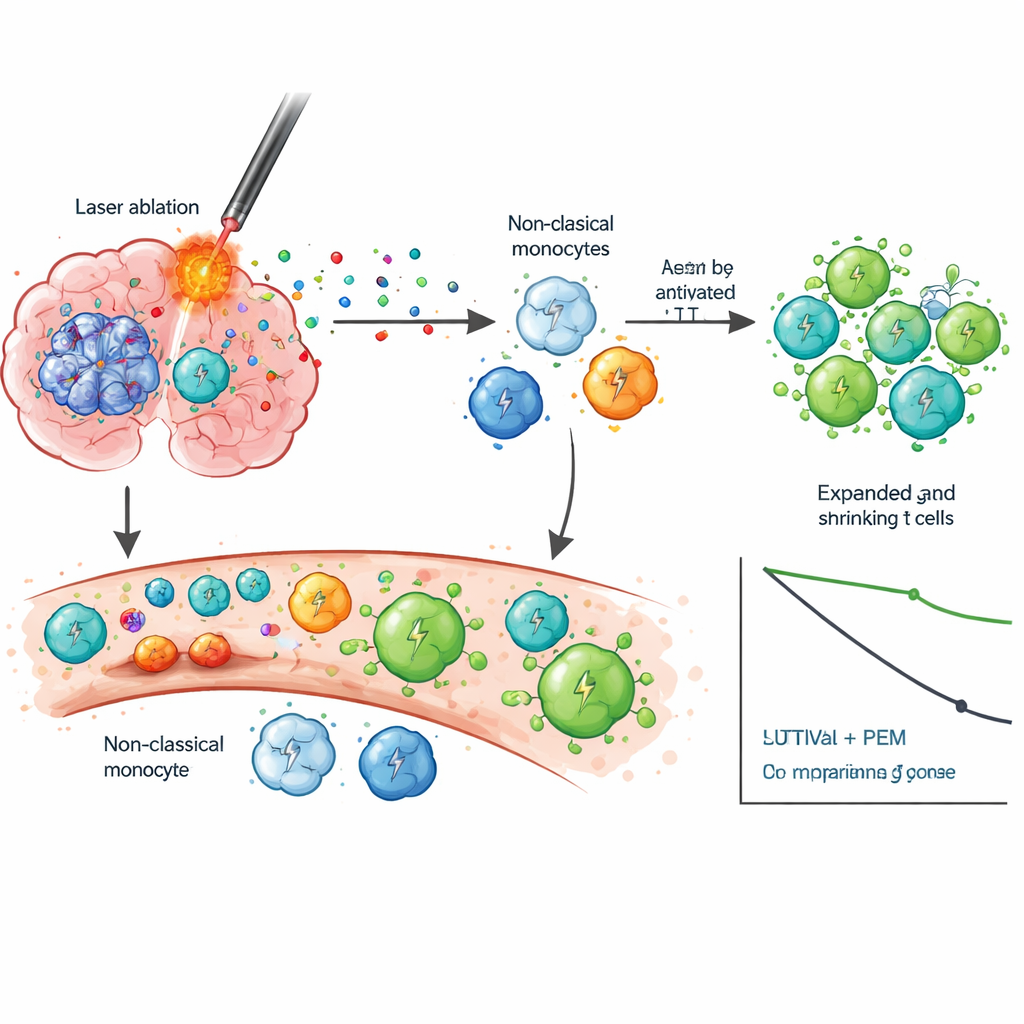
Wat dit voor patiënten zou kunnen betekenen
Voor mensen met terugkerend hooggradig astrocytoom suggereert dit werk dat MRI‑gestuurde laserablatie om de tumor te verkleinen, de bloed‑hersenbarrière kort te versoepelen en tumorfragmenten in de circulatie vrij te maken het toneel kan bereiden zodat immunotherapie kan werken waar die gewoonlijk faalt. Door een „signaalvuur” voor het immuunsysteem aan te steken en vervolgens de PD‑1‑rem met pembrolizumab te verwijderen, lijkt de combinatie duurzamere T‑celresponsen op te roepen en de overleving te verlengen bij een kanker met zeer beperkte opties. Omdat de studie relatief klein was en de randomisatie vroegtijdig stopte, benadrukken de auteurs dat grotere, volledig gecontroleerde trials nog steeds nodig zijn. Toch wijzen de resultaten op een veelbelovende nieuwe strategie: het koppelen van precies gerichte fysieke tumorvernietiging aan immuunmiddelen om een koude, resistente hersentumor te veranderen in een tumor die het lichaam eindelijk kan herkennen en bestrijden.
Bronvermelding: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Trefwoorden: glioblastoom, laserablatie, pembrolizumab, immunotherapie, hersen‑tumor