Clear Sky Science · nl
Overmatige FGFR3-signaaloverdracht bij achondroplasie verstoort het turnover van chondrocyten in de rustzone via CREB-signaalgeving
Waarom deze studie naar botgroei belangrijk is
Achondroplasie is de meest voorkomende oorzaak van genetische dwerggroei met korte ledematen. Het raakt niet alleen de lengte, maar ook de gezondheid van de wervelkolom, mobiliteit en levenskwaliteit. Huidige behandelingen helpen, maar herstellen de botgroei niet volledig. Deze studie gebruikt een geavanceerd muismodel om een eerder onopgemerkt probleemgebied in groeiende botten bloot te leggen en wijst op een nieuw schakelmechanisme in de signaaloverdracht, genaamd CREB, als veelbelovend doelwit voor toekomstige therapieën.
Hoe gezonde botten in lengte groeien
Lange botten, zoals het dijbeen, groeien in lengte bij de groeischijven nabij hun uiteinden. Die groeischijven zijn georganiseerd in drie hoofdlagen van kraakbeencellen. Bovenaan ligt de rustzone, waar cellen zich gedragen als een stamcelpool: ze delen langzaam en zenden dochtercellen naar beneden. Daaronder bevat de proliferatiezone snel delende cellen die in ordelijke kolommen gestapeld zijn en de lengtegroei aandrijven. Het verst doorontwikkeld is de hypertrofische zone, met vergrote, rijpe cellen die de vorming van nieuw bot begeleiden. Het evenwicht tussen deze zones zorgt dat botten met de juiste snelheid en vorm groeien.
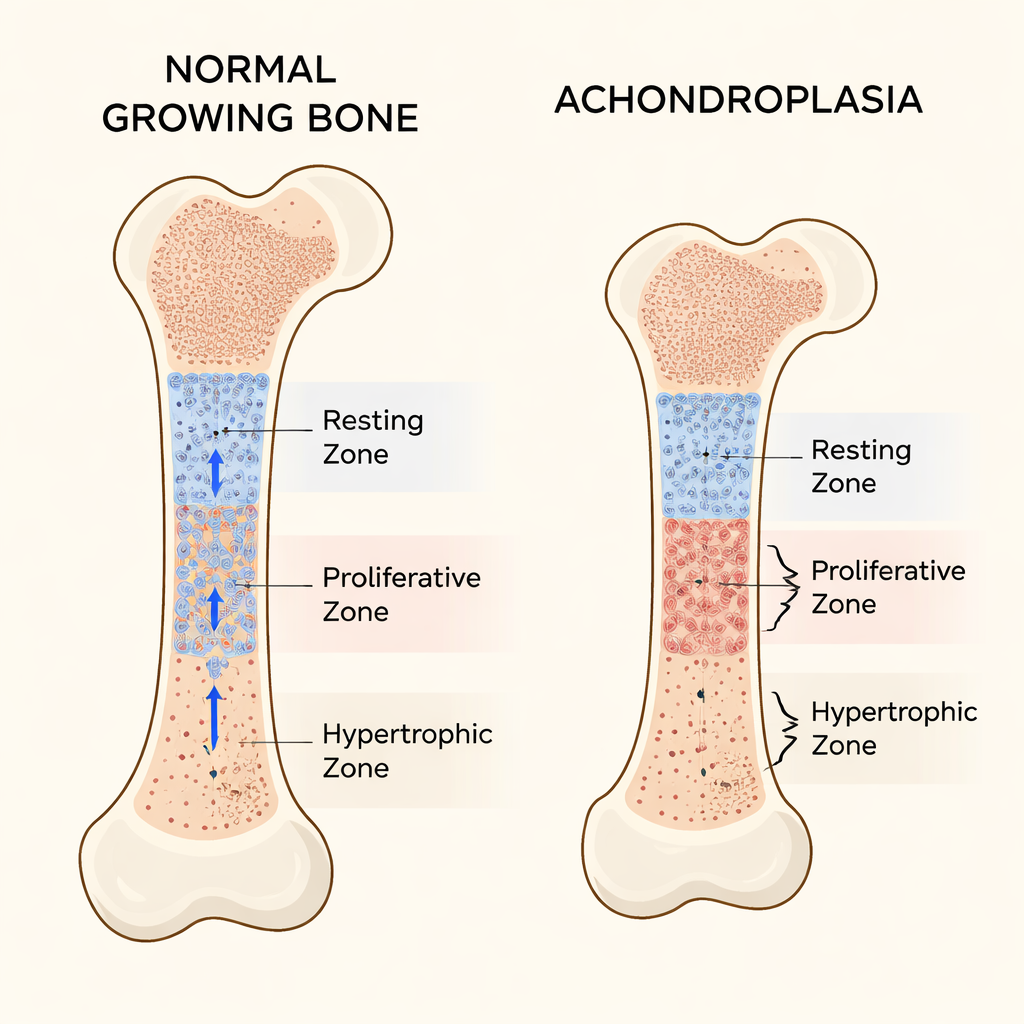
Wat er misgaat bij achondroplasie
Bij de meeste mensen met achondroplasie veroorzaakt een enkele mutatie in het FGFR3-gen dat de receptor overactief wordt en de botgroei afremt. Eerder onderzoek toonde aan dat deze signaaloverdracht de celdeling in de proliferatiezone vertraagt en de uiteindelijke vergroting van cellen in de hypertrofische zone blokkeert. Met muizen die de menselijke achondroplasie-mutatie dragen, bevestigden de auteurs ernstige kortere ledematen en verlaagde groeischijven. Zorgvuldige metingen toonden echter iets dat grotendeels over het hoofd was gezien: de rustzone zelf werd ongewoon dik. In plaats van als een stabiele, goed functionerende stamcelreserve te dienen, breidde dit gebied zich uit en bevatte het cellen met weinig normaal kraakbeenmatrix.
Rustzonecellen verliezen hun "stamcelachtige" gedrag
Om deze uitbreiding te doorgronden, volgde het team hoe groeischijfcelllen zich over tijd deelden en bewogen. Bij normale muizen deelden rustzonecellen zelden, en migreerden hun nakomelingen recht omlaag in kolommen om de proliferatiezone aan te vullen. Bij de gemuteerde muizen deelden veel meer cellen in de rustzone langzaam en bleven ter plaatse zitten, waardoor een drukke laag ontstond die de onderste zones niet goed voedde. Lijntracering met multikleuren genetische labels toonde dat clonale kolommen kort en ongeorganiseerd waren, met dochtercellen die in willekeurige richtingen zwierven in plaats van nette stapels te vormen. Merkers van stamcelachtige identiteit, zoals het eiwit CD73, waren verloren in de uitgezette rustzone, wat suggereert dat overactieve FGFR3 de normale stamcelnis heeft aangetast.
Een nieuwe verdachteling in de signaalweg: CREB
De onderzoekers gebruikte vervolgens single-cell RNA-sequencing om duizenden individuele groeischijfcellen te profileren. Ze identificeerden een onderscheidende cluster die overeenkwam met de uitgebreide rustzone en rijk was aan een gen genaamd Spon1, naast andere. Padanalyses lieten activatie zien van CREB, een eiwit dat genen aanzet wanneer het in zijn gefosforyleerde vorm staat. Microscopy toonde dat rustzonecellen in de gemuteerde muizen sterk geactiveerde CREB en diens co-activator CBP tot expressie brachten, samen met hoge niveaus van FGFR3 en downstream moleculen zoals STAT5. In celkweek verhoogde stimulatie van de FGFR3-route de CREB-activiteit en verhoogde SPONDIN1 (het SPON1-eiwit), terwijl blokkering van FGFR3 of CREB deze signalen reduceerde. Dit plaatst CREB als een belangrijke schakel tussen de overactieve receptor aan het celoppervlak en het afwijkende gedrag van rustzonecellen.
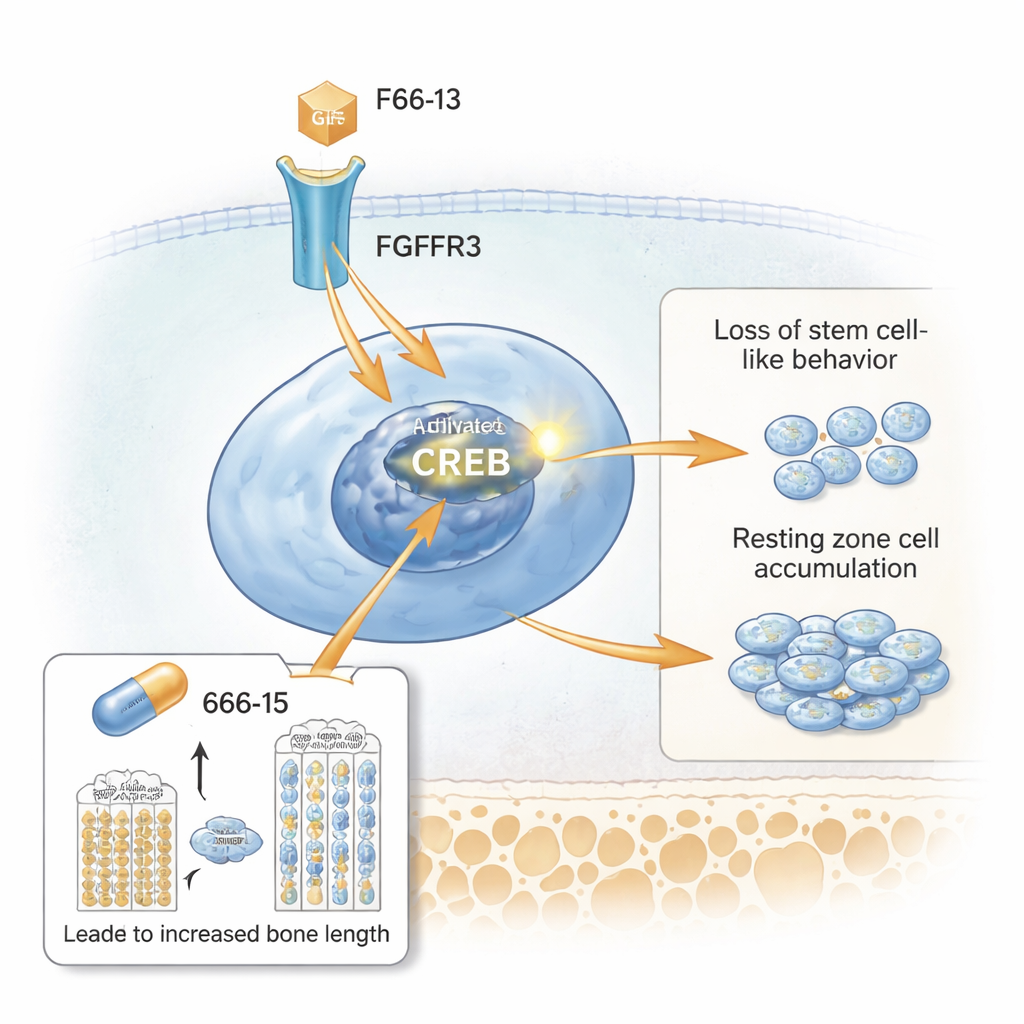
Testen van een middel dat CREB dempt
Tenslotte vroegen de onderzoekers of het onderdrukken van CREB de groeiproblemen kon verlichten. Ze behandelden achondroplasie-modelmuizen met een kleinmolecuul CREB-remmer, 666-15, tijdens de periode van snelle groei na de geboorte. Vergeleken met onbehandelde gemuteerde muizen hadden de muizen die 666-15 kregen een hoger lichaamsgewicht en langere dijbenen. Hun groeischijven leken normaler: de rustzone werd dunner, de proliferatieve en hypertrofische zones herstelden in hoogte, en eiwitten van de kraakbeenmatrix verschenen opnieuw. Merkers van overactieve CREB-signaalgeving, waaronder gefosforyleerd CREB, SPONDIN1 en STAT5, namen af in de rustzone, terwijl de stamcelachtige merker CD73 terugkeerde. Belangrijk: hetzelfde middel had bij de geteste dosis weinig effect op gezonde controlemuizen, wat erop wijst dat het vooral werkt wanneer CREB abnormaal verhoogd is.
Wat dit betekent voor toekomstige behandelingen
De studie laat zien dat bij achondroplasie overactieve FGFR3 meer doet dan alleen het vertragen van delende en vergrotende cellen; het ontregelt ook de rustige, stamcelachtige rustzone door CREB te activeren. Deze verstoring berooft de lagere lagen van de groeischijf van nieuwe cellen en draagt bij aan korte botten. Bestaande middelen zoals vosoritide richten zich vooral op andere routes in de proliferatieve en hypertrofische zones en herstellen de botlengte slechts gedeeltelijk. Door CREB toe te voegen aan de lijst van doelwitten — vooral in de rustzone — zouden toekomstige combinatiebehandelingen de groei bij kinderen met achondroplasie mogelijk vollediger kunnen normaliseren.
Bronvermelding: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Trefwoorden: achondroplasie, FGFR3, groeischijf, kraakbeenstamcellen, CREB-signaalgeving