Clear Sky Science · nl
High-throughput chemische proteomica-workflow voor het in kaart brengen van dynamiek in eiwitcitrullinatie
Waarom het veranderen van eiwitbouwstenen ertoe doet
Onze cellen stellen continu bij hoe eiwitten functioneren door kleine chemische aanpassingen toe te voegen nadat ze zijn gemaakt. Een van die aanpassingen, citrullinatie genoemd, verandert subtiel de lading van een veelvoorkomend aminozuur en kan de vouwing van eiwitten, het binden aan DNA of interacties met andere moleculen hervormen. Deze kleine wijzigingen worden steeds vaker in verband gebracht met auto-immuunziekten, infecties, kanker en hersenfunctie — maar ze zijn berucht lastig te detecteren. Deze studie introduceert een high-throughput laboratoriumworkflow die het eindelijk mogelijk maakt citrullinatie over duizenden eiwitten in kaart te brengen, waardoor wordt onthuld wanneer en waar het in weefsels en immuuncellen voorkomt.
Een verborgen schakelaar op eiwitten
Citrullinatie treedt op wanneer enzymen die PADs heten het aminozuur arginine chemisch wijzigen en daarmee zijn positieve lading verwijderen. Die ogenschijnlijk kleine wijziging kan de manier waarop DNA is verpakt versoepelen, de stijfheid van structurele eiwitten veranderen of beïnvloeden hoe het immuunsysteem eigen weefsels herkent. Abnormale citrullinatie is in verband gebracht met reumatoïde artritis, neurodegeneratieve aandoeningen, virusinfecties en kanker. Toch zijn gecitrullineerde eiwitten zeldzaam en gemakkelijk te verwarren met andere, meer voorkomende modificaties, waardoor standaard massaspectrometriemethoden ze vaak missen. Het gevolg is dat onderzoekers tot nu toe slechts een gefragmenteerd beeld hadden van het lichaamseigen ‘citrullinoom’ — de volledige set gecitrullineerde eiwitten.
Een twee-stappen tag-en-vang strategie
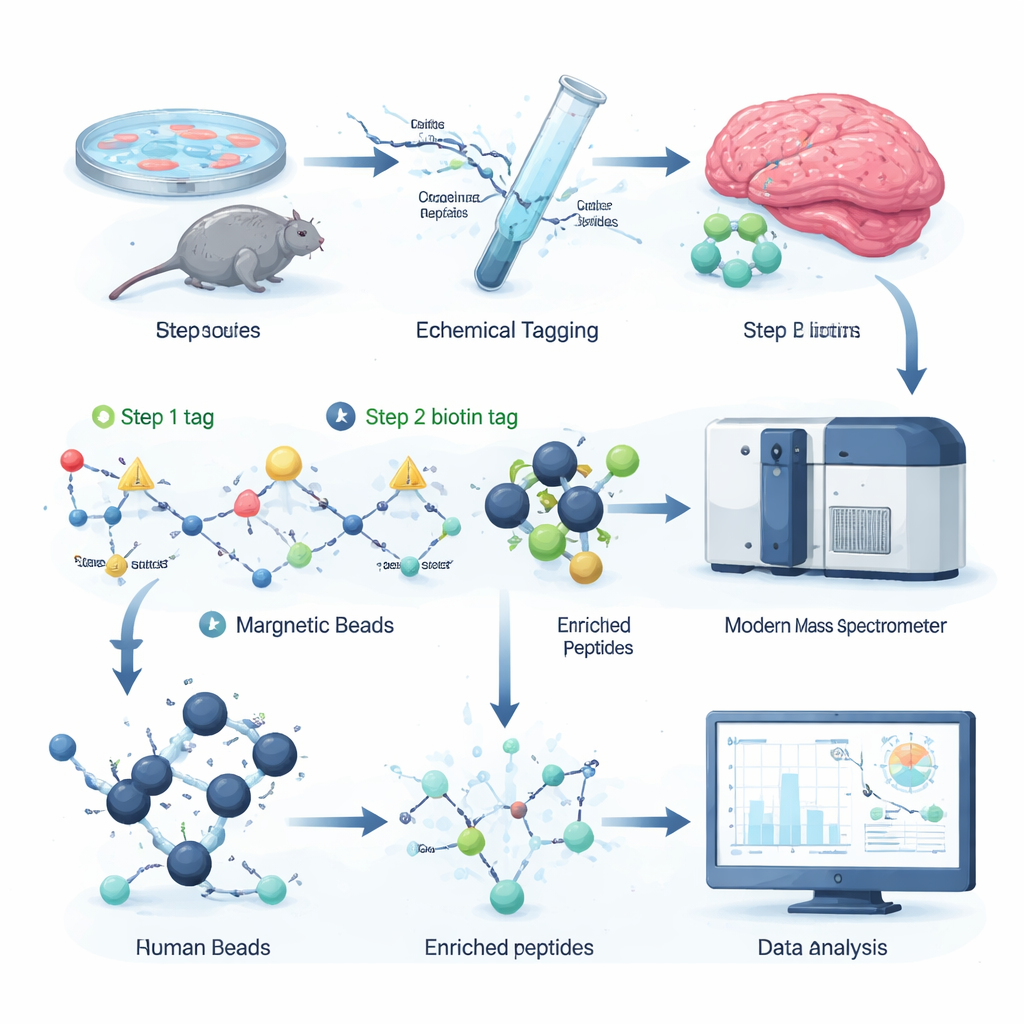
De auteurs ontwikkelden een chemische labelingsstrategie die selectief een verwijderbaar “handvat” aan citrullineplaatsen op peptiden bevestigt, de fragmenten van eiwitten die via massaspectrometrie worden geanalyseerd. In de eerste stap herkent een klein reactief molecuul citrulline en installeert een klein label. In de tweede stap wordt een groter biotinlabel ‘geklikt’, waardoor de gelabelde peptiden uit een complex mengsel met streptavidinebolletjes kunnen worden gevist, een veelgebruikt biochemisch hulpmiddel. Een milde chemische behandeling knipt vervolgens het omvangrijke deel van het label af, waardoor een kleine, goed gedefinieerde massaverschuiving achterblijft die de massaspectrometer gemakkelijk kan detecteren. Omdat alle reagentia commercieel verkrijgbaar zijn en het volledige protocol in 96-well platen past, is de workflow snel, schaalbaar en compatibel met bestaande proteomica-opstellingen.
Meer van het citrullinoom zien
Door bekende gecitrullineerde peptiden in celextracten te spiken en systematisch te verdunnen, toonde het team aan dat hun verrijkingsstrategie het signaal van gecitrullineerde peptiden meer dan tienmaal versterkt, zelfs wanneer ze minder dan één op de duizend moleculen vertegenwoordigen. In complexe monsters steeg het aantal gedetecteerde citrullinatieplaatsen en hun gemeten intensiteiten dramatisch na verrijking. Toepassing van de methode op muizenhersenweefsel onthulde twee- tot driemaal meer onderscheidende citrullinatieplaatsen dan een eerdere state-of-the-art methode, waaronder vele op myeline-basiseiwit, dat zenuwvezels isoleert, en op eiwitten die betrokken zijn bij synaptische communicatie. Dit suggereert dat citrullinatie zowel kan beïnvloeden hoe zenuwcellen signaleren als hoe de bedradingsstructuur van de hersenen wordt onderhouden.
Immuuncellen die plakkerige eiwitwebben werpen
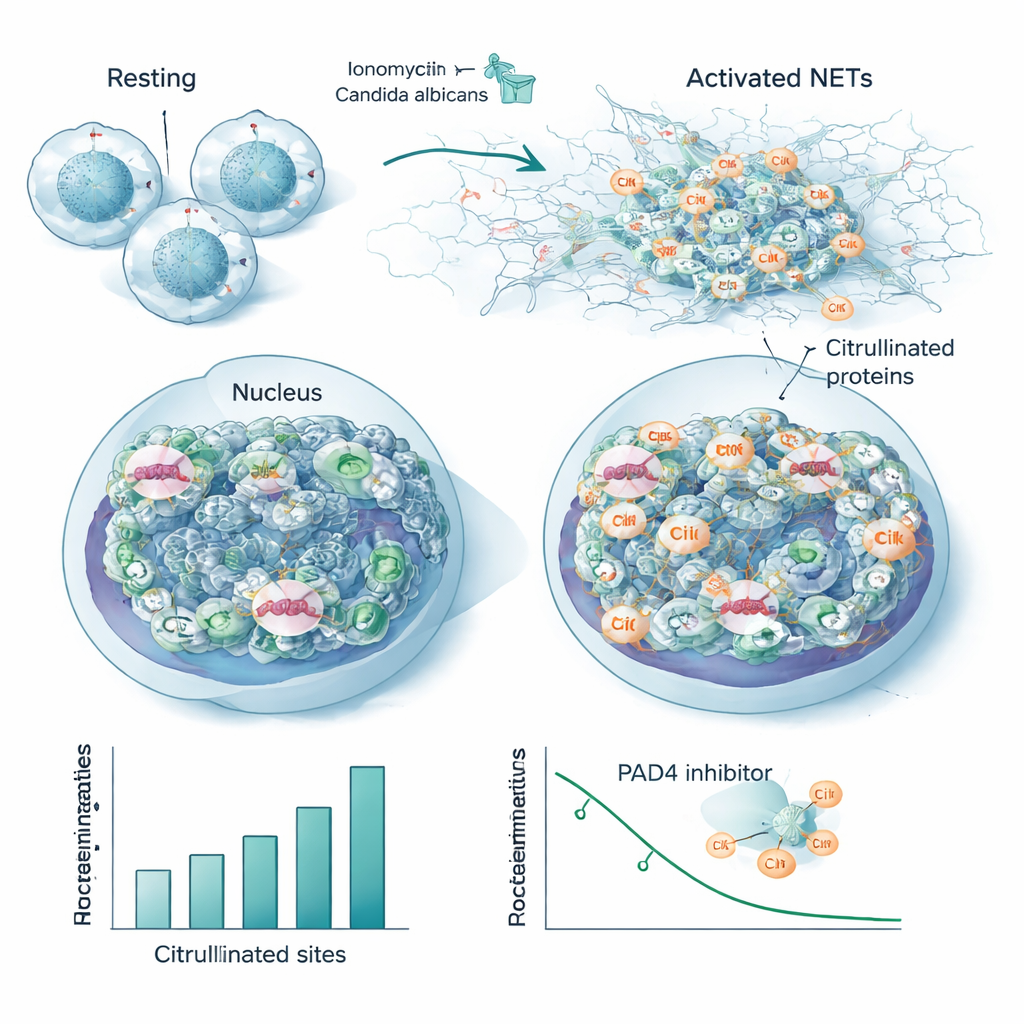
Neutrofielen, een type witte bloedcel in de voorste linie, kunnen indringers bestrijden door plakkerige webben van DNA en eiwitten vrij te geven, neutrofiele extracellulaire netwerken of NETs genoemd. De vorming van NETs is afhankelijk van PAD4, een citrullinerend enzym dat chromatine versoepelt zodat DNA kan ontsnappen. Met hun nieuwe workflow volgden de onderzoekers hoe citrullinatie veranderde in humane neutrofielen die werden blootgesteld aan toenemende doses van een chemische activator. Ze detecteerden tot 1.700 gecitrullineerde peptidefragmenten verdeeld over 580 eiwitten, waarbij honderden plaatsen in een dosisafhankelijke manier toenamen of afnamen terwijl de totale eiwitniveaus constant bleven. Histonen — de eiwitten die DNA verpakken — vertoonden wijdverspreide citrullinatie, niet slechts op enkele klassieke plaatsen, en varianten van het linkerhiston H1 waren bijzonder gemodificeerd. Structurele eiwitten zoals actineregulatoren en lamin B, dat de kernmembraan vormgeeft, werden ook sterk gecitrullineerd, wat wijst op een gecoördineerde versoepeling van zowel chromatine als cellulaire scaffold tijdens NET-vrijgave.
Een kernachtig citrullinatiehandtekening bij infectie
Om een echte infectie na te bootsen, stimuleerde het team neutrofielen met hitte-gedode Candida albicans, een veelvoorkomend schimmelpathogeen. Hoewel dit minder gemodificeerde plaatsen opleverde dan de sterke chemische activator, overlappen de overgrote meerderheid van de gecitrullineerde eiwitten en posities tussen de twee triggers. Deze overlap definieert een geconserveerd “kerncitrullinoom” geassocieerd met NET-vorming, waaronder veel nucleaire en cytoskeletale eiwitten en verschillende bekende autoantigenen — de exacte doelwitten van antilichamen bij auto-immuunziekten. Wanneer de onderzoekers een PAD4-blokkerend middel toevoegden, verloren veel van deze dezelfde plaatsen hun citrullinatie op een dosisafhankelijke manier, waarmee ze rechtstreeks aan de activiteit van het enzym werden gekoppeld en suggererend dat ze als gevoelige meetpunten voor PAD4-remming kunnen dienen.
Wat dit betekent voor gezondheid en ziekte
Door een ongrijpbare modificatie in een meetbaar signaal te veranderen, maakt deze workflow het mogelijk te kaarteren waar en wanneer citrullinatie voorkomt in weefsels, immuunreacties en ziektmodellen. Voor niet-specialisten is de kernboodschap dat citrullinatie werkt als een subtiele moleculaire dimmer op eiwitten, en dat het kunnen zien van de patronen in hoge resolutie kan helpen verklaren hoe auto-immuunziekten ontstaan, hoe infecties immuuncellen hervormen en hoe herseneiwitten in de loop van de tijd veranderen. De schaalbaarheid van de methode en het gebruik van standaardlabapparatuur betekenen dat ze breed kan worden toegepast, wat de deur opent naar het ontdekken van nieuwe medicijndoelen, precisiediagnostiek en een dieper begrip van hoe kleine chemische wijzigingen grote biologische gevolgen kunnen hebben.
Bronvermelding: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Trefwoorden: citrullinatie, auto-immuunziekte, neutrofiele extracellulaire netwerken, massaspectrometrie, post-translationele modificatie