Clear Sky Science · nl
Fysiopathologische betekenis van verminderde KAT7‑afhankelijke histon H3K14‑acetylatie tijdens zinktekort
Waarom piepkleine voedingsstoffen belangrijk zijn voor onze gezondheid
Zink is een sporenelement dat ons lichaam slechts in kleine hoeveelheden nodig heeft, maar het ondersteunt stilletjes honderden eiwitten die cellen laten functioneren. Wanneer zink ontbreekt—door voeding, ziekte of veroudering—wordt dat in verband gebracht met problemen variërend van slechte groei tot verzwakte immuniteit en leververvetting. Deze studie stelt een diepere vraag: hoe merken cellen eigenlijk dat zink opraakt, en hoe wordt dat tekort omgezet in duurzame veranderingen in genactiviteit en orgaangezondheid?
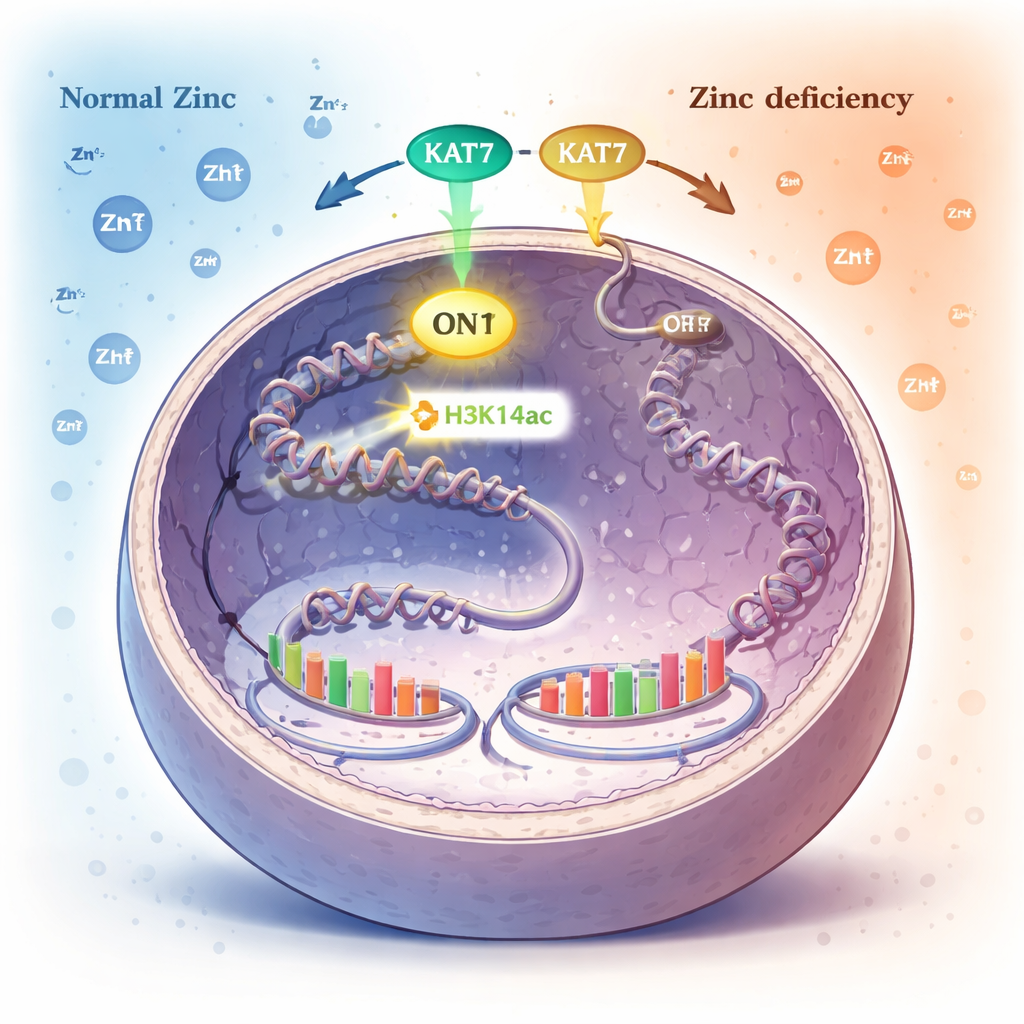
Een chemische markering op DNA‑verpakking als interne zink‑alarm
Binnen de kern is DNA omwikkeld rond eiwitspoelen die histonen worden genoemd. Cellen regelen welke genen actief zijn door kleine chemische markeringen aan deze histonen toe te voegen of te verwijderen. Een dergelijke markering, acetylatie op een specifieke positie van histon H3 (H3K14ac), wordt aangebracht door een enzym dat KAT7 heet. De auteurs ontdekten dat wanneer zink schaars wordt, de niveaus van deze H3K14ac‑markering sterk dalen, terwijl veel andere veelvoorkomende histonmarkeringen onveranderd blijven. Dit wees op H3K14ac, en het KAT7‑enzym dat het aanbrengt, als een belangrijke sensor van de zinkstatus.
Hoe zink een sleutelenzym ingeschakeld houdt
Door systematisch verschillende enzymen uit te schakelen, toonden de onderzoekers aan dat KAT7 de belangrijkste bron is van H3K14ac in menselijke cellen. KAT7 bevat een kleine zinkbindende structuur binnen zijn actieve centrum. Wanneer cellen in zinktekort werden gebracht, nam KAT7’s vermogen om het H3K14ac‑merk te plaatsen af, ook al bleef het eiwit zelf in de kern en gekoppeld aan zijn hulp‑partners aanwezig. Gedetailleerde tests met gezuiverde KAT7‑fragmenten toonden aan dat goed gebonden zink in dit gebied essentieel is voor zijn activiteit; het verstoren van zinkbinding schakelde het enzym uit, en het zorgvuldig toevoegen van zink herstelde de functie. In wezen gedraagt KAT7 zich als een zinkafhankelijke schakelaar die een specifiek histonmerk reguleert.
Het omzetten van zinkverlies in genveranderingen die zinkniveaus herstellen
Wat doet het verlies van dit histonmerk daadwerkelijk? Met behulp van genoom‑brede kaartlegging liet het team zien dat H3K14ac vooral is verrijkt bij enhancer‑regio’s—regulerende DNA‑streken die omliggende genen fijn afstellen. Onder zinkarme omstandigheden werd H3K14ac van veel enhancers verwijderd, en hoe groter het verlies, hoe sterker de verandering in de activiteit van naburige genen. Een opvallend gen was ZIP10, dat codeert voor een eiwit in het celmembraan dat zink opneemt. Wanneer H3K14ac bij de enhancer van ZIP10 daalde, steeg het niveau van ZIP10 in het membraan, waardoor er meer zink de cel in kon stromen. Het blokkeren van KAT7 of het verhinderen van het verlies van H3K14ac verstoorde deze reactie en verminderde de zinkopname, zelfs nadat zink weer werd toegevoegd. Dit toont aan dat cellen zink‑schaarste omzetten in een epigenetisch signaal dat het zink‑importapparaat versterkt om het evenwicht te herstellen.
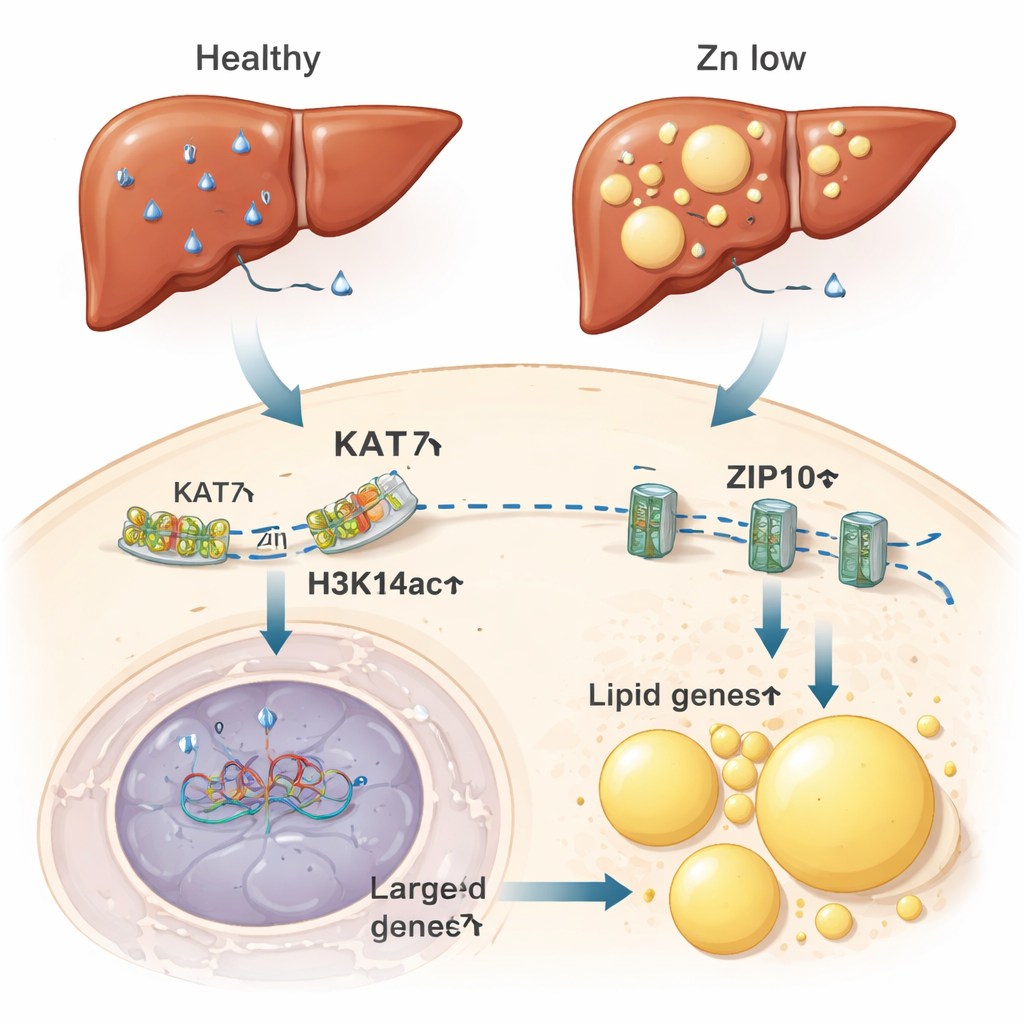
Van zink‑gehongerde cellen naar vette lever
De auteurs vroegen vervolgens of deze zinkgevoelige schakel gevolgen heeft in hele dieren. Bij muizen die een zinkarme voeding kregen, liet de lever—een centraal knooppunt van zink‑ en vetmetabolisme—verminderde zinkniveaus, lagere H3K14ac en verzwakte KAT7‑activiteit zien. Deze veranderingen gingen gepaard met een hogere expressie van genen die vetopslag en de vorming van lipidedruppels, de microscopische vetpakketjes in cellen, bevorderen. De lever van zinktekortmuizen stapelde vet op tot een omvang vergelijkbaar met die bij muizen op een vetrijk dieet. Opmerkelijk genoeg was het al voldoende om KAT7‑activiteit met een geneesmiddel te verlagen—zonder dieetverandering—om vetophoping in levercellen te bevorderen. Omgekeerd verminderde het toedienen van extra zink de vetophoping die door een vetrijk dieet werd veroorzaakt.
Wat dit betekent voor het risico op menselijke ziekte
In klinische context bekeken de onderzoekers menselijke studies die zinkniveaus in leverweefsel maten. In meerdere rapporten hadden mensen met leververvetting en gerelateerde aandoeningen significant minder zink in hun lever dan gezonde controles. Samen met de muisexperimenten suggereert dit dat chronisch zinktekort vetteleverziekte kan bevorderen door KAT7 te beëindigen, het H3K14ac‑merk te wissen en aanhoudend genen aan te zetten die vetopslag bevorderen. In eenvoudige bewoordingen onthult het werk een interne “zink‑naar‑epigenetica”‑circuits: wanneer zink daalt, verliest een zinkafhankelijk enzym kracht, wat de DNA‑verpakking op manieren verandert die aanvankelijk cellen helpen meer zink op te nemen, maar na verloop van tijd de lever ook richting ongezonde vetophoping kunnen duwen.
Bronvermelding: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Trefwoorden: zinktekort, epigenetica, levervet, histonacetylatie, zinktransporters