Clear Sky Science · nl
Drievoudige targeting van STING, TGF-β en PD-L1 versterkt CXCL16–CXCR6-signaalering voor krachtige antitumorrespons
Het veranderen van koude tumoren in hete tumoren
Kankerimmunotherapie heeft de behandeling voor sommige patiënten revolutionair veranderd, maar veel tumoren blijven ongevoelig voor deze krachtige middelen. Deze studie onderzoekt waarom bepaalde vormen van kanker moderne immuun-“checkpoint”-middelen weerstaan en stelt een slimmere, drievoudige aanpak voor die de afweer van het lichaam activeert, elite-dodende T-cellen aantrekt en deze cellen actief houdt, juist binnen de tumor.
Waarom huidige immuunmiddelen niet voldoende zijn
De meeste goedgekeurde immunotherapieën richten zich op één rem op immuuncellen, zoals het PD-1/PD-L1-pad. Een nieuwere klasse middelen probeert verder te gaan door ook TGF-β te blokkeren, een molecuul dat de immuniteit sterk onderdrukt bij gevorderde kankers. Eén zulk middel, YM101, combineert TGF-β- en PD-L1-blokkade in één antilichaam en toonde veelbelovende resultaten in muizen. Maar zelfs bij genetisch identieke dieren krimpten sommige tumoren nauwelijks. Door responsieve en resistente tumoren te vergelijken, vonden de onderzoekers dat succesvolle behandeling samenhing met sterke “innate” immuunactivatie, vooral signalering via een pad dat STING heet, dat afwijkend DNA detecteert en antivirale alarmtekens activeert.
Een derde hefboom toevoegen: de STING-route
Aangezien zwakke innate-activatie het ontbrekende puzzelstuk leek, combineerde het team YM101 met een pilvormige STING-agonist genaamd MSA-2 in meerdere muismodellen van tumoren, inclusief typisch moeilijk behandelbare “koude” tumoren. De drievoudige aanpak—STING-activatie plus TGF-β- en PD-L1-blokkade—verkleinde tumoren effectiever, verlengde de overleving en beschermde muizen vaak tegen terugkeer van tumoren na heruitdaging, wat wijst op langdurig immuungeheugen. Dit presteerde beter dan de meer conventionele combinatie van een STING-agonist met alleen PD-L1-blokkade, en versterkte zelfs STING-agonisttherapie wanneer alleen TGF-β werd geblokkeerd, wat aangeeft dat TGF-β zelf een belangrijke rem vormt op STING-gedreven immuniteit. 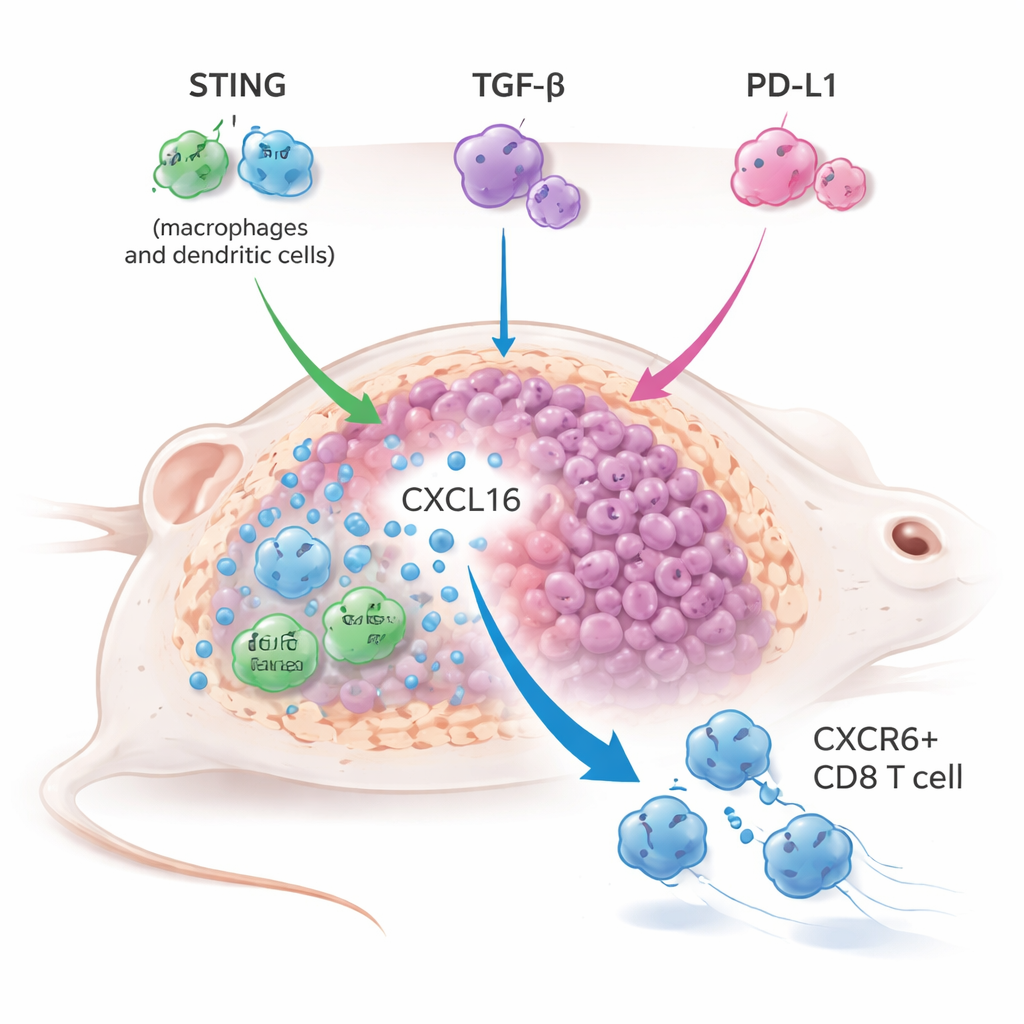
Het rekruteren van een gespecialiseerde dodelijke eenheid
Om te begrijpen hoe deze drievoudige strategie werkte, gebruikten de onderzoekers single-cell RNA-sequencing en gedetailleerde immuunprofilering van behandelde tumoren. Ze ontdekten een opvallende uitbreiding van een specifieke subset dodelende T-cellen, gekenmerkt door de receptor CXCR6. Deze CXCR6+ CD8-T-cellen waren sterk bewapend, met hoge expressie van granzymen, perforine en ontstekingsmoleculen, en toonden duidelijke tekenen van activatie en proliferatie. Tegelijkertijd verhoogden tumorgeassocieerde macrofagen en dendritische cellen de productie van een chemokine genaamd CXCL16, die aan CXCR6 bindt en helpt deze T-cellen in de tumor te behouden. Wanneer de CXCL16–CXCR6-koppeling werd verbroken—ofwel door CXCL16 te blokkeren of door CXCR6 genetisch uit T-cellen te verwijderen—verloor de gecombineerde behandeling grotendeels haar antitumorkracht, wat bewijst dat deze as centraal is voor het succes van de therapie.
Hoe de signaalketen wordt aangezet
Dieper gravend vroegen de onderzoekers hoe STING-activatie en TGF-β-blokkade gezamenlijk CXCL16 versterken. In menselijke en muisimmuuncellen verhoogden STING-agonisten sterk CXCL16 en het antivirale cytokine IFN‑β, terwijl extra TGF-β beide sterk verminderde. De onderzoekers toonden aan dat STING IFN‑I-signaleringsroutes activeert, die de transcriptiefactor STAT1 inschakelen; STAT1 bindt vervolgens direct aan het regelgebied van het CXCL16-gen en zet het aan. TGF-β verstoort deze keten door een cruciale stap in STING-signaleringsroutes te remmen, waarschijnlijk via een eiwit genaamd HDAC4 en reactieve zuurstofsoorten, waardoor IRF3-activatie en downstream IFN‑β- en CXCL16-productie worden afgezwakt. Het blokkeren van TGF-β haalt deze rem weg, waardoor STING-agonisten het STAT1–CXCL16-pathway in myeloïde cellen volledig kunnen ontsteken en zo CXCR6+ T-cellen de signalen geven die ze nodig hebben om in de tumor te blijven en te vechten.
Het bouwen van een enkel precisiemiddel
Om dit complexe regime praktischer en tumorgereflecteerder te maken, ontwierpen de onderzoekers een enkel “immuunstimulerend antilichaam-conjugaat” genaamd Y101S. Dit molecuul combineert het dubbele TGF-β/PD-L1-blokkerende antilichaam met een STING-agonist die vastzit aan een afbreekbare linker. Y101S zoekt PD-L1–positieve myeloïde cellen in de tumor op, wordt door die cellen geïnternaliseerd en geeft vervolgens het STING-middel vrij binnenin deze cellen. In meerdere muiskankers evenaarde of overtrof Y101S de werkzaamheid van het toedienen van YM101 plus een hoge dosis vrije STING-agonist, ondanks dat het slechts een klein fractie van die STING-dosis droeg. Het verhoogde CXCL16+ macrofagen en dendritische cellen, breidde CXCR6+ CD8-T-cellen uit, induceerde duurzaam immuungeheugen en concentreerde ontstekingssignalen in tumoren terwijl gezonde organen gespaard werden, met een gunstig veiligheidsprofiel in muizen. 
Wat dit betekent voor toekomstige kankerbehandelingen
Voor niet-specialisten is de kernboodschap dat het aanvallen van kanker met slechts één of twee immuumschakelaars mogelijk niet voldoende is—vooral wanneer tumoren vroege alarmsystemen actief dempen. Dit werk laat zien dat het combineren van STING-activatie met blokkade van TGF-β en PD-L1 het tumormilieu kan herbedraden, krachtig een gespecialiseerde groep dodelijke T-cellen kan aantrekken en in stand kan houden, en diepere, duurzamere reacties kan bewerkstelligen in preklinische modellen. Het drievoudig gerichte antilichaam–drug Y101S belichaamt deze strategie in één gerichte medicatie en biedt een routekaart voor de volgende generatie immunotherapieën gericht op tumoren die momenteel standaard checkpoint-middelen weerstaan.
Bronvermelding: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Trefwoorden: kankerimmunotherapie, STING-route, TGF-beta-blokkade, PD-L1 antilichaam, CXCL16 CXCR6 T-cellen