Clear Sky Science · nl
Positieve cooperativiteit tussen RAS-bindende en cysteïnerijke domeinen reguleert RAF-membraanbindingssnelheden via lateraal opnieuw binden
Waarom deze kleine moleculaire dans ertoe doet
In onze cellen worden levens-of-doodbeslissingen over groei, deling en overleving vaak genomen aan het oppervlak van het celmembraan. Een sleutelspeler in deze beslissingen is een eiwit genaamd RAF, dat helpt groeisignalen door te geven en dat vaak verkeerd geconfigureerd is bij kanker. Deze studie onthult, in ongekende kinetische details, hoe RAF zich vastklampt aan celmembranen, hoe lang het daar blijft, en waarom drukbezette gebieden met een ander eiwit, RAS, RAF langer actief kunnen houden dan verwacht.
Signalen die samenkomen aan het celoppervlak
RAF werkt in een belangrijke signaalroute die bekendstaat als de MAPK-route, die externe aanwijzingen zoals groeifactoren koppelt aan veranderingen in genactiviteit. In zijn rusttoestand zweeft RAF in het celinterieur in een gevouwen, zelfgeïnhibeerde vorm. Het wordt pas geactiveerd wanneer het RAS ontmoet, een klein moleculair schakelaartje dat verankerd is aan de binnenkant van het celmembraan. RAS moet in zijn “aan”-toestand verkeren en ingebed zijn in het juiste type lipiden om RAF te kunnen rekruteren en activeren. Omdat RAF-moleculen relatief schaars zijn vergeleken met veel andere signaalcomponenten, beïnvloedt de precieze manier waarop ze het membraan aangaan en vroegtijdig loslaten voorkomen sterk of een cel zwak of sterk reageert op een groeisignaal.
Twee handen om het membraan vast te pakken
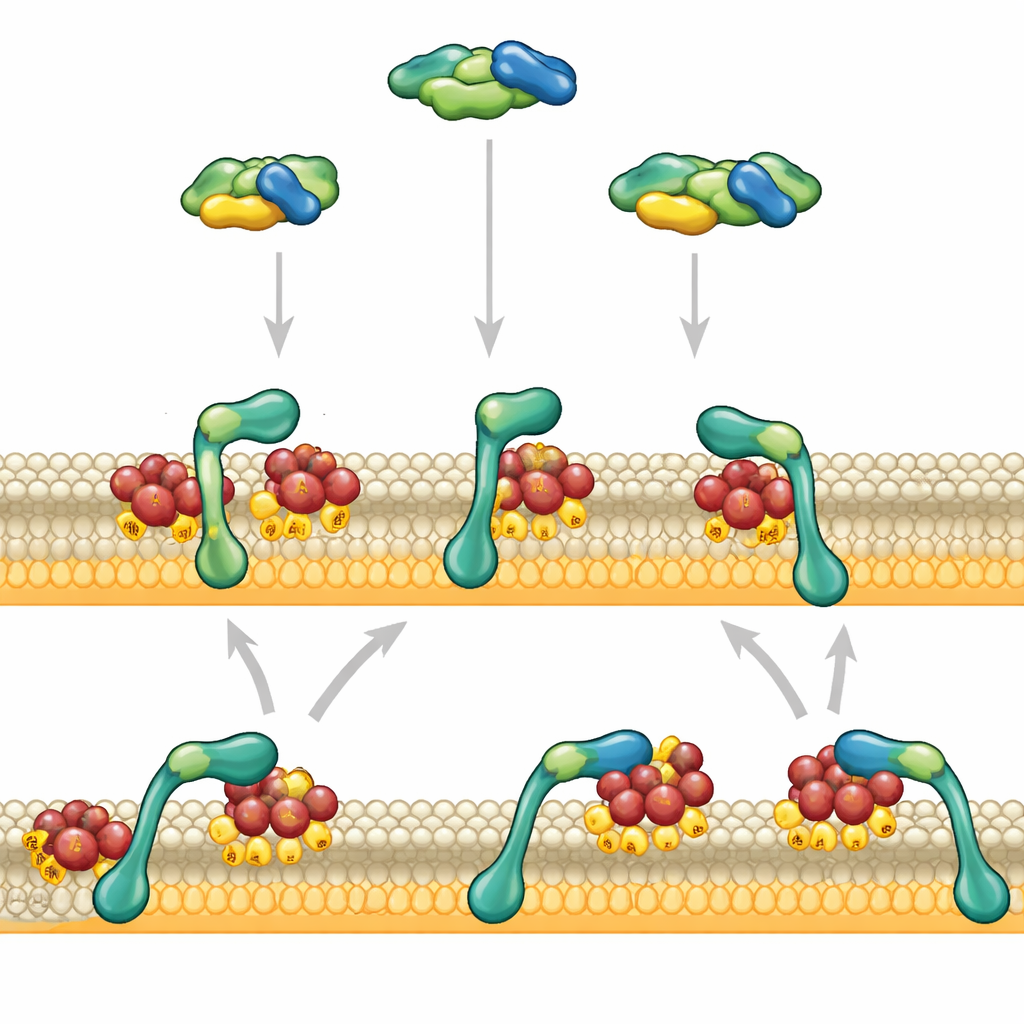
De auteurs concentreerden zich op twee regio’s aan RAFs voorzijde: één die RAS vastgrijpt en één die de voorkeur heeft voor negatief geladen membraanlipiden. Met behulp van kunstmatige membranen en gezuiverde eiwitten observeerden ze individuele RAF-fragmenten die binden aan RAS-bezet oppervlak met geavanceerde microscopie. Wanneer het RAS-bindende domein alleen werkte, raakte het het membraan kort aan en liet het na ongeveer een seconde weer los. Het lipidenminnende domein, op zichzelf, plakte nauwelijks. Maar wanneer deze twee domeinen aan elkaar verbonden waren, gedroegen ze zich heel anders: RAF hechtte nu sterk en bleef tientallen seconden op het membraan, vooral wanneer het membraan veel negatief geladen lipiden droeg die vergelijkbaar zijn met die in echte cellen.
Coöperatie die het vertrek vertraagt
Deze dramatische verandering kwam niet doordat RAF het membraan sneller vond, maar omdat het langzamer losliet. Eerst herkent RAFs RAS-bindende segment geactiveerde RAS en legt RAF zo aan het membraan vast. Pas na deze eerste handdruk gaat het lipidebindende domein volledig de omliggende lipiden aan, waardoor RAF’s zijwaartse beweging vertraagt en het steviger verankerd raakt. Dit tweede contact stabiliseert op zijn beurt de oorspronkelijke RAS–RAF-interactie, waarmee een positieve terugkoppeling ontstaat tussen eiwit–eiwit- en eiwit–lipidecontacten. Experimenten waarbij de korte schakel die de twee domeinen verbindt werd veranderd, toonden aan dat hun strakke ruimtelijke coördinatie cruciaal is: de schakel flexibeler of langer maken verzwakte RAFs vermogen om op het membraan te blijven.
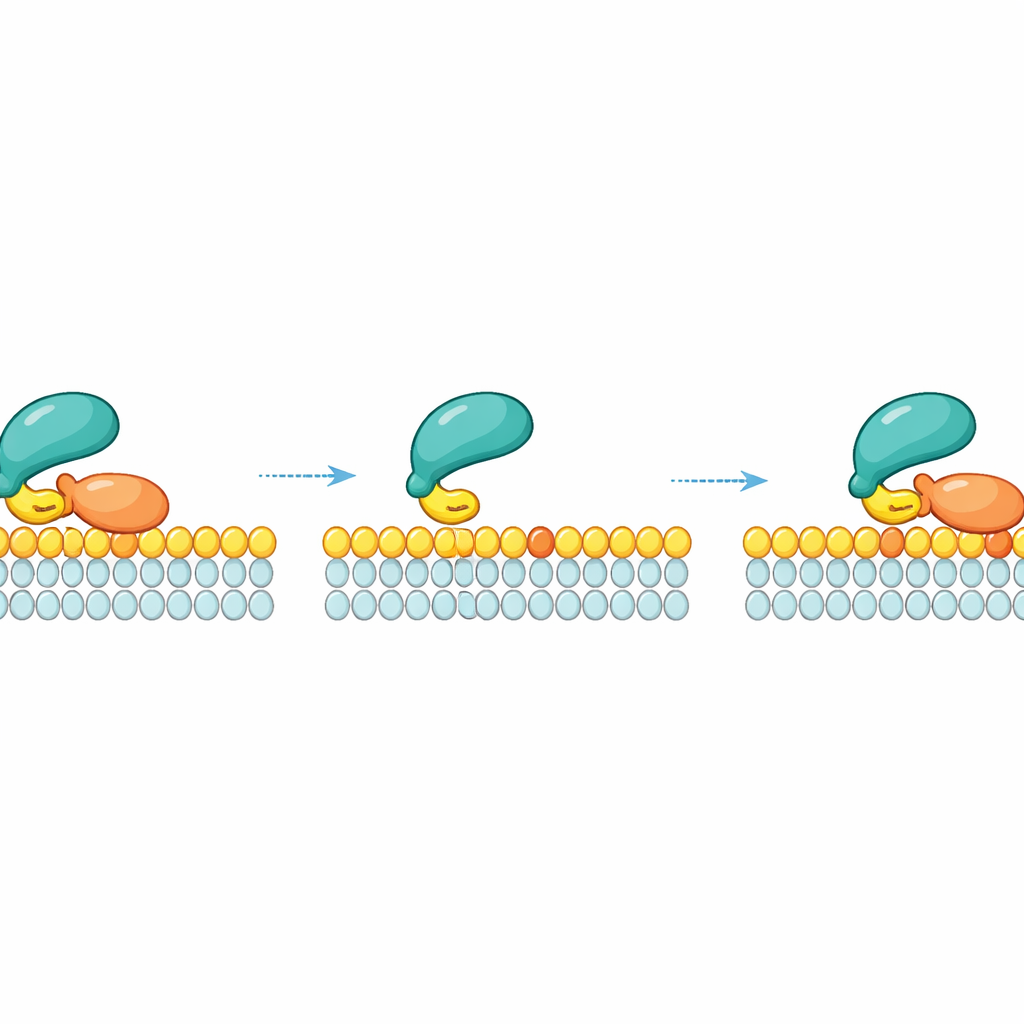
Lateraal opnieuw binden: glijden in plaats van ervanaf vallen
Een belangrijk inzicht van het werk is dat RAF niet simpelweg in de omringende vloeistof loslaat zodra het een specifiek RAS-molecuul loslaat. In plaats daarvan kan RAF, nadat RAS loslaat, kort via zijn zwakke lipidecontact aan het membraan blijven hangen en zijwaarts schuiven. Terwijl het in deze tijdelijke toestand verkeert, kan het een naburig RAS-molecuul op hetzelfde membraangebied opnieuw “vastgrijpen”. Dit laterale opnieuw binden creëert een kinetisch vangnet: bij hoge lokale RAS-dichtheid — zoals in nanoclusters waar RAS-moleculen dicht opeengepakt zijn — heeft RAF veel kansen om RAS opnieuw te binden voordat het wegdrijft. Metingen en simulaties lieten zien dat hoe groter de dichtheid van actief RAS op het membraan, hoe langer RAF membaangebonden blijft door deze herhaalde lokale heraankoppelingen.
Van verlengde verblijven naar betrouwbare activatie
De verlengde tijd die RAF op het membraan doorbrengt heeft belangrijke consequenties. RAF-activatie is geen enkelvoudig evenement maar een meerstapsreeks die vormveranderingen, verwijdering van remmende labels en het koppelen van twee RAF-moleculen tot een actief dimer omvat. De studie suggereert dat alleen RAF-moleculen die lang genoeg op het membraan verblijven deze reeks kunnen voltooien, een vorm van “kinetische proofreading” die cellen helpt accidentele activatie door vluchtige, zwakke signalen te vermijden. Door te onthullen hoe de wisselwerking tussen RAS-binding, lipide-engagement en lateraal opnieuw binden RAFs membraangebonden verblijftijd bepaalt, schetst het werk een algemene strategie waarmee cellen veel kleine, zwakke interacties op membranen kunnen gebruiken om krachtige signaalroutes fijn af te stemmen.
Bronvermelding: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Trefwoorden: RAS, RAF-kinase, celmembraan signalering, lateraal opnieuw binden, kinetische proofreading