Clear Sky Science · nl
Structurele en moleculaire basis voor allosterische regulatie en katalytische koppeling van menselijke phosphoribosylformylglycinamidine synthase
Waarom dit enzym belangrijk is voor de gezondheid
Elke cel in uw lichaam heeft purines nodig, kleine moleculen die reacties aandrijven, energie opslaan en genetische informatie dragen. Kankercellen, die snel delen, hebben bijzonder veel purines nodig en herschikken vaak de manier waarop ze worden gemaakt. Deze studie richt zich op een humaan enzym dat FGAMS wordt genoemd, een sleutelspeler in de de novo synthese van purines. Door de driedimensionale structuur van FGAMS en de bewegingen en communicatie tussen zijn onderdelen bloot te leggen, laten de auteurs zien hoe het enzym wordt aan- en uitgezet en hoe het mogelijk gericht kan worden om tumor groei te vertragen.
De bouwstenen van het leven onder controle
Cellen maken purines via een arbeidsintensieve assemblagelijn die bekendstaat als de de novo-route, die energie verbruikt en meerdere enzymen gebruikt om een complex ringvormig molecuul op te bouwen. FGAMS voert de vierde stap in deze reeks uit en bevindt zich in het hart van een groter enzymcomplex, het purinosoom, dat helpt ingrediënten efficiënt door te geven. Omdat snelgroeiende kankercellen deze route vaak opdrijven, zijn enzymen zoals FGAMS aantrekkelijke medicijndoelen: het blokkeren ervan kan tumoren berooien van de nucleotiden die ze nodig hebben, terwijl gezonde cellen terugvallen op recyclemechanismen.
Een vormveranderende moleculaire machine
FGAMS bestaat uit drie verbonden delen of domeinen die elk een verschillende taak vervullen en in een nauwkeurige volgorde moeten samenwerken. Het ene domein knipt ammoniak af van het aminozuur glutamine, een ander gebruikt die ammoniak om een klein suikermolecuul te modificeren, en een derde domein fungeert als regulerend knooppunt. Met hoogresolutie cryo-elektronenmicroscopie vingen de onderzoekers FGAMS in drie verschillende werktoestanden: gebonden aan een energiedragend molecuul, met een kortstondig reactietussenproduct gevangen, en met meerdere substraten en tussenproducten aanwezig tegelijk. Vergelijking van deze toestanden toonde aan dat flexibele lussen en een N-terminale “arm” dramatisch bewegen en het enzym herconfigureren naarmate de chemie vordert.
Verborgen tunnel en moleculaire poorten
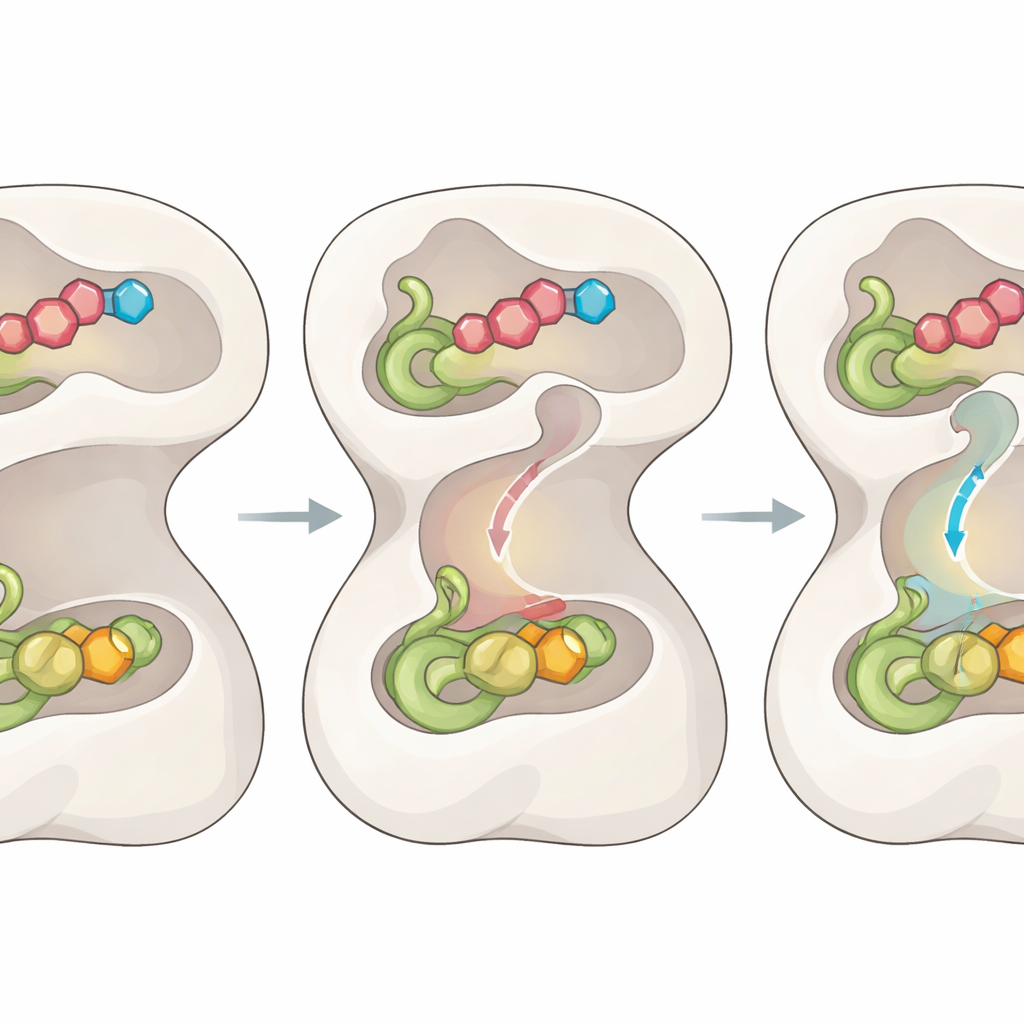
Een belangrijk raadsel was hoe de in het ene domein vrijgemaakte ammoniak veilig naar de verre plaats wordt geleid waar ze wordt gebruikt, zonder weg te diffuse ren en schade te veroorzaken. De nieuwe structuren onthullen een tot nu toe onzichtbare interne tunnel die de twee plaatsen verbindt, samen met een reeks “poorten” gevormd door specifieke aminozuren. Wanneer de juiste substraten binden en het tussenproduct ontstaat, klapt een centrale lus in een geordende positie, trekt aan het N-terminale domein en herschikt nabijgelegen lussen in het katalytische domein. Deze choreografie opent twee toegangspoorten zodat glutamine kan worden verwerkt en vormt tijdelijk een regio die het hoogenergetische tussenproduct stabiliseert dat nodig is voor het verbreken van bindingen.
Chemie koppelen via beweging
Terwijl de reactie vordert, wacht het enzym niet simpelweg af; het gebruikt elke chemische stap als een signaal. Zodra er een covalent thioester-tussenproduct ontstaat in het ammoniakproducerende domein, worden de eerdere bewegingen gedeeltelijk omgekeerd. Dit ontspant de centrale lus en herpositioneert de poorten om ontsnappingsroutes af te sluiten, terwijl twee extra poorten aan weerszijden van de tunnel opendraaien. Subtiele verschuivingen in een handvol “flessenhals”-residuen verwijden de binnenste doorgang, waardoor een ammoniakmolecuul rechtstreeks door de tunnel naar het tweede actieve centrum kan reizen, waar het reageert met het gevangen tussenproduct om het uiteindelijke product te vormen. Het muteren van de poortresiduen veroorzaakt lekkage van ammoniak of ontkoppeling van de twee helften van de reactie, wat bevestigt dat dit poort- en kanaalsysteem essentieel is voor efficiënte katalyse.
Van structurele inzichten naar therapeutische wegen
Door FGAMS te volgen gedurende zijn katalytische cyclus geeft de studie een gedetailleerd beeld van hoe domeinbewegingen, flexibele lussen, interne poorten en een tijdelijk tunnelpaadje zijn gekoppeld om de chemie te coördineren. Voor een algemeen publiek is de kernboodschap dat het enzym werkt als een kleine programmeerbare fabriek: het opent zijn deuren en interne lopende band alleen wanneer alle juiste onderdelen aanwezig zijn, wat snelheid en veiligheid garandeert. Omdat FGAMS de purineproductie in kankercellen ondersteunt en geassocieerd is met slechte overleving bij levertumoren, bieden de structurele blauwdrukken en nieuw geïdentificeerde controlepunten meerdere aanknopingspunten voor het ontwerpen van geneesmiddelen die de tunnel blokkeren, de poorten bevriezen of sleutel-tussenproducten vastzetten, wat mogelijk leidt tot een nieuwe klasse gerichte kankertherapieën.
Bronvermelding: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Trefwoorden: purinebiosynthese, allosterische regulatie, ammoniakkanalisatie, kankermetabolisme, cryo-EM-structuur