Clear Sky Science · nl
Moleculair werkingsmechanisme van het kleine molecuul SMT-738 op de bacteriële lipoproteïnetransporter LolCDE
Waarom dit nieuwe antibioticum ertoe doet
Naarmate hospitalere infecties onze beste antibiotica blijven ontwijken, hebben artsen dringend medicijnen nodig die gevaarlijke bacteriën doden zonder de nuttige microben die we dragen te verwoesten. Deze studie licht toe hoe een veelbelovend experimenteel middel, SMT-738, een cruciale transportmachine in de buitenste laag van moeilijk te behandelen bacteriën lamlegt. Door precies te laten zien waar en hoe dit middel de machine blokkeert, wijst het werk de weg naar gerichtere antibiotica die superbugs raken terwijl veel van het darmmicrobioom gespaard blijft.
Het buitenste pantser van schadelijke bacteriën
Veel van de zorgwekkendste ziekenhuispathogenen behoren tot de groep die bekendstaat als Gramnegatieve bacteriën. Ze zijn moeilijk te doden omdat ze zich omhullen met een dubbel gelaagd buitenpantser. Deze buitenste laag wordt opgebouwd en in stand gehouden door verschillende moleculaire machines die belangrijke bouwstenen van het binnenmembraan, waar ze worden gemaakt, naar het oppervlak verplaatsen. Een belangrijke categorie lading bestaat uit lipoproteïnen, die helpen het buitenoppervlak intact te houden en processen ondersteunen zoals nutriëntopname en antibioticaresistentie. Een transportsysteem genaamd de Lol-route, en in het bijzonder een pomp genaamd LolCDE, onttrekt lipoproteïnen uit het binnenmembraan en geeft ze door aan chaperonnes die ze naar het buitenoppervlak afleveren. Omdat deze stappen essentieel zijn, vormen ze aantrekkelijke doelen voor nieuwe antibiotica.
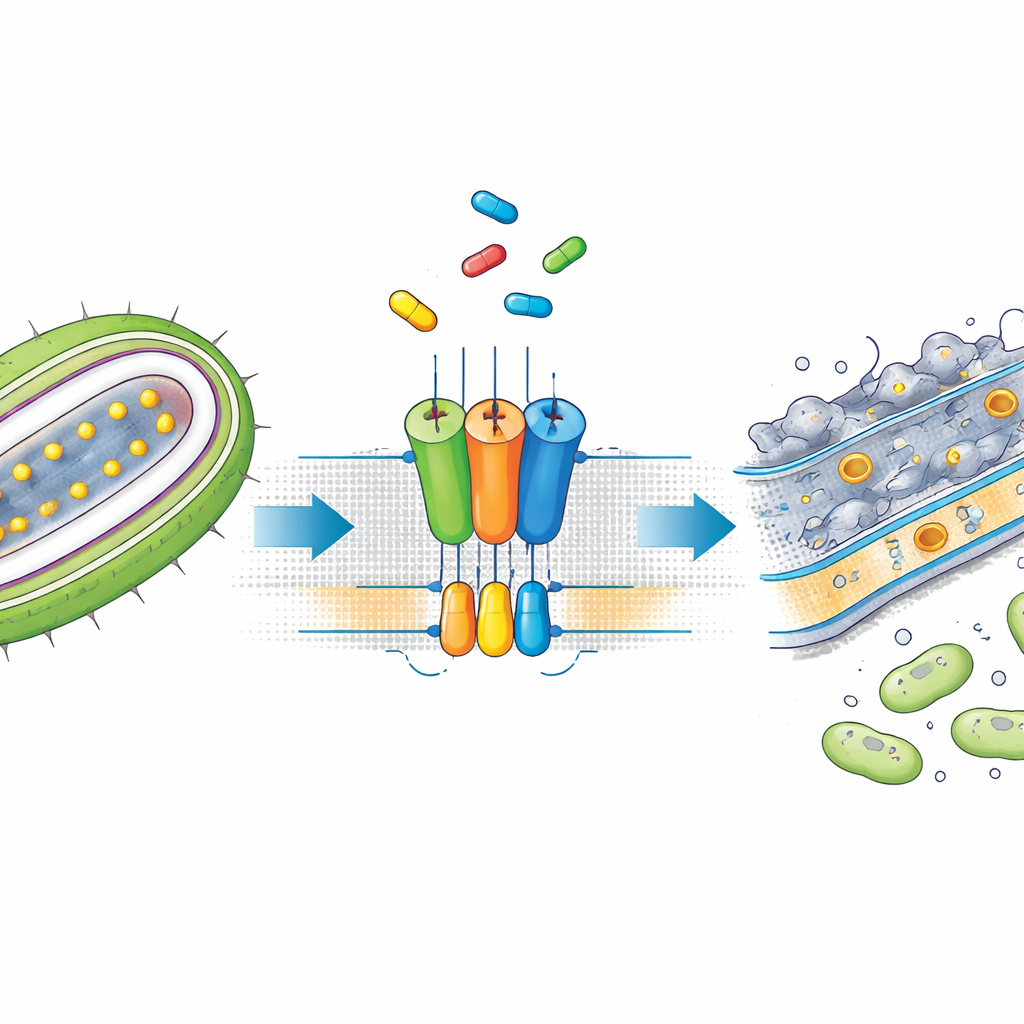
Een klein molecuul dat de lopende band stopt
SMT-738 kwam uit eerdere screenings naar voren als een krachtige remmer van Gramnegatieve ziekteverwekkers uit de familie Enterobacteriaceae, inclusief multiresistente stammen van Escherichia coli en Klebsiella pneumoniae. Toch was de precieze werkingswijze onduidelijk. De auteurs toonden eerst aan dat SMT-738 voorkomt dat een testlipoproteïne door LolCDE wordt vrijgegeven in geconstrueerde bacteriën, waarmee werd bevestigd dat het middel de transportstap daadwerkelijk stilzet. Belangrijk is dat bacteriën met bepaalde mutaties in de genen voor het LolCDE-complex resistent werden tegen SMT-738, wat suggereert dat het middel rechtstreeks aan deze pomp bindt. Deze observaties vormden de basis voor een structurele diepgaande analyse van hoe de verbinding met de transporter interageert.
De pomp van binnenuit blokkeren
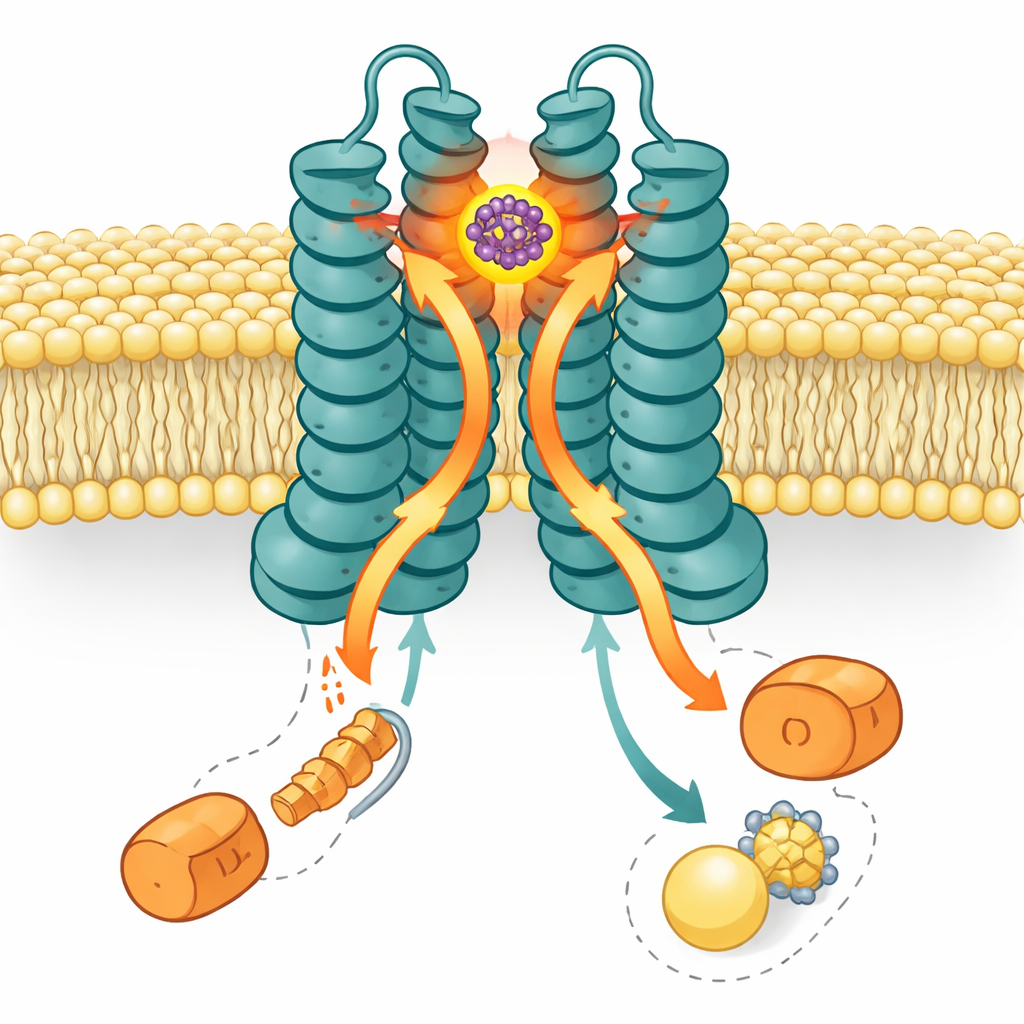
Met behulp van hoge-resolutie cryo-elektronenmicroscopie maakten de onderzoekers een driedimensionale opname van LolCDE met SMT-738 vergrendeld in positie. De structuur toont het middel geklemd in een pocket aan het periplasmatische uiteinde—de zijde naar de ruimte tussen binnen- en buitenmembraan—tussen twee kerndelen, LolC en LolE. Deze plaats overlapt met het normale aanknoopgebied voor lipoproteïne-lading. Wanneer SMT-738 deze pocket bezet, verschuiven omringende aminozuren in LolC en LolE tot ongeveer een nanometer. Die verschuivingen veroorzaken sterische botsingen met de plaats waar het lipoproteïne en zijn vetstaarten normaal zouden zitten, waardoor lading effectief wordt verhinderd de pomp binnen te gaan. Het muteren van veel van deze pocketrande-residuen verzwakte of verhinderde de binding van het medicijn of maakte bacteriën resistent, wat mooi overeenkomt met het structurele beeld.
Het veroorzaken van een eenzijdige uitval
Het verhaal stopt niet bij de bindingsplaats. LolCDE wordt aangedreven door twee kopieën van een motoronderdeel genaamd LolD, dat aan de cytoplasmatische zijde zit en ATP verbrandt om transport mogelijk te maken. Opmerkelijk is dat in de SMT-738–gebonden structuur slechts één LolD bevestigd bleef; de partner-LolD was losgeraakt. Biochemische gels en ATPase-assays bevestigden dat binding van SMT-738 leidt tot verlies van één LolD en de energieomzetting van de pomp sterk vermindert. Computersimulaties van de transporter in een membraan ondersteunden dit beeld: toen SMT-738 in zijn pocket ging zitten, verspreidden conformationele veranderingen zich naar beneden en duwden de koppelschroeven die LolC en LolE met LolD verbinden. Deze verschuivingen duwden de LolD die aan LolC gebonden was in een ongunstige botsing, waardoor deze losschoot, terwijl de LolD aan LolE bleef zitten. Het resultaat is een asymmetrische, “vastgezette” machine die lipoproteïnen niet langer kan verplaatsen.
Waarom sommige bacteriën worden geraakt en andere gespaard
SMT-738 heeft een wenselijke eigenschap: het valt Enterobacteriaceae die resistent zijn tegen medicijnen krachtig aan, maar laat veel andere Gramnegatieve soorten in de darm grotendeels ongemoeid. Om deze selectiviteit te begrijpen vergeleek het team de sequenties van LolE van gevoelige en resistente bacteriën en concentreerde zich op posities die SMT-738 raken. Twee residuen in LolE, vooral één overeenkomstig positie D264 in E. coli, sprongen eruit. Bij gevoelige pathogenen kwamen deze posities overeen met de drug-contactversie in E. coli, terwijl ze bij veel resistente darmcommensalen door andere aminozuren waren vervangen. Toen de onderzoekers E. coli zo construeerden dat deze substituties aanwezig waren, werden de bacteriën sterk resistent tegen SMT-738 terwijl ze nog steeds LolCDE produceerden. Simulaties suggereerden dat deze veranderingen de lokale flexibiliteit rond de pocket wijzigen, waardoor de bindingscapaciteit van SMT-738 afneemt. Interessant genoeg vertrouwde een andere LolCDE-remmer, lolamicin, op slechts deels overlappende contactpunten en vertoonde een ander resistentiepatroon, wat wijst op verschillende manieren om dezelfde pomp te targeten.
Nieuwe bouwplannen voor toekomstige antibiotica
Door structurele beeldvorming, mutatiescans, biochemische tests en computersimulaties te combineren, laat dit werk zien dat SMT-738 niet slechts een stop in een kanaal is. In plaats daarvan klemt het middel vast aan de periplasmatische zijde van de LolCDE-pomp, blokkeert de lipoproteïne-ingang en veroorzaakt vervolgens langafstandsschommelingen die één van de twee motorunits doen losschieten, waardoor de transporter in een niet-werkende toestand bevriest. Dit “allostere vastzet”-mechanisme vertegenwoordigt een nieuwe manier om een bacteriële machine uit te schakelen en helpt verklaren waarom SMT-738 zich kan richten op gevaarlijke pathogenen terwijl veel van het microbioom gespaard blijft. De gedetailleerde kaart van de bindingspocket en het sleutelresidu voor selectiviteit in LolE bieden nu een rationeel ontwerpklare blauwdruk voor het ontwikkelen van volgende-generatie antibiotica die deze kwetsbaarheid met nog grotere potentie en precisie benutten.
Bronvermelding: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Trefwoorden: antibioticaresistentie, Gramnegatieve bacteriën, lipoproteïnentransport, LolCDE-remmer, cryo-EM-structuur