Clear Sky Science · nl
De photolyase/cryptochrome van Aspergillus nidulans detecteert oxidatieve stress en verhuist van de kern naar mitochondriën
Hoe schimmels licht en stress waarnemen
Zonlicht houdt planten en schimmels in leven, maar brengt ook risico’s zoals DNA-schade en schadelijke zuurstofhoudende chemicaliën. Deze studie onderzoekt hoe een veelvoorkomende schimmel, Aspergillus nidulans, één eiwit — CryA — gebruikt om zowel licht als oxidatieve stress te detecteren en zichzelf te beschermen. Begrijpen hoe deze “duale sensor” werkt verdiept niet alleen onze kennis van hoe microben met vijandige omgevingen omgaan, maar kan ook inzicht geven in hoe cellen in het algemeen signalen tussen hun kern en hun energieproducerende mitochondriën coördineren.
Een blauwlicht-reparatie-enzym met een verborgen rol
CryA behoort tot een familie eiwitten die bekendstaat om het herstellen van DNA-schade veroorzaakt door ultraviolette straling. Deze eiwitten, photolyases en cryptochromen genoemd, gebruiken een lichtabsorberende molecule (een flavine) om blauw licht te benutten en beschadigde DNA-basen te repareren. De onderzoekers bevestigden dat CryA de klassieke architectuur van een DNA-reparatie-enzym heeft, de gebruikelijke lichtinzamelende cofactoren bindt en in evolutionaire bomen met bekende photolyases clustert. Op grond daarvan alleen zou CryA een routinematig reparatie-instrument lijken. Eerder werk suggereerde echter al dat het ook de ontwikkeling van de schimmel beïnvloedt en zich meer als een lichtgereguleerde schakelaar gedraagt dan als een simpel moleculair werktuig.
Een hoofdregelaar voor lichtgevoelige genen
Om CryA’s regulerende kant te onthullen, volgde het team waar het eiwit zich in de cel bevindt en hoe veranderingen in de hoeveelheid CryA de schimmelgroei beïnvloeden. Ze ontdekten dat CryA onder normale omstandigheden in de kern ophoopt, waar het DNA is opgeslagen. Bij verwijdering van het cryA-gen produceerde de schimmel meer seksuele structuren; bij geforceerde overproductie van CryA werd de vorming van de gewone aseksuele sporen vrijwel geheel onderdrukt, waardoor bleekgekleurde, pluizige kolonies ontstonden. Genexpressietests toonden aan dat veel door licht geactiveerde en ontwikkeling-gerelateerde genen te sterk werden aangezet zonder CryA en te zwak bij overexpressie van CryA. Gezamenlijk onthullen deze resultaten CryA als een negatief feedbackelement: licht verhoogt cryA-niveaus, CryA verplaatst zich vervolgens naar de kern en dempt de licht- en ontwikkeling-geïnduceerde genen, waardoor wordt voorkomen dat de respons ontspoort. 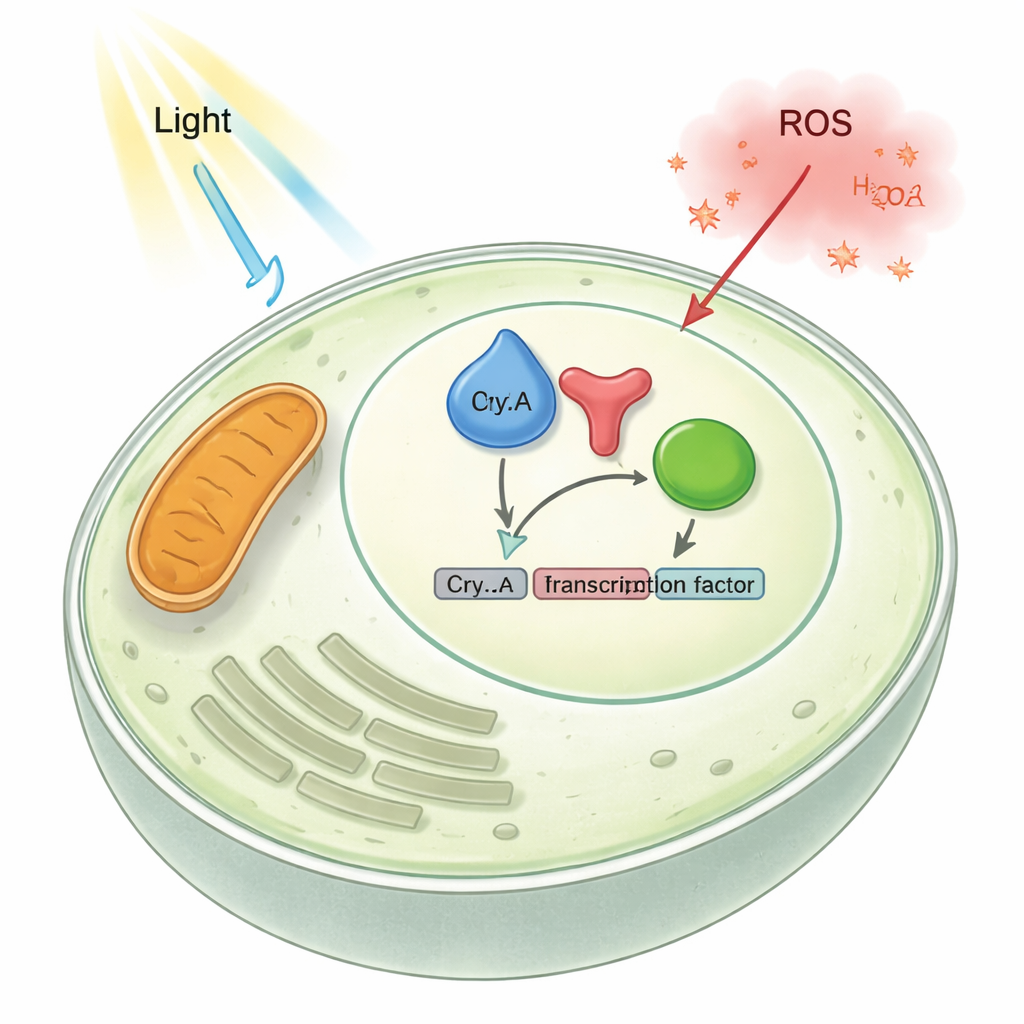
Onderlinge communicatie met de belangrijkste licht- en stressroutes
De schimmel vertrouwt al op een andere photoreceptor, een roodlichtsensor genaamd fytochroom (FphA), en op een stressroute die eindigt in een transcriptiefactor genaamd AtfA. Met behulp van eiwit–eiwit interactietesten in levende cellen en met gezuiverde eiwitten toonden de onderzoekers aan dat CryA fysiek zowel FphA als AtfA in de kern bindt. Wanneer cryA werd verwijderd, werden genen die normaal gesproken door fytochroom via rood licht geactiveerd worden sterker tot expressie gebracht; bij overexpressie van cryA werden ze moeilijker aan te zetten. Chromatine-experimenten wezen uit dat in afwezigheid van CryA een sleutelligen dat op licht reageert meer activerende histonmerken droeg, wat suggereert dat CryA normaal gesproken de chromatine-openende activiteit veroorzaakt door fytochroom afremt. In feite knijpt CryA zowel de lichtsensor als de downstream transcriptiefactor samen, en fungeert het als een gedeelde rem voor licht- en stresssignalen.
Een snelle stresssensor die naar mitochondriën springt
Oxidatieve stress — een overschot aan reactieve zuurstofsoorten zoals waterstofperoxide — vormt een voortdurend gevaar voor cellen. De auteurs vonden dat dergelijke stress, net als licht, de expressie van cryA verhoogt. Opvallend was dat bij toevoeging van waterstofperoxide CryA in minder dan een minuut van de kern naar de mitochondriën verhuisde. Deze sprong vereiste een korte, flexibele aanhangsel aan de N-terminus van het eiwit en, in het bijzonder, een enkele cysteïne-aminozuur daarin. Wanneer die cysteïne was veranderd in een ander residu, kon CryA bij stress de kern niet meer verlaten. Het afkappen van de N-terminale staart dwong CryA permanent naar de mitochondriën te verhuizen. Deze geconstrueerde stammen reageerden verschillend op oxidanten: nucleus-only en mitochondriën-only versies van CryA veranderden de resistentie van de schimmel tegen waterstofperoxide en menadion en herschikten de expressie van antioxidantgenen. De bevindingen suggereren dat CryA meer doet dan stress detecteren — het helpt mogelijk de communicatie tussen mitochondriën en de kern te coördineren zodat antioxidantverdedigingen worden afgestemd op het type en niveau van schade. 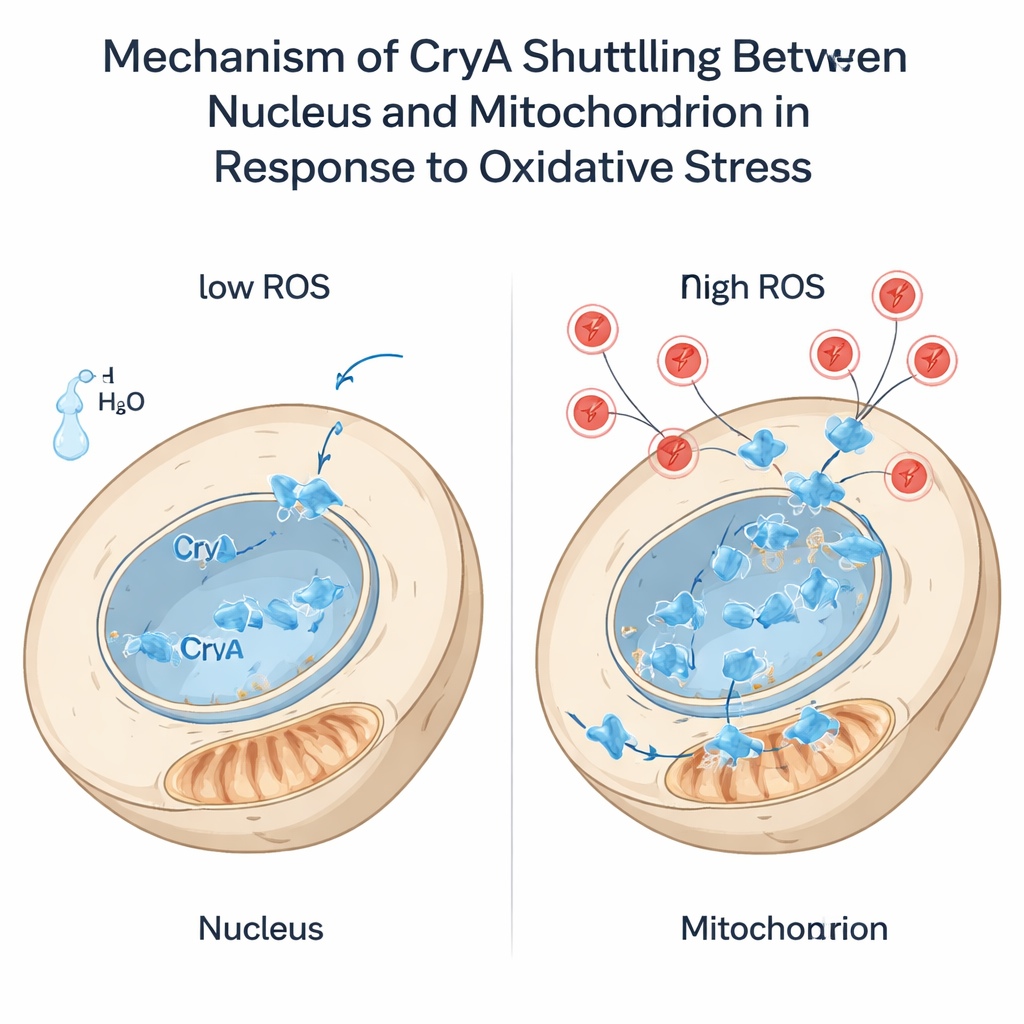
Waarom dit belangrijk is
Voor een niet-specialist kan CryA worden opgevat als een cellulaire verkeersregelaar die zowel het externe licht als de interne oxidatieve stress in de gaten houdt en vervolgens beslist wanneer groei, ontwikkeling en genactiviteit vertraagd moeten worden. Door tussen kern en mitochondriën te shuttelen en zich in te schakelen in belangrijke signaalroutes voorkomt het dat de schimmel overreageert op licht of stress, terwijl het toch een snelle beschermende respons mogelijk maakt. Vergelijkbare eiwitten en mechanismen bestaan in veel organismen, dus dit werk biedt een venster op hoe levende cellen omgevingssignalen en interne schadesignalen integreren om te overleven in een veranderende wereld.
Bronvermelding: Landmark, A., Rudolf, T., Hundshammer, K. et al. The photolyase/cryptochrome of Aspergillus nidulans senses oxidative stress and shuttles from nuclei to mitochondria. Nat Commun 17, 1483 (2026). https://doi.org/10.1038/s41467-026-69403-2
Trefwoorden: lichtwaarneming, oxidatieve stress, cryptochrome, mitochondriën, schimmelontwikkeling