Clear Sky Science · nl
Myoferlin is een component van laatstadium vRNP-verkeersblaasjes voor omhulde RNA-virussen
Waarom dit van belang is voor alledaagse gezondheid
Seizoensgriep en andere luchtweginfecties lijken misschien routine, maar samen doden ze jaarlijks miljoenen mensen wereldwijd. Veel van deze virussen, waaronder influenza A en respiratoir syncytieel virus (RSV), ontlopen al vaccins en antivirale middelen door snel te muteren. Deze studie bekijkt in plaats daarvan iets wat virussen niet makkelijk kunnen veranderen: de menselijke celmachine die ze kapen om uit geïnfecteerde cellen te ontsnappen. Door een gedeelde kwetsbaarheid in die machinerie bloot te leggen, wijst het werk op toekomstige geneesmiddelen die een hele reeks luchtweginfecties tegelijk kunnen afzwakken.
Een cellulair bezorgtraject dat virussen uitbuiten
Onze luchtwegcellen hergebruiken voortdurend delen van hun buitenmembraan via een proces dat recycling heet. Kleine membraanblaasjes, of vesikels, vervoeren lading van binnen de cel terug naar het oppervlak, gestuurd door een familie eiwitten die samen bekendstaan als Rab11. Influenzavirus A, RSV en een verwant virus genaamd Sendai benutten deze route laat in de infectie. Ze laden hun genetische lading, verpakt als ribonucleoproteïnecomplexen, op Rab11-bevattende vesikels die ze naar de bovenkant (luchtweggerichte zijde) van de cel vervoeren, waar nieuwe virusdeeltjes uitknoppen en zich verspreiden. Tot nu toe was Rab11 de enige gastheerfactor die duidelijk gedeeld werd door deze verkeersblaasjes, waardoor er een groot gat bleef in ons begrip van hoe ze zich vormen en functioneren.
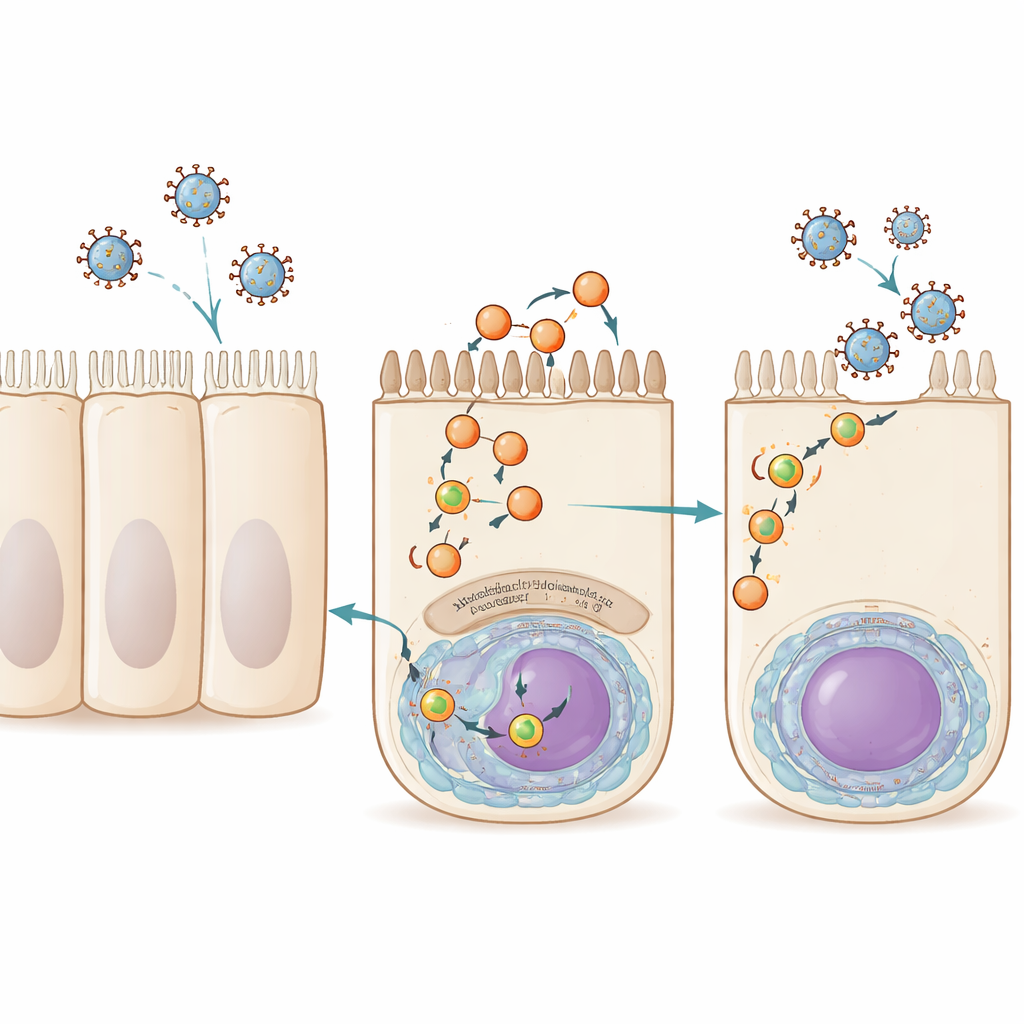
Een nieuwe speler vinden: myoferlin
De onderzoekers begonnen door te vragen welke menselijke eiwitten fysiek geassocieerd zijn met het genoomverpakkingsmachinery van influenza op verschillende momenten tijdens de infectie. Ze bouwden een influenzavirus A waarvan de polymerase een moleculaire tag droeg, en gebruikten vervolgens massaspectrometrie om menselijke eiwitten te kataloquiseren die aan dit complex gebonden waren vroeg en laat in de infectie. Onder honderden kandidaten stak er één uit op latere tijdpunten: myoferlin, een groot membraan-geassocieerd eiwit dat eerder in verband is gebracht met spierontwikkeling, endocytose en membraanreparatie. Wanneer het team myoferlinniveaus in longafgeleide cellen verminderde met behulp van kleine interfererende RNA's of het blokkeerde met een klein-molecuul remmer, produceerden de cellen nog steeds normaal viraal RNA en virale eiwitten, maar gaven ze veel minder infectieuze influenzadeeltjes af. Dit wees erop dat myoferlin niet nodig is voor het kopiëren van het virale genoom, maar cruciaal is voor de latere stadia wanneer nieuwe virussen worden geassembleerd en de cel verlaten.
Myoferlin reist mee met viraal materiaal
Hoge-resolutie beeldvorming onthulde waar myoferlin zich bevindt tijdens de infectie. In niet-geïnfecteerde cellen overlapt myoferlin grotendeels met Rab11-positieve recyclingvesikels, zowel nabij de kern als naar de rand van de cel toe, en het verlies van elk van beide eiwitten verstoort de normale distributie van het andere. Tijdens influenza-infectie wordt het Rab11-netwerk dramatisch herschikt in vergrote, onregelmatige vesikels die virale ribonucleoproteïnen dragen. Myoferlin blijft aanwezig in deze geremodelde vesikels en toont sterke co-localisatie met het virale genoom en Rab11. Wanneer het team een geneesmiddel gebruikte dat virale genoomcomplexen en hun drager-vesikels laat samenklonteren, werd myoferlin in dezelfde aggregaten meegenomen, wat bevestigt dat het een ingebouwd onderdeel is van deze laatstadium verkeersstructuren en niet slechts toevallig in de buurt zit.
Een gedeeld knooppunt voor meerdere luchtweginfecties
De studie vroeg vervolgens of deze afhankelijkheid van myoferlin uniek is voor influenza of breder gedeeld wordt. Het wegknippen van myoferlin in longcellen geïnfecteerd met RSV of Sendai-virus veroorzaakte opnieuw een sterke daling in het aantal vrijgegeven infectieuze virussen, zonder de virale RNA-niveaus te verlagen. Single-molecule beeldvorming liet de genomen van beide virussen samenklonteren met myoferlin en Rab11 in cytoplasmatische plekken die waarschijnlijk transportschijven vertegenwoordigen in plaats van replicatiefabrieken. Dit patroon ondersteunt een verenigend beeld: verschillende omhulde luchtweg-RNA-virussen, ondanks diverse levenswijzen, convergeren op hetzelfde Rab11–myoferlin vesikelsysteem wanneer het tijd is om hun voltooide genomen naar het celoppervlak te verplaatsen voor verpakking en uitgang.
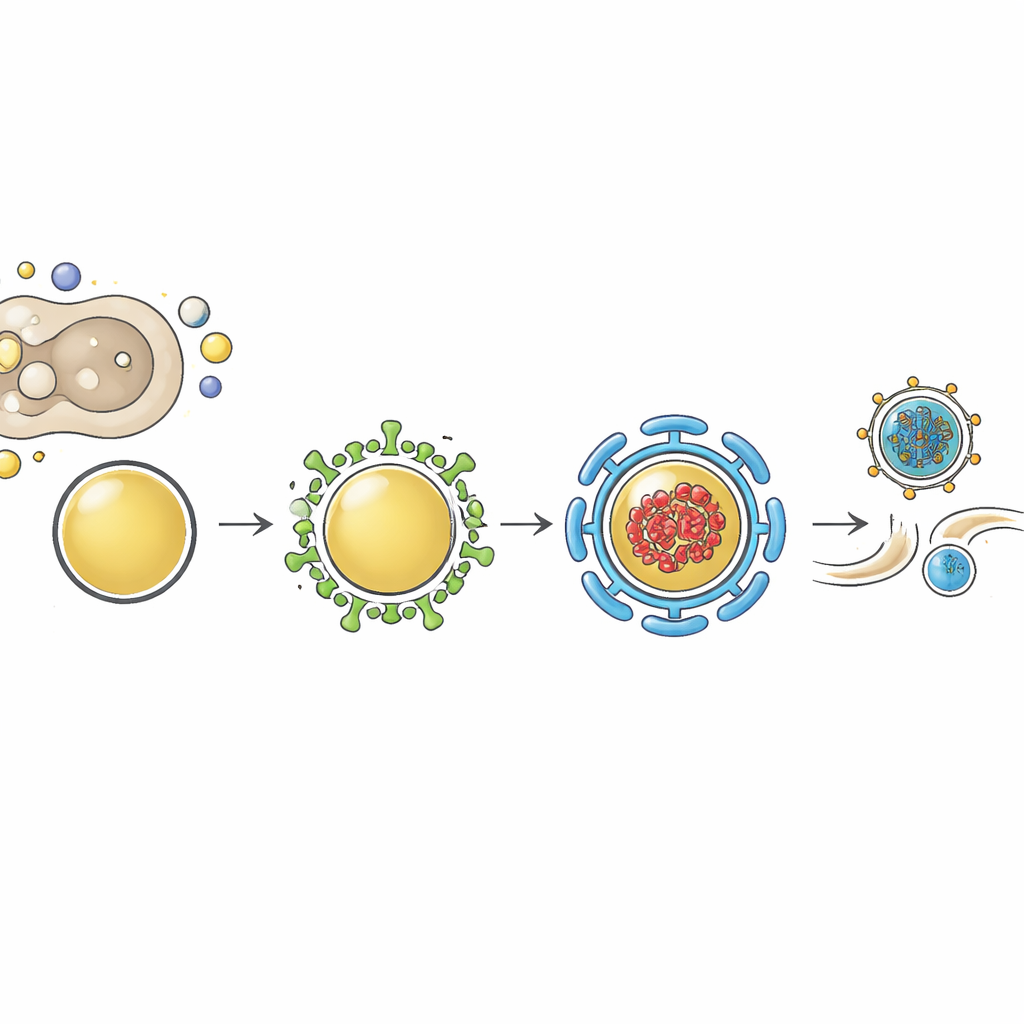
Hoe myoferlin virusdragende vesikels vormt
Myoferlin bestaat uit meerdere "C2"-domeinen die membranen en partner-eiwitten kunnen binden. Eerder werk toonde aan dat een van deze domeinen een familie van membraan-herschikkende eiwitten genaamd EHD's aangaat. In deze studie werden fluorescerend gelabelde EHD1 en EHD2 gevonden binnen dezelfde geremodelde vesikels die influenzagenomen en Rab11 dragen, vooral wanneer deze vesikels experimenteel werden geclusterd. Het verlagen van EHD2-niveaus, net als het verlagen van myoferlin, verlaagde de influenzaverdiensten zonder de genomereplicatie te beïnvloeden. Bovendien zorgde het verwijderen van myoferlin ervoor dat EHD2-eiwitniveaus daalden, wat suggereert dat myoferlin helpt EHD2 te stabiliseren of correct te positioneren op membranen. De auteurs stellen voor dat myoferlin op Rab11-positieve vesikels zit en EHD-eiwitten rekruteert om hun membranen te boetseren, waarmee de vorming van gespecialiseerde "onregelmatig gecoate vesikels" wordt voltooid die geoptimaliseerd zijn voor het transporteren van viraal materiaal naar afknoppingsplaatsen.
Wat dit betekent voor toekomstige antivirale strategieën
Samengevat plaatsen de bevindingen myoferlin als een centrale organisator van een gastheer-recyclingroute waarop veel omhulde luchtwegvirussen vertrouwen in een kritisch laat stadium. Omdat het richten op virale eiwitten alleen vaak leidt tot snelle resistentie, zijn gastheerfactoren die door meerdere virussen worden hergebruikt aantrekkelijke geneesmiddeldoelwitten. Het verstoren van de functie van myoferlin, of zijn samenwerking met Rab11 en EHD-eiwitten, zou in principe de verspreiding van diverse pathogenen kunnen vertragen of blokkeren, van influenza en RSV tot andere Rab11-afhankelijke virussen zoals sommige coronavirussen. Er is nog veel werk nodig om dit concept naar veilige therapieën te vertalen, maar de studie levert een gedetailleerde kaart van een gedeelde ontsnappingsroute van virussen — en zet myoferlin in de schijnwerpers als een veelbelovend knelpunt langs dat pad.
Bronvermelding: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Trefwoorden: influenza, ademhalingsvirussen, vesiculair verkeer, gastheerverwekkers, myoferlin