Clear Sky Science · nl
Gekweekte exosoom-nanovesikels voor de aflevering van antilichamen bij de behandeling van inflammatoire darmziekte
Nieuwe hoop voor een hardnekkige darmaandoening
Inflammatoire darmaandoeningen (IBD) kunnen het dagelijks leven veranderen in een voortdurende strijd tegen pijn, diarree en vermoeidheid, en verhogen bovendien op lange termijn het risico op darmkanker. Veel huidige medicijnen dempen oplevingen, maar herstellen niet echt de verkeerde immuunreacties die de ziekte aansturen, waardoor symptomen vaak terugkeren. Deze studie introduceert een slim ontworpen ‘slimme’ nanopartikel dat via de bloedbaan reist, ontstoken delen van de darm vindt en een tweedelige behandeling aflevert die zowel schadelijke ontsteking afremt als langdurige immuunbalans helpt herstellen.
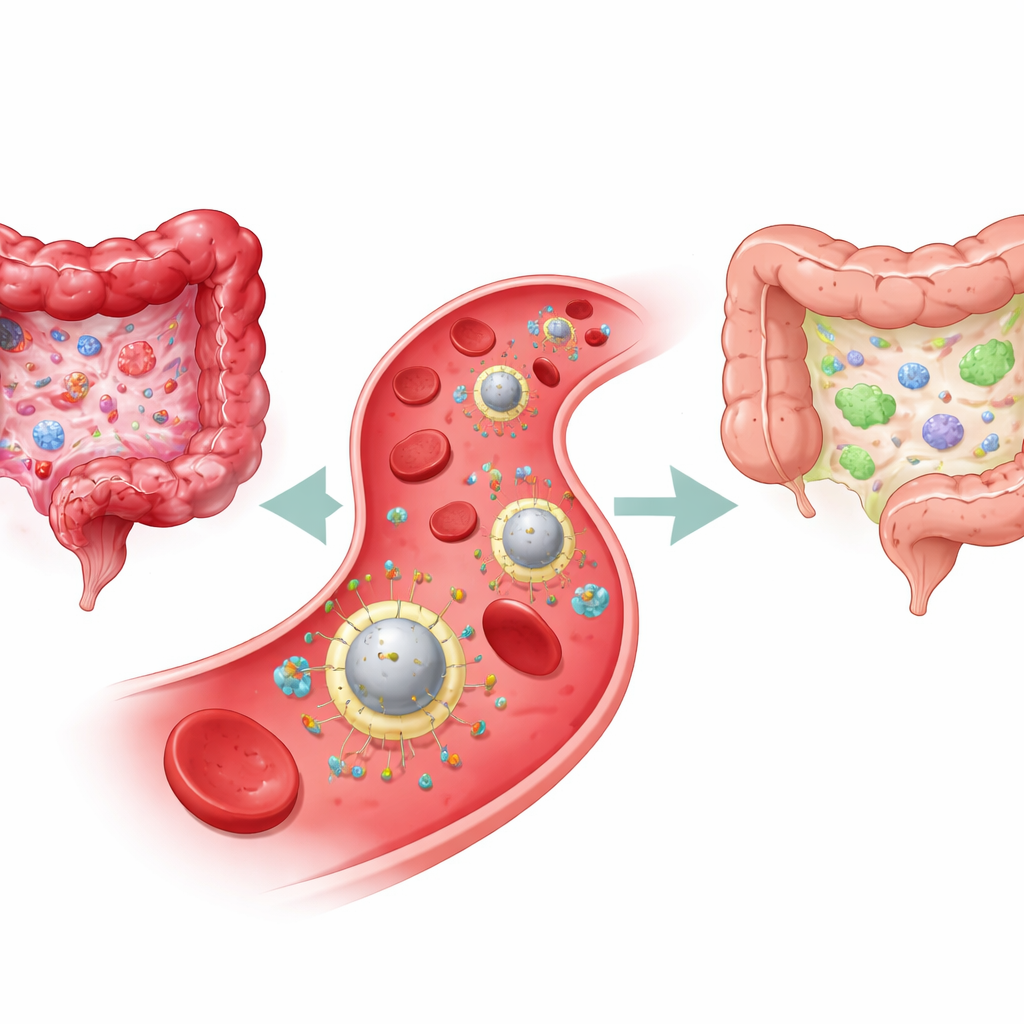
Waarom huidige behandelingen tekortschieten
IBD, waaronder de ziekte van Crohn en colitis ulcerosa, ontstaat door een chronisch trekken en duwen in het immuunsysteem van de darm. Aan de ene kant staan agressieve immuuncellen en ontstekingsmoleculen die het darmslijmvlies beschadigen; aan de andere kant staan regulatorische cellen die deze reactie normaal gesproken onder controle houden. Standaardtherapieën—zoals steroïden, immunosuppressiva en biologische geneesmiddelen—proberen voornamelijk de ontsteking overal in het lichaam te dempen. Ze kunnen symptomen verlichten, maar doen vaak weinig om de onderliggende immuunbalans te herstellen, en brede immuunsuppressie kan het risico op infecties verhogen. Zelfs nieuwere antilichaamtherapieën die een belangrijk ontstekingssignaal, interleukine-23 (IL-23), blokkeren helpen maar een deel van de patiëntenpopulatie en circuleren nog wijdverspreid, niet alleen daar waar ze nodig zijn.
Een doelgerichte, van vorm veranderende geneesmiddel ontwikkelen
De onderzoekers wilden een behandeling ontwerpen die zich meer gedraagt als een levende cel dan als een eenvoudig medicijn. Ze begonnen met kleine blaasje die regulatoire T-cellen natuurlijk afgeven—immuuncellen die tolerantie en vredeshandhaving bevorderen. Deze blaasje, exosomen genoemd, dragen eiwitten en genetisch materiaal die andere immuuncellen subtiel kunnen aansturen naar een kalmerende modus. Het team fuseerde deze exosomen met fragmenten van plaatjesmembraan, gebruikmakend van de eigenschap van plaatjes om aan beschadigde bloedvaten in ontstoken weefsel te kleven. Op het oppervlak van deze hybride schaal bevestigden ze IL-23-blokkerende antilichamen met behulp van een moleculaire ‘draad’ die kan worden doorgeknipt door enzymen (matrixmetalloproteïnasen) die alleen overvloedig aanwezig zijn in ontstoken darmweefsel. Het resultaat, PrEXO-a23 genoemd, is een nanovesikel dat in het bloed circuleert, zich vasthecht aan beschadigde darmvaten en vervolgens zijn antilichaam-lading alleen loslaat waar de ziekte actief is.
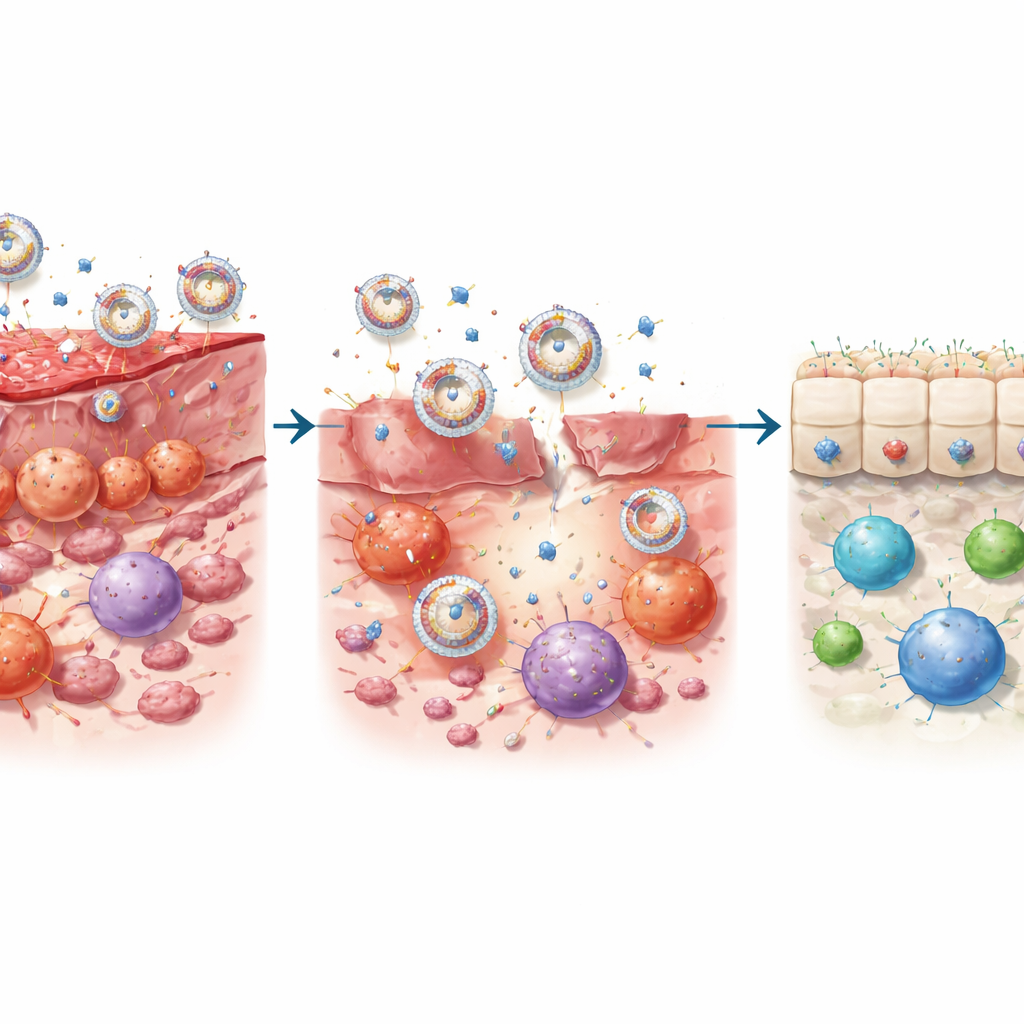
Het immuunmilieu van de darm heropvoeden
In celstudies presteerde PrEXO-a23 beter dan ofwel het antilichaam of de exosomen afzonderlijk. Het verminderde sterk de vorming van inflammatoire T-helper 17 (Th17)-cellen en de afgifte van schadelijke cytokinen die het darmslijmvlies beschadigen, terwijl het menselijke darmepitheelcellen beschermde tegen celdood. Tegelijkertijd duwde het dendritische cellen—poortwachters die T-cellen instrueren—weg van een vijandige, activerende staat richting een ‘tolerante’ staat die de groei van regulatorische T-cellen bevordert. In muismodellen van colitis homden de nanovesikels efficiënt naar ontstoken colonweefsel, werden ze opgenomen door meerdere immuunceltypen en gaven ze antilichamen vrij als reactie op lokale enzymactiviteit. Deze dubbele werking—het blokkeren van IL-23-gedreven ontsteking en het versterken van tolerantiebevorderende signalen—bracht ontstekingsmarkers dicht bij normaal en herstelde een gezondere verdeling van T-celtypes.
Weefsel herstellen en lange termijn schade voorkomen
Muizen met chemisch geïnduceerde colitis die PrEXO-a23 kregen verloren minder gewicht, hadden langere, gezondere darmen en vertoonden minder miltvergroting, een teken van systemische ontsteking. Microscopisch onderzoek toonde een bewaarde darmarchitectuur en strakkere verbindingen tussen epitheellaagcellen, wat duidt op een herstelde barrière. De behandeling hielp ook de darmflora te herbalanceren, door families te vergroten die met darmgezondheid geassocieerd zijn en die te verminderen die met ziekte worden geassocieerd. In een ernstiger model dat de progressie van chronische colitis naar darmkanker nabootst, verlichtte PrEXO-a23 niet alleen de aanhoudende ontsteking maar voorkwam het volledig de ontwikkeling van tumoren en remde het de verdikking en verharding van de darmwand die kenmerkend is voor fibrose. Moleculaire analyses wezen op herstel van beschermende p53-signaleringsroutes—een centrale beschermer tegen kanker—wat belangrijk bleek voor het anti-kanker effect.
Op weg naar slimmer, duurzamer IBD‑zorg
Voor de niet‑specialist is de kernboodschap dat dit werk verder gaat dan alleen het ‘afschakelen’ van ontsteking. Door gerichte bezorging, lokale afgifte van antilichamen en immuunkalmerende exosoomlading in één klein pakket te combineren, kalmeert PrEXO-a23 zowel actieve ziekte als helpt het het immuunsysteem opnieuw te trainen richting blijvende tolerantie. Bij muizen leidde dit niet alleen tot symptoomverlichting maar ook tot bescherming tegen littekenvorming en darmkanker, twee van de meest gevreesde complicaties van langdurige IBD. Hoewel er nog veel testen nodig zijn voordat zo’n therapie patiënten kan bereiken, laat de studie zien hoe biologisch geïnspireerde nanogeneesmiddelen op een dag mogelijk meer precieze, duurzame controle kunnen bieden over complexe immuunaandoeningen zoals IBD.
Bronvermelding: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Trefwoorden: inflammatoire darmaandoening, nanomedicine, immuuntolerantie, exosomen, preventie van colorectale kanker