Clear Sky Science · nl
Structurefouten in amyloïde-β-fibrillen stimuleren secundaire nucleatie
Waarom kleine onvolkomenheden in herseneiwitten ertoe doen
Bij Alzheimer en verwante hersenziekten klonteren bepaalde eiwitten samen tot lange, draadachtige structuren die amyloïde fibrillen worden genoemd. Deze fibrillen markeren niet alleen de ziekte; ze helpen ook bij het genereren van nieuwe, zeer toxische eiwitdeeltjes die hersencellen kunnen beschadigen. Deze studie stelt een eenvoudige maar belangrijke vraag: fungeren zeldzame structurele "fouten" in amyloïde fibrillen als de belangrijkste hete plekken die nieuwe schadelijke groei op gang brengen? Het antwoord kan wijzen op nieuwe manieren om deze aandoeningen te vertragen of te stoppen door slechts een paar kritieke locaties te richten in plaats van het hele eiwitoppervlak.
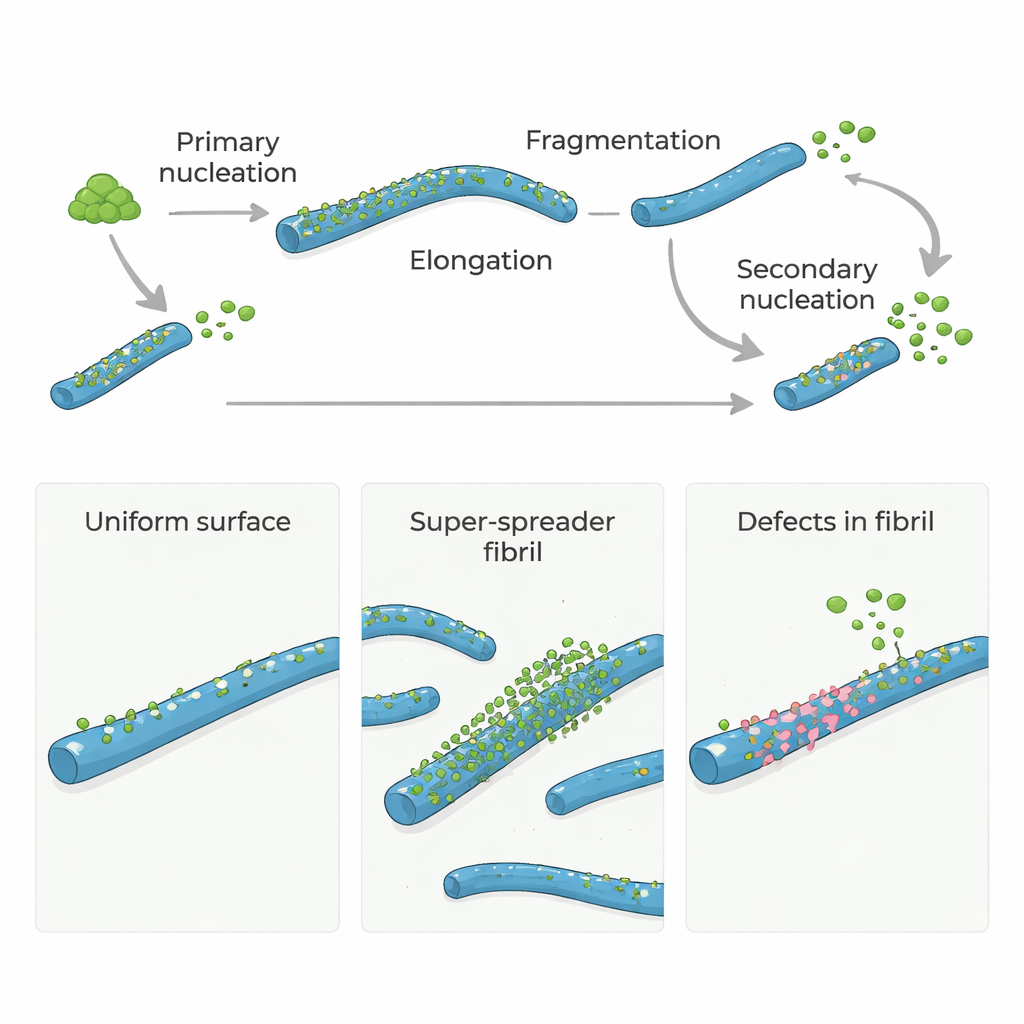
Van stil eiwit naar uit de hand lopende kettingreactie
Amyloïde-β (Aβ)-eiwitten, centraal bij de ziekte van Alzheimer, vormen zich normaal gesproken niet heel snel spontaan tot klonters. Om te beginnen moeten een paar monomeren langzaam samenkomen tot de eerste kleine fibrillen, een stap die primaire nucleatie wordt genoemd. Zodra deze initiële fibrillen bestaan, groeien ze snel doordat meer monomeren aan hun uiteinden toevoegen. Nog belangrijker is dat bestaande fibrillen nieuwe fibrillen op hun oppervlakken kunnen aantriggeren in een proces dat bekendstaat als secundaire nucleatie. Deze oppervlakgestuurde stap kan het systeem overspoelen met nieuwe fibrillen en kleine, toxische oligomeren, waardoor een trage druppelstroom verandert in een uit de hand lopende kettingreactie.
Zijn alle fibriloppervlakken even gevaarlijk?
Veel modellen gaan ervan uit dat het hele oppervlak van een amyloïde fibril even goed is in het katalyseren van secundaire nucleatie. Recente experimenten suggereerden echter dat slechts een klein deel van het oppervlak echt actief is. Om dit te onderzoeken gebruikten de auteurs een natuurlijke moleculaire "chaperon" genaamd Brichos, waarvan bekend is dat het secundaire nucleatie van Aβ40 en Aβ42 (twee belangrijke vormen van amyloïde-β) blokkeert. Door zorgvuldig te meten hoeveel fluorescent gelabeld Brichos aan fibrillen hecht, ontdekten ze dat het sterk bindt maar in zeer lage aantallen: ongeveer één Brichos-molecuul per 100–150 Aβ-moleculen in een fibril. Toch was deze spaarzame dekking voldoende om meer dan 90% van de secundaire nucleatie te onderdrukken, wat betekent dat slechts zeldzame, gelokaliseerde plekken — in plaats van het hele oppervlak — de productie van nieuwe toxische assemblages domineren.
Het onderzoeken van de rol van verborgen defecten
Deze bevindingen suggereerden dat de cruciale nucleatieplaatsen structurele defecten zouden kunnen zijn — kleine onregelmatigheden die zich vormen tijdens de groei van fibrillen, zoals verkeerd uitgelijnde lagen of gedeeltelijk blootgestelde binnenkernen. Om dit idee direct te testen, kweekt de groep Aβ40-fibrillen onder twee verschillende omstandigheden. De ene reeks, de "controle"-fibrillen, werd gevormd onder typische, sterk overs verzadigde condities die snelle groei en kinetische vergrendeling van defecten bevorderen. De andere reeks werd gemaakt met een langzaam, temperatuurgecontroleerd annealingsprotocol: fibrillen werden gegroeid bij een zeer lage effectieve aandrijvende kracht, dicht bij hun oplosbaarheidsgrens, waar incorrecte structuren kunnen oplossen of herstellen voordat ze vergrendeld raken. Hoge-resolutie cryo-elektronenmicroscopie liet zien dat beide reeksen fibrillen in grote lijnen identiek leken in vorm en twist, wat aangeeft dat het annealingsproces de basismorfologie niet veranderde.
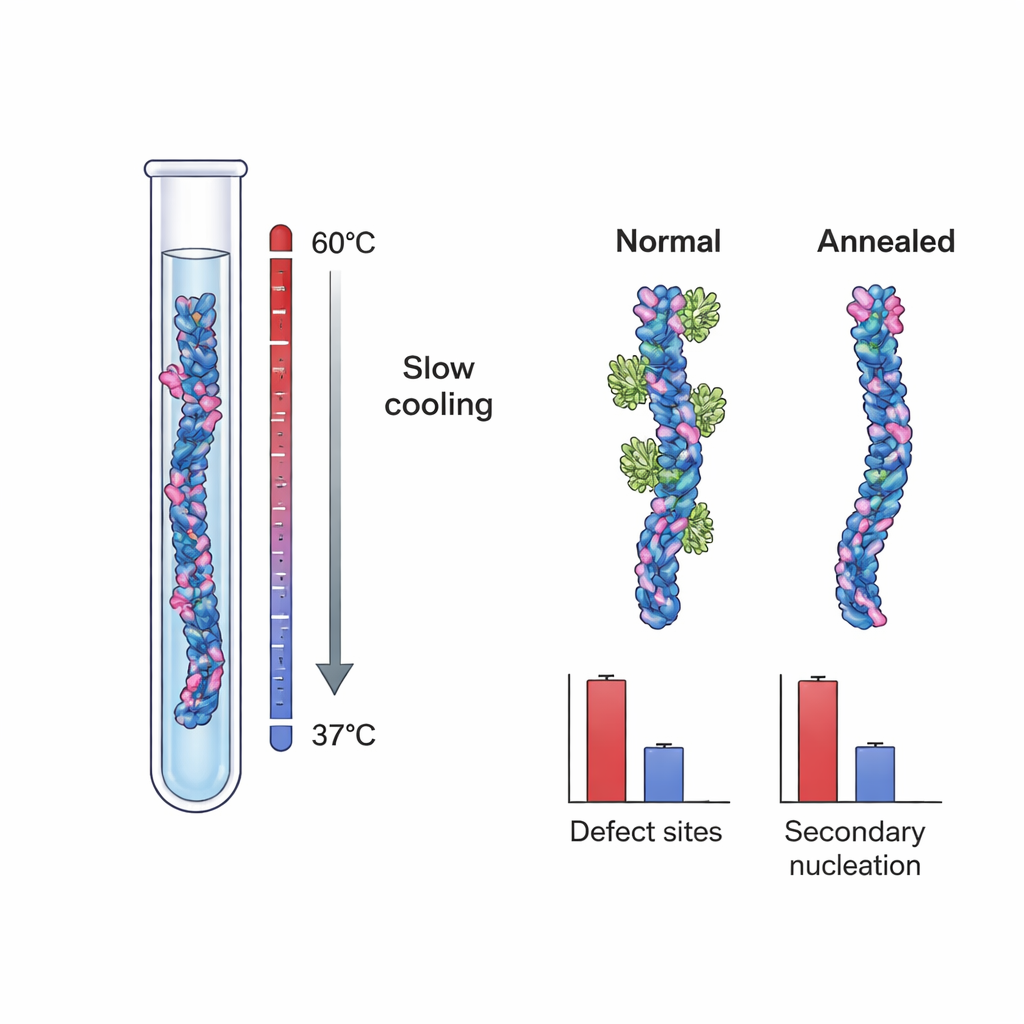
Minder fouten, minder gevaarlijke groeipunten
Toen het team Brichos-binding aan deze twee fibriltypes mat, ontdekten ze een opvallend verschil. Controle Aβ40-fibrillen hadden ongeveer één Brichos-bindingsplaats per ~100 monomeren, wat opnieuw wijst op zeldzame maar belangrijke plekken. Geannealde fibrillen hadden echter slechts ongeveer één plaats per ~800 monomeren — een bijna 90% reductie in de frequentie van plekken. In afzonderlijke tests waarbij deze fibrillen als "zaden" aan verse Aβ40-oplossingen werden toegevoegd, waren geannealde fibrillen veel minder effectief in het triggeren van nieuwe aggregatie, zelfs wanneer hun totale massa werd afgestemd op die van controlefibrillen. Gedetailleerde kinetische modellering liet zien dat deze daling in zaaiend vermogen niet eenvoudigweg verklaard kon worden door verschillen in fibrillengte. In plaats daarvan kwam het kwantitatief overeen met het gereduceerde aantal Brichos-bindingsplaatsen, wat sterk ondersteunt dat groeideffecten fungeren als de belangrijkste motoren van secundaire nucleatie.
Een algemeen principe met therapeutische belofte
Door thermodynamische argumenten te combineren met heranalyse van eerder werk en vergelijking tussen meerdere amyloïde-vormende eiwitten, betogen de auteurs dat zeldzame groeidefecten waarschijnlijk centraal staan bij secundaire nucleatie in veel systemen, niet alleen bij Aβ gerelateerd aan Alzheimer. Deze defecten maken de dichtgepakt opgebouwde binnenkern van de fibril gedeeltelijk bloot, en bieden een kant-en-klare mal waar nieuwe oligomeren en fibrillen veel gemakkelijker kunnen ontstaan dan op een glad oppervlak. Het herkennen van deze defecten als de sleutelschuldigen opent nieuwe wegen voor geneesmiddelontwerp. In plaats van te proberen elke mogelijke interactie op een fibriloppervlak te blokkeren, zouden therapieën zich kunnen richten op het afschermen of repareren van slechts deze schaarse defectplekken, of op het verminderen van de omstandigheden die hun ontstaan bevorderen. In praktische termen kan dat betekenen dat de effectieve concentratie van amyloïde-vormende eiwitten in de hersenen wordt verlaagd, of dat er moleculen worden ontworpen, geïnspireerd door Brichos, die defectgedreven nucleatiehubs herkennen en neutraliseren. Als dit succesvol is, zouden dergelijke strategieën de belangrijkste bron van toxische oligomeren kunnen afsnijden en het verloop van amyloïde-gekoppelde ziekten kunnen vertragen.
Bronvermelding: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Trefwoorden: amyloïde fibrillen, Ziekte van Alzheimer, secundaire nucleatie, eiwitaggregatie, Brichos-chaperon