Clear Sky Science · nl
Ultrasnelle oplosmiddelgemoduleerde roaming‑mechanisme in bromoform onthuld door femtoseconde röntgenoplossingsverstrooiing
Waarom kleine moleculen in water en lucht ertoe doen
Bromoform is een klein, natuurlijk geproduceerd molecuul met grote milieu‑effecten. Wanneer zonlicht dit molecuul in de atmosfeer of in zeewatervlucht vrijstelt, kan het broomatomen loslaten die bijdragen aan de afbraak van ozon, het schild dat ons beschermt tegen schadelijke ultraviolette straling. Deze studie stelt een ogenschijnlijk eenvoudige vraag met verstrekkende gevolgen: verandert de vloeibare omgeving van bromoform wat er gebeurt in de eerste billi‑ (triljoenste) seconden na belichting, en beïnvloedt dat uiteindelijk hoeveel ozon‑vreterig broom er verschijnt?
Licht dat een molecuul uiteentrekt
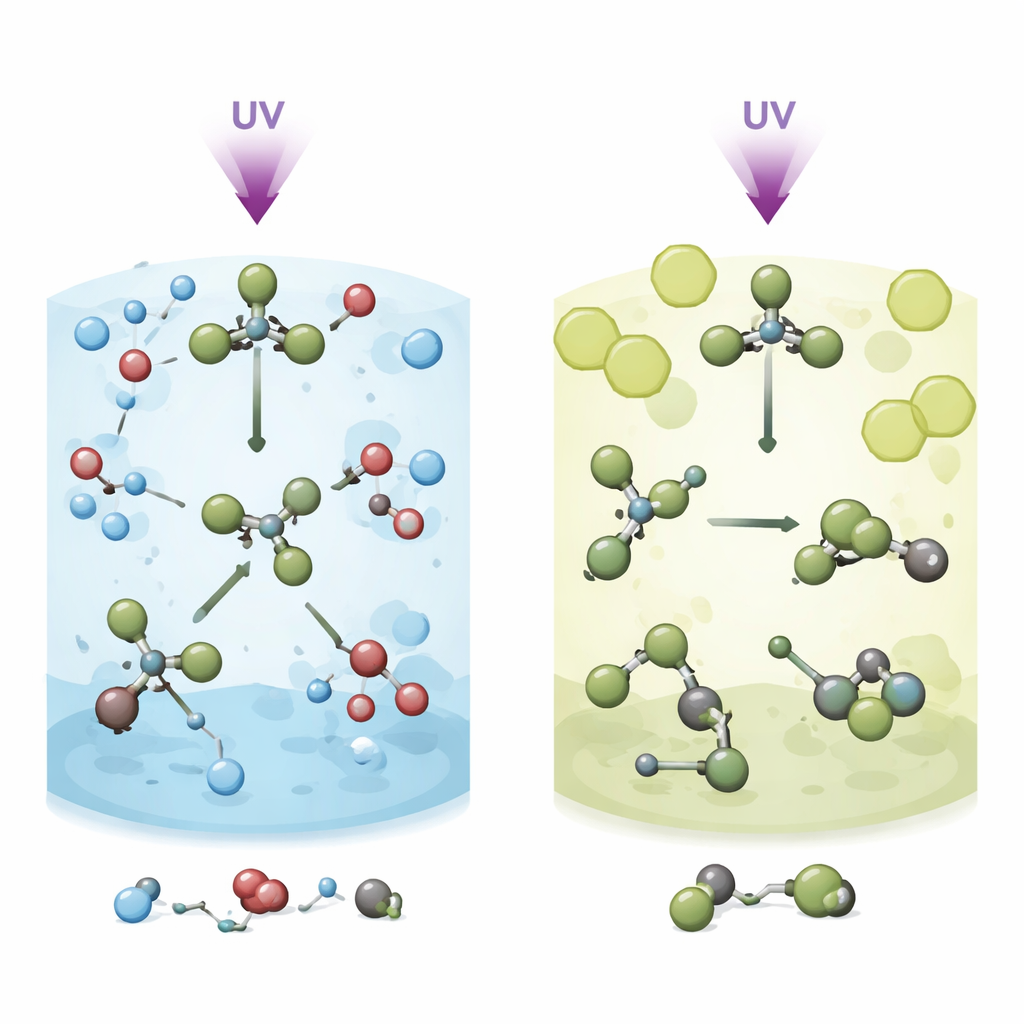
De onderzoekers beginnen door extreem korte pulsen ultraviolet licht op bromoform opgelost in twee verschillende vloeistoffen te schijnen: methanol, dat polair en chemisch reactief is, en methylcyclohexaan, dat niet‑polair en relatief inert is. Het licht verzwakt snel één van de koolstof–broombindingen van bromoform, waardoor het molecuul begint uiteen te vallen. In plaats van simpelweg weg te vliegen, blijft één broomatoom echter hangen en ‘roamt’ rond het overgebleven deel van het molecuul, CHBr₂. Deze roaming‑beweging creëert een vluchtige, herschikte vorm die een isomeer wordt genoemd. De centrale vraag is wat er met dit roaming‑intermediair gebeurt in verschillende vloeistoffen, en hoe die keuze bepaalt of bromoform vrije broomatomen afgeeft of wordt omgeleid naar andere producten.
Moleculaire films maken met röntgenstralen
Om deze gebeurtenissen in beeld te brengen, gebruikt het team femtoseconde tijds‑geresolveerde röntgenoplossingsverstrooiing bij de European X‑ray Free‑electron Laser. In essentie leggen ze een stroboscoopfilm vast van hoe inter‑atomaire afstanden in real time veranderen, met zowel pico‑ als sub‑picoseconde resolutie. Door de gemeten verstrooiingspatronen te vergelijken met computergegenereerde patronen voor veel mogelijke structuren, reconstrueren ze hoe bindingslengtes en hoeken binnen bromoform zich ontwikkelen na excitatie. Geavanceerde analysemethoden en door machine learning versnelde simulaties helpen hen overlappende reactiepaden te scheiden en precieze levensduren toe te wijzen aan kortlevende soorten.
Twee vloeistoffen, twee zeer verschillende lotsbestemmingen
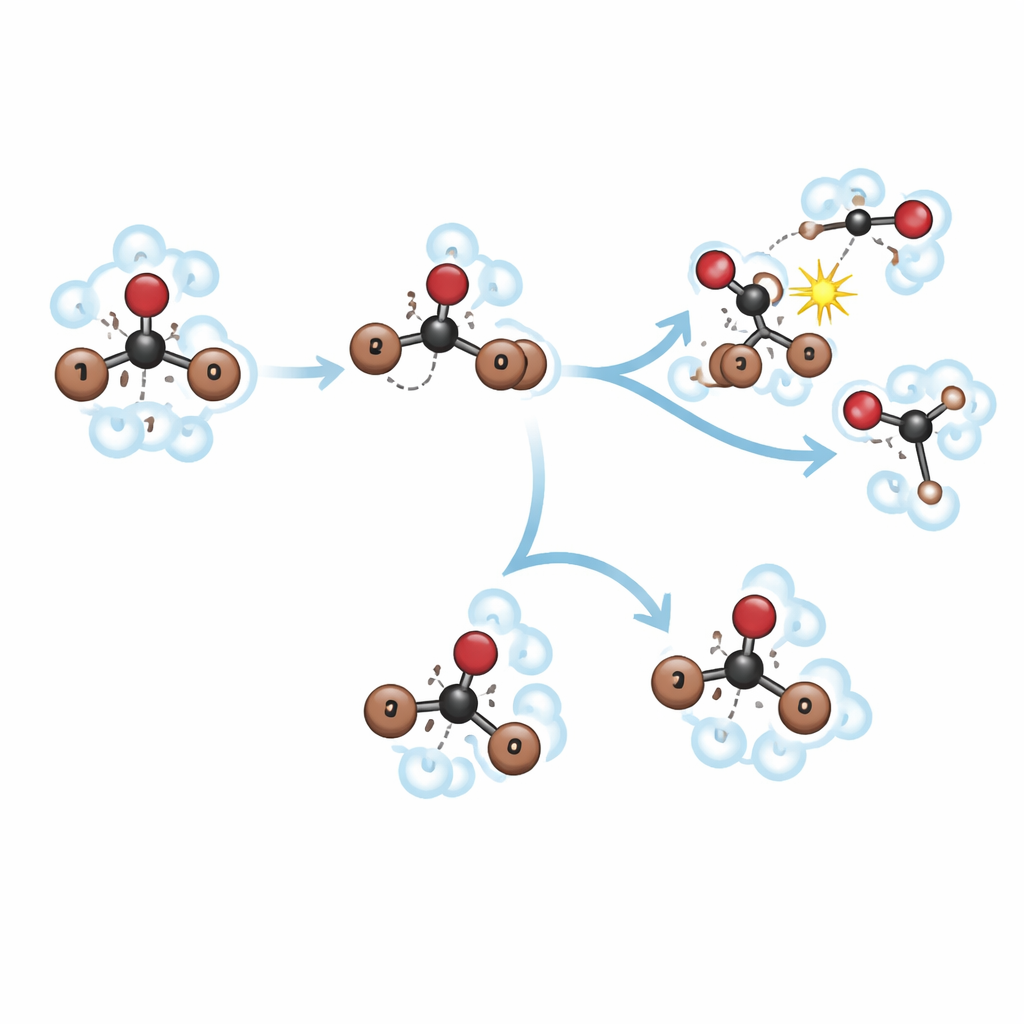
In methanol is het roaming‑intermediair aanwezig maar kortlevend. Binnen ruwweg 150 femtoseconden breekt de initiële koolstof–broombinding, waardoor CHBr₂ en een roaming broom ontstaan. In de volgende ~400 femtoseconden rekt en buigt dit hete, trillende isomeer herhaaldelijk, waardoor de fragmenten vaak in contact komen met nabijgelegen methanolmoleculen. In plaats van te ontspannen tot een stabiele herschikte vorm, wordt de roamingstructuur snel onderschept door methanol in een “methanolyse”‑reactie. Dit produceert nieuwe moleculen, CH₃OCHBr₂ en HBr, terwijl vrije CHBr₂‑ en Br‑fragmenten uit een parallel, meer direct scheuringspad langzamer blijven reageren over enkele picoseconden. De nauwe moleculaire “kooi” van het oplosmiddel en de reactieve hydroxylgroepen werken samen om bromoform deze chemische reactieroute in te sturen in plaats van naar een langlevend isomeer.
Wanneer de vloeistof een stap terugdoet en roaming doorgang laat vinden
In methylcyclohexaan verandert het verhaal dramatisch. Dezelfde ultravioletpuls veroorzaakt opnieuw roaming binnen ongeveer 150 femtoseconden, maar de niet‑polaire vloeistof omsluit bromoform losser en reageert er niet snel mee. Hier hebben het roaming broom en het CHBr₂‑deel ruimte om zich te heroriënteren en zich in een stabiele isomere structuur te zetten in plaats van onmiddellijk met oplosmiddelmoleculen te reageren. Directe splitting in afzonderlijke CHBr₂‑ en Br‑fragmenten blijft optreden en concurreert met isoomervorming, maar nu overleeft de herschikte isomeer veel langer. Simulaties tonen aan dat de grotere, zachtere solvatiekkooi in methylcyclohexaan dit gasachtige roaming‑gedrag aanmoedigt, terwijl de krappe, sterk interacterende kooi in methanol hetzelfde intermediair rechtstreeks in chemische reactie kanaliseert.
Wat dit betekent voor ozon en daarbuiten
Gezamenlijk laten deze experimenten en berekeningen zien dat roaming een universele vroege stap is wanneer bromoform ultraviolet licht absorbeert in vloeibare omgevingen, maar dat het omringende oplosmiddel bepaalt wat er daarna gebeurt. In methanol‑achtige omgevingen dient roaming voornamelijk om zeer snelle reacties met de vloeistof aan te sturen, waardoor de vorming van langlevende isomeren wordt beperkt en de wijze en timing van het verschijnen van broomhoudende producten worden bepaald. In methylcyclohexaan‑achtige omgevingen voedt roaming daarentegen een langlevende herschikte vorm die later broom op andere tijdschalen kan vrijgeven. Door deze ultrasnelle bewegingen rechtstreeks te filmen, toont het werk aan dat het microscopische karakter van druppels, aerosolen en andere gecondenseerde‑faseomgevingen sterk de chemische paden van ozon‑relevante moleculen kan beheersen, wat wetenschappers helpt om nauwkeurigere modellen van atmosferische en oplossingsfase‑fotochemie te bouwen.
Bronvermelding: Su, P., Zhang, J., Wang, H. et al. Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering. Nat Commun 17, 2514 (2026). https://doi.org/10.1038/s41467-026-69374-4
Trefwoorden: bromoform, roaming‑mechanisme, ultrasnelle fotochemie, oplosmiddeleffecten, ozonafbraak