Clear Sky Science · nl
Concurrerende waterstofbindingsordes sturen de anomalie van waters oppervlaktespanning
Waarom het oppervlak van water vreemder is dan het lijkt
Het oppervlak van water laat insecten over vijvers lopen, bepaalt de vorm van regendruppels en regelt hoe bellen ontstaan en uiteenspatten. Toch vinden wetenschappers, wanneer ze meten hoe “strak” dat oppervlak is — de oppervlaktespanning — dat water zich verrassend eigenaardig gedraagt naarmate het kouder wordt, vooral wanneer het onder zijn normale vriespunt wordt afgekoeld. Dit artikel gebruikt geavanceerde computersimulaties om te laten zien hoe de verborgen ordening van watermoleculen aan het oppervlak dit al lang bestaande mysterie verklaart.
Twee verborgen typen vloeibaar water
Hoewel we water ervaren als een eenvoudige, uniforme vloeistof, kunnen zijn moleculen zich lokaal op twee contrasterende manieren organiseren. De ene ordening is dichter en meer ongeordend; de auteurs noemen dit de ρ-toestand. De andere is opener en symmetrischer, waarbij elk molecuul ruwweg omgeven is in een vierpunts-, tetraëdrisch patroon; dit wordt de S-toestand genoemd. Eerder werk suggereerde dat het evenwicht tussen deze twee lokale patronen helpt veel van waters vreemde bulk-eigenschappen te verklaren. Hier onderzoeken de auteurs hoe ditzelfde tweestatenbeeld zich afspeelt aan de lucht–water-grens, waar de oppervlaktespanning ontstaat.
Hoe het oppervlak moleculen op één lijn trekt
Op de grens tussen lucht en water voelen moleculen niet langer gelijke aantrekking in alle richtingen. Deze gebroken symmetrie bevoordeelt ρ-toestandmoleculen waarvan de waterstofatomen en moleculaire dipolen gemakkelijk in een voorkeursrichting kunnen leunen. Simulaties tonen dat nabij kamertemperatuur en iets daaronder de bovenste laag van water vol raakt met deze gealigneerde ρ-toestandmoleculen, terwijl S-toestandmoleculen iets dieper onder het oppervlak en in de bulk vaker voorkomen. Omdat ρ-toestandmoleculen sterk op één lijn komen te liggen, creëren ze een onbalans van krachten — stressanisotropie — die een relatief grote oppervlaktespanning genereert vergeleken met gewone vloeistoffen zoals benzeen.
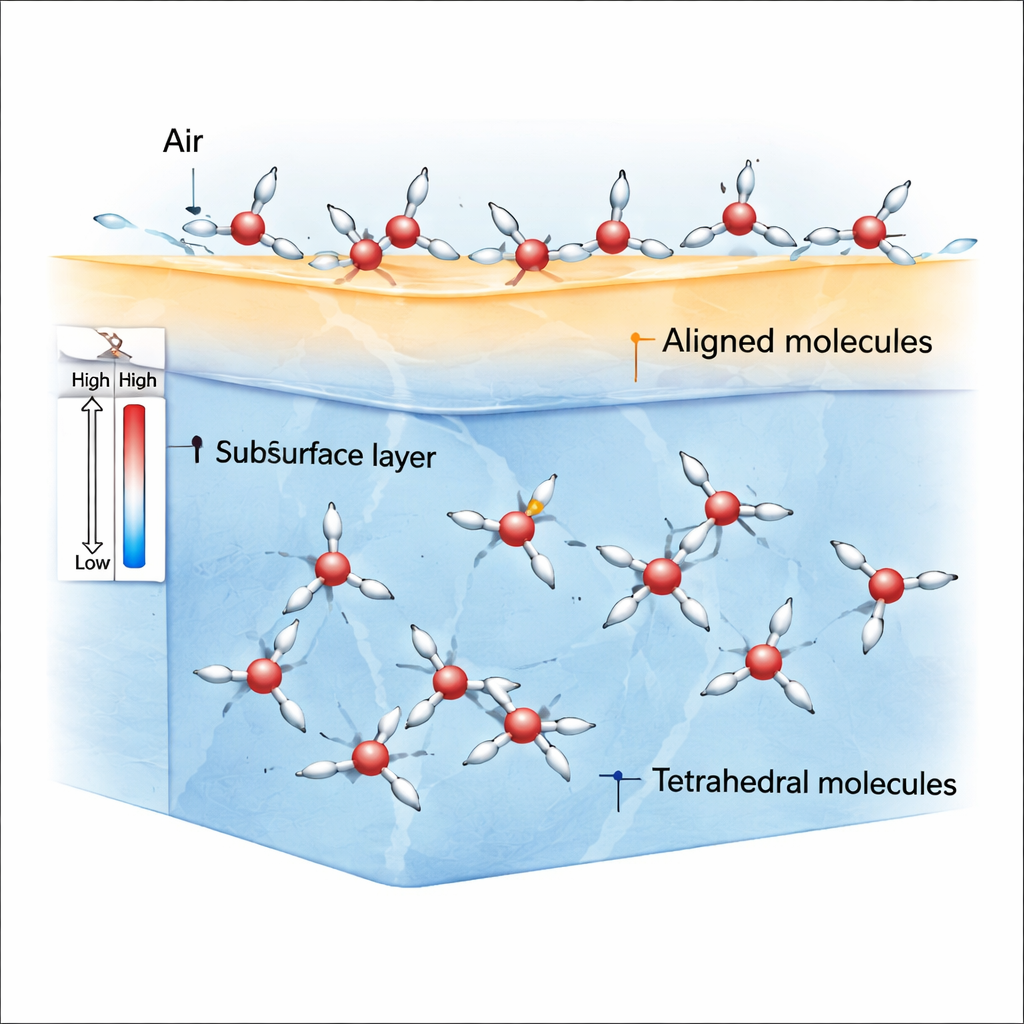
Waarom afkoeling eerst het aanspannen vertraagt en daarna versnelt
Bij de meeste eenvoudige vloeistoffen maakt afkoeling het oppervlak geleidelijk strakker, waardoor de oppervlaktespanning bijna lineair toeneemt. Water doet dit alleen bij hogere temperaturen. Als het afkoelt richting ongeveer –0,15 °C (275 K) begint de stijging van de oppervlaktespanning te vertragen. De simulaties laten zien dat deze vertraging optreedt omdat de ρ-toestandmoleculen aan het oppervlak al zo gealigneerd zijn als ze kunnen worden; verdere afkoeling verandert hun bijdrage nauwelijks. Tegelijkertijd blijven S-toestandmoleculen in de subsurface grotendeels willekeurig georiënteerd, zodat zij weinig doen om de oppervlaktedruk te verhogen. Het nettoresultaat is een soort plateau: de temperatuur blijft dalen, maar de oppervlaktespanning groeit slechts traag.
Diepe superkoeling triggert een tweede aanspanning
Wanneer water veel verder wordt gekoeld, ver onder zijn normale vriespunt in het diep supergekoelde regime (rond 250 K en lager), verandert het gedrag opnieuw. Het aandeel S-toestand, tetraëdrische structuren neemt scherp toe, zelfs nabij het oppervlak. Cruciaal is dat deze S-toestandmoleculen niet langer in willekeurige richtingen wijzen. Hun dipolen beginnen zich te oriënteren langs de richting loodrecht op het oppervlak, aangedreven door interacties tussen naburige moleculaire dipolen en door een gebied met negatieve druk net onder het oppervlak. Zodra dat gebeurt, begint S-toestandwater, dat eerder het oppervlak verzachtte, het oppervlak juist te versterken. Deze extra, geordende bijdrage veroorzaakt een hernieuwde, snellere toename — de “reëntrante” stijging — van de oppervlaktespanning bij lage temperaturen.
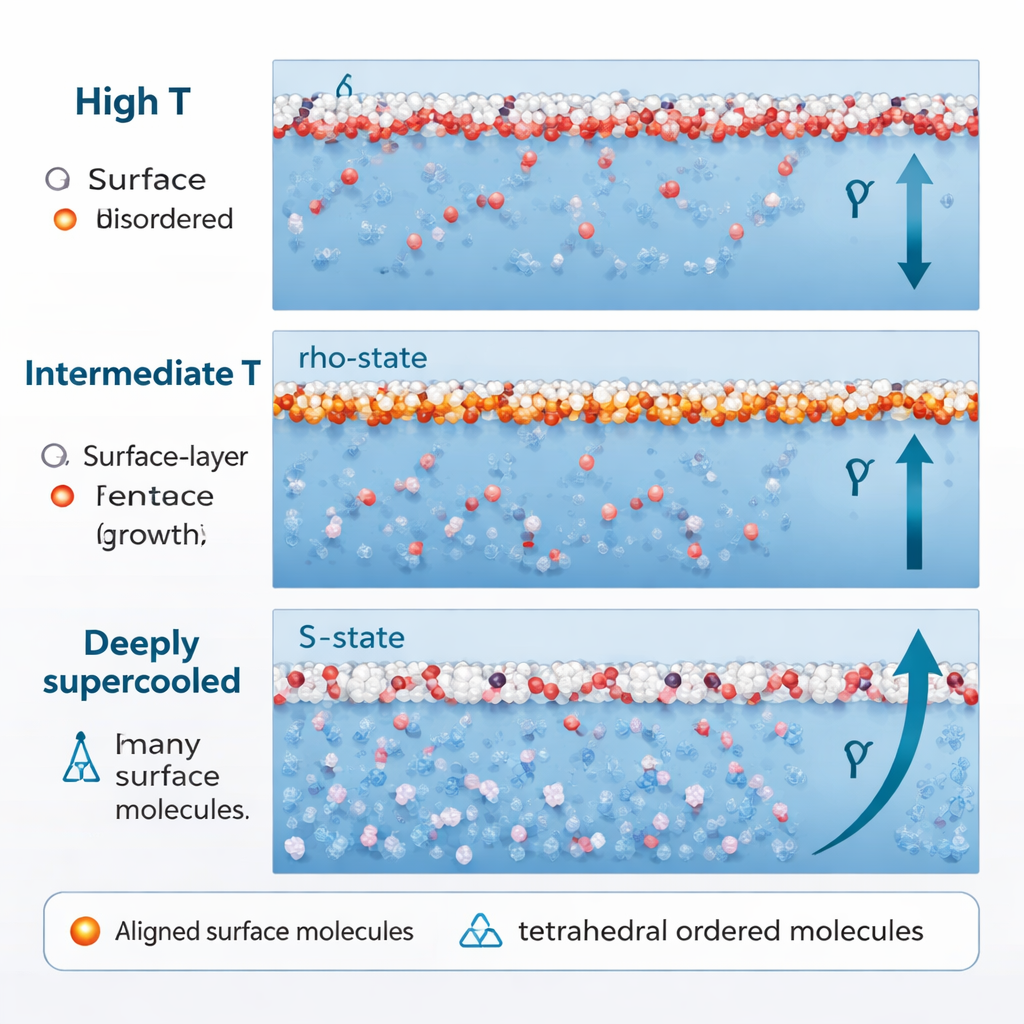
Van oppervlakkige raadsels naar ijs en verder
Dezelfde tetraëdrische S-toestandclusters die het oppervlak bij lage temperaturen verzwaren, lijken ook op vroege bouwstenen van bepaalde ijsvormen, en de simulaties vinden ze verrijkt nabij de interface. Dat betekent dat de lucht–water-grens als een wieg voor ijsvorming kan fungeren, wat helpt verklaren waarom bevriezing vaak bij oppervlakken begint. Breder gezien levert het werk een concrete, molecuulniveauverbinding tussen hoe watermoleculen zich ordenen en oriënteren en hoe sterk het oppervlak naar binnen trekt. Dit structureel-mechanische beeld lost niet alleen de vreemde temperatuurcurve van waters oppervlaktespanning op, maar biedt ook een routekaart om interfaciale verschijnselen in andere netwerkvormende vloeistoffen te begrijpen en te beheersen, van supergekoeld water in wolken tot materialen die in technologie en biologie worden gebruikt.
Bronvermelding: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Trefwoorden: oppervlaktespanning van water, waterstofbinding, supergekoeld water, vloeistructuur, ijsnucleatie