Clear Sky Science · nl
STING werkt samen met TOX om HO-1-expressie te onderdrukken en ferroptose in tumor-infiltrerende CD8+ T-cellen en resistentie tegen immunotherapie te veroorzaken
Waarom dit onderzoek van belang is voor kankerbehandeling
Moderne kankerimmunotherapieën werken door de eigen dodelijke T-cellen van het lichaam te bevrijden, maar veel tumoren vinden nog steeds manieren om deze cellen uit te schakelen. Deze studie onthult een verborgen zelfvernietigingsschakelaar in CD8+ “killer”-T-cellen die tumoren uitbuiten, en toont aan dat het uitschakelen van die schakelaar immunotherapie veel effectiever kan maken.
Een verborgen doodspad binnen tumorbestrijdende T-cellen
Binnen een tumor zouden CD8+ T-cellen kankercellen moeten opsporen en vernietigen. In plaats daarvan raken ze vaak zeldzaam, traag en kortlevend. De auteurs richtten zich op twee moleculen in T-cellen—STING, een sensor van DNA-schade, en TOX, een eiwit dat wordt geassocieerd met T-celuitputting. Ze maakten muismodellen waarbij CD8+ T-cellen STING, TOX, of beide misten, en implanteren vervolgens verschillende tumortypes. Verrassend genoeg ruimden muizen waarvan de T-cellen ofwel STING ofwel TOX misten tumoren veel beter op. Hun tumoren groeiden langzamer, bevatten veel meer CD8+ T-cellen, en deze T-cellen produceerden grotere hoeveelheden kanker-dodende moleculen zoals interferon-gamma en granzym B. Dit wijst op een intern programma dat T-cellen binnen tumoren heimelijk saboteert.
Hoe ijzergestuurde celdood de immuniteit verzwakt
Door genexpressie in tumor-infiltrerende T-cellen te onderzoeken, vonden de onderzoekers dat normale T-cellen binnen tumoren voorbereid waren op een specifieke vorm van celdood die ferroptose wordt genoemd. In tegenstelling tot apoptose wordt ferroptose veroorzaakt door ijzerstapeling en de ophoping van beschadigde lipiden in celmembranen. In gewone CD8+ T-cellen die aan tumorcellen werden blootgesteld, waren genen die ijzeraccumulatie en lipidenbeschadiging bevorderen geactiveerd, terwijl beschermende genen werden onderdrukt. Daarentegen vertoonden STING- of TOX-deficiënte T-cellen het omgekeerde patroon: ze drukten meer van de beschermende enzymen HO-1 en GPX4 uit, hadden lagere ijzerniveaus, minder lipidperoxidatie, gezondere mitochondriën en weerstonden ferroptotische celdood. Laboratoriumtesten bevestigden dat het chemisch blokkeren van ferroptose normale T-cellen in leven hield, terwijl het verwijderen van STING of TOX ze van nature resistent maakte.
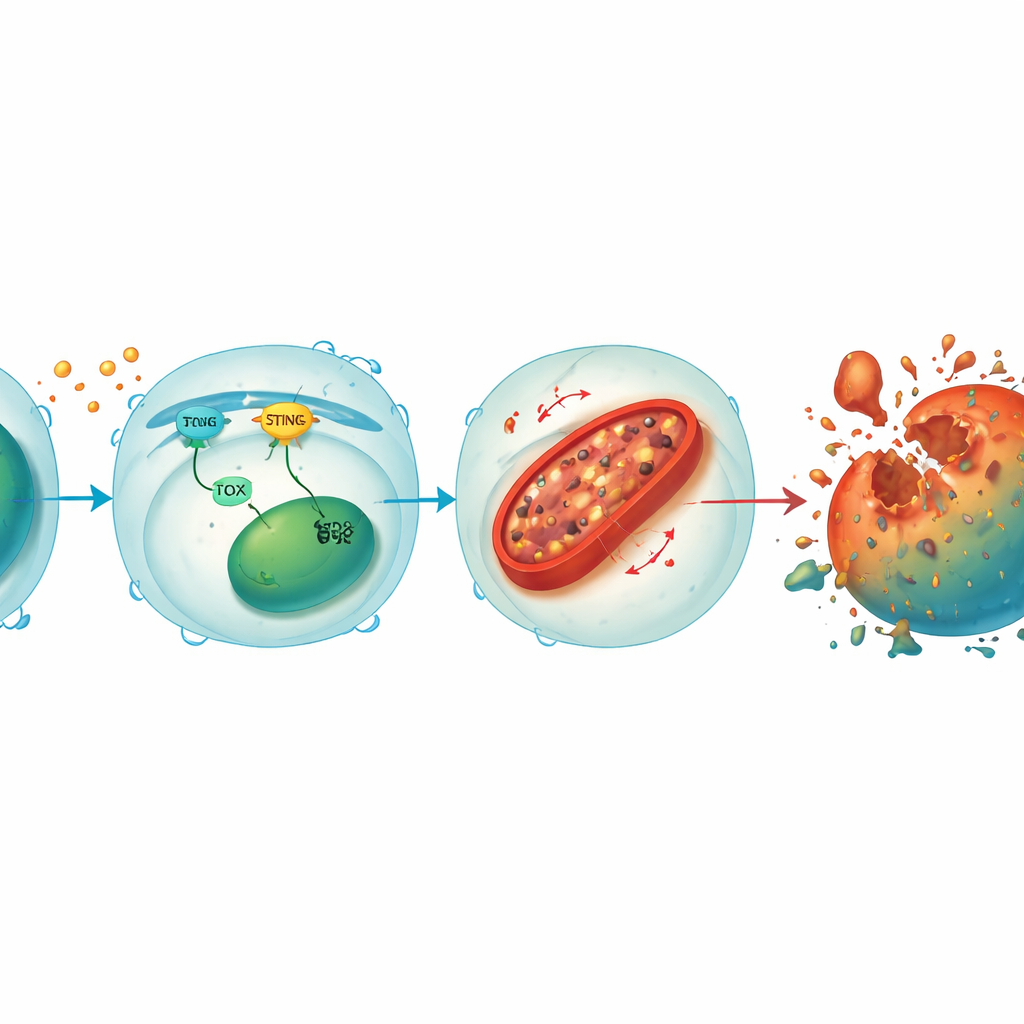
Een lus die stresssignalen koppelt aan mitochondriale schade
Dieper gravend ontdekten de onderzoekers dat STING en TOX een versterkende lus vormen binnen CD8+ T-cellen. Wanneer tumor- of virale signalen STING activeren, zet dat downstream factoren in gang die TOX verhogen, en TOX helpt op zijn beurt STING-activiteit te handhaven. Gezamenlijk onderdrukken ze HO-1, een enzym dat normaal helpt het cellulaire ijzer onder controle te houden. Met HO-1 onderdrukt, hoopt ijzer zich op in mitochondriën—de energiefabrieken van de cel—wat leidt tot hoge niveaus reactieve zuurstofsoorten en oxidatie van membraanlipiden. Deze mitochondriale schade put de energieproductie uit en duwt de T-cel uiteindelijk in ferroptose. Het herstellen van STING of TOX in knockout-T-cellen bracht ijzerstapeling en celdood terug, terwijl het verder verlagen van HO-1 zelfs de beschermde T-cellen weer kwetsbaar maakte, waarmee HO-1 als een centrale rem op dit destructieve pad wordt benadrukt.
Hoe door de tumor gemaakte lactaat de trekker overhaalt
De tumormicro-omgeving is rijk aan lactaat, een bijproduct van het veranderde metabolisme van kanker. De studie toont aan dat dit lactaat niet slechts metabool afval is—het helpt actief de ferroptose-schakelaar in T-cellen om te zetten. Vergeleken met andere cellen waren CD8+ T-cellen bijzonder gevoelig voor lactaat. Wanneer lactaat via specifieke transporters de cellen binnenkomt, veroorzaakt het ijzerstapeling, mitochondriale krimp, DNA-verlies in mitochondriën en meer oxidatieve schade. Tegelijkertijd verhoogde lactaat STING- en TOX-activiteit en onderdrukte het HO-1 verder. T-cellen zonder STING of TOX waren veel beter bestand tegen lactaat-geïnduceerd letsel. Het blokkeren van een belangrijke lactaattransporter met een geneesmiddel (AZD3965) beschermde CD8+ T-cellen tegen ferroptose in muizen, verhoogde hun aanwezigheid in tumoren en vertraagde tumorgroei, wat het voordeel nabootste van het genetisch verwijderen van STING in T-cellen.
Een kwetsbaarheid in een therapeutisch voordeel veranderen
Deze mechanistische inzichten hebben praktische implicaties. Wanneer de onderzoekers adoptieve celtherapie gebruikten—het infunderen van muizen met in het laboratorium geactiveerde T-cellen—vonden ze dat T-cellen die zo werden geconstrueerd dat ze STING of TOX misten veel sterkere tumorcontrole gaven dan normale T-cellen. Bovendien leidde het combineren van deze “ferroptose-resistente” T-cellen met bestaande behandelingen zoals PD-1- of TIM-3-remmers, cisplatine-chemotherapie of een STING-activerend middel tot aanzienlijk betere tumorkrimp dan eender welke monotherapie. Ten slotte waren in tumormonsters van patiënten met baarmoederhalskanker hogere TOX- en lagere HO-1-niveaus in tumor-infiltrerende lymfocyten gekoppeld aan slechtere overleving, wat suggereert dat deze route ook klinische uitkomsten bij mensen beïnvloedt.
Wat dit betekent voor toekomstige kankerzorg
In eenvoudige bewoordingen onthult de studie dat tumoren onze beste kankerbestrijdende T-cellen van binnenuit kunnen laten ‘roesten’ door een ijzergestuurde vorm van celdood te stimuleren. Een lactaat–STING–TOX-circuit vermindert de bescherming door HO-1, beschadigt mitochondriën en leidt tot ferroptose, waardoor het aantal effectieve CD8+ T-cellen afneemt. Het verstoren van dit circuit—door T-cellen te ontwerpen zonder STING of TOX, door HO-1 te versterken of door lactaatinname te blokkeren—houdt T-cellen in leven, energiek en klaar om aan te vallen. Dit werk wijst op volgende generatie immunotherapieën die metabole en genetische aanpassing van T-cellen combineren met bestaande geneesmiddelen om resistentie te overwinnen en duurzamere kankercontrole te bieden.
Bronvermelding: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Trefwoorden: kankerimmunotherapie, CD8 T-cellen, ferroptose, tumormicro-omgeving, STING TOX HO-1-route