Clear Sky Science · nl
Door microbiota afgeleid IPA beschermt tegen colitis door de intestinale HMGCS2-gemedieerde ketogenese te reguleren om mucosale genezing te bevorderen
Waarom darmbacteriën ertoe doen bij een beschadigde darm
Wanneer de bekleding van de darm beschadigd is, zoals bij inflammatoire darmziekten (IBD) of na intensieve medische behandelingen, moet het lichaam snel dit innerlijke “huidlaagje” herstellen om te voorkomen dat schadelijke inhoud in de bloedbaan terechtkomt. Deze studie onthult hoe één molecuul, gemaakt door behulpzame darmbacteriën, de darm kan helpen zichzelf te genezen en wijst op nieuwe manieren om chronische darmstoornissen te behandelen zonder het immuunsysteem breed te onderdrukken.
Een behulpzaam signaal van vriendelijke microben
De onderzoekers begonnen met het vergelijken van chemische vingerafdrukken uit stoelgangmonsters van mensen met IBD en gezonde vrijwilligers, evenals in verschillende muismodellen van colitis. Uit honderden moleculen stak er één bovenuit: indool-3-propionzuur (IPA), een afbraakproduct van het dieetaminozuur tryptofaan dat door bepaalde darmbacteriën wordt gemaakt. IPA-niveaus waren consequent lager bij mensen met de ziekte van Crohn en bij muizen met colitis dan bij gezonde tegenhangers. Dit suggereerde dat verlies van IPA mogelijk bijdraagt aan wat er misgaat wanneer de darmslijmvlies ontstoken raakt en niet goed herstelt.
De beschermende wand van de darm versterken
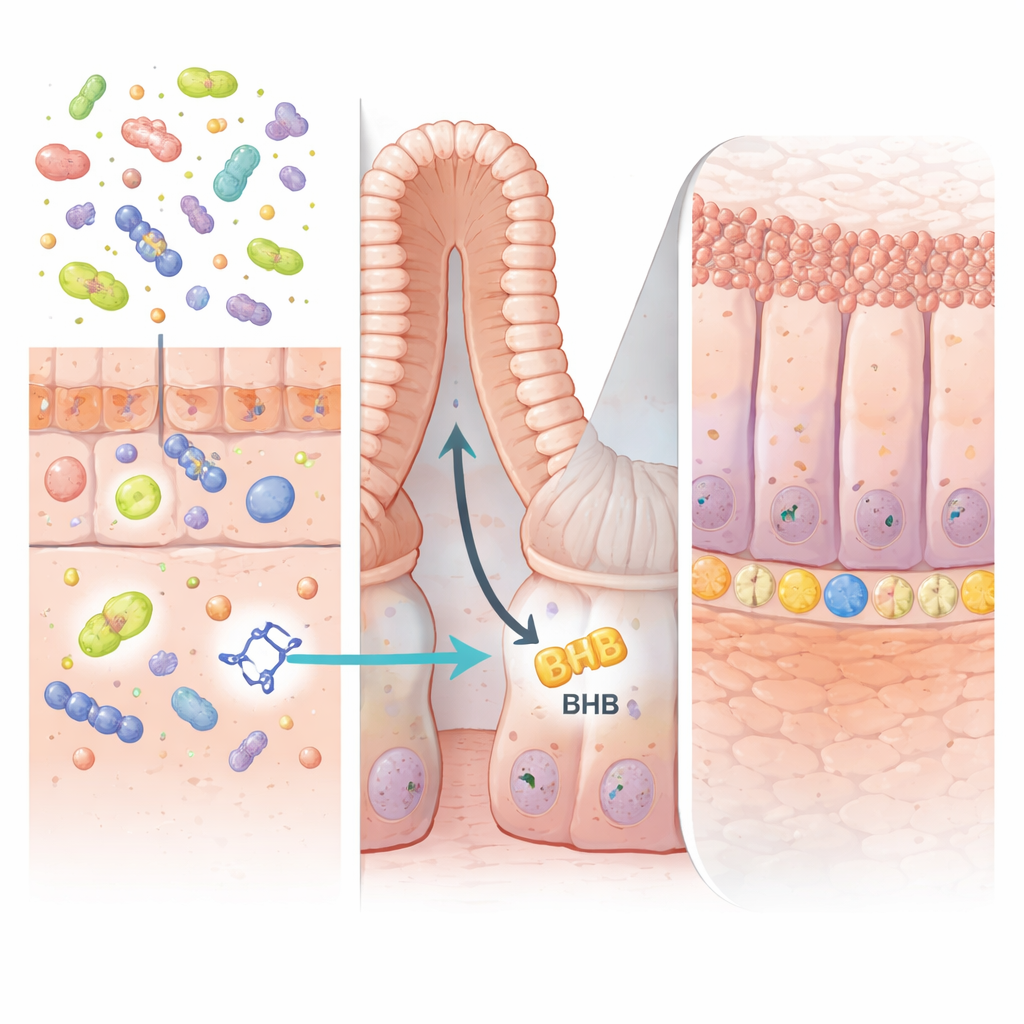
Om te testen of IPA slechts een ziektebijverschijnsel was of daadwerkelijk beschermde, gaven de onderzoekers IPA aan muizen voordat ze verschillende vormen van darmletsel opwekten, waaronder chemische colitis en stralingsschade. Muizen die voldoende doses IPA kregen, hadden langere, gezondere dikke darmen, minder ontstekingsveranderingen onder de microscoop en een dikkere slijmlaag met strakkere celverbindingen. Ze verloren minder ontstekingsmarkers en hadden meer gobletcellen, die de beschermende slijmlaag produceren. Belangrijk is dat deze voordelen ook werden gezien bij kiemvrije muizen zonder resident microbioom, wat toont dat IPA, eenmaal aanwezig, direct op het darmslijmvlies kan werken zonder andere microben.
Stamcellen van brandstof voorzien met een speciaal soort energie
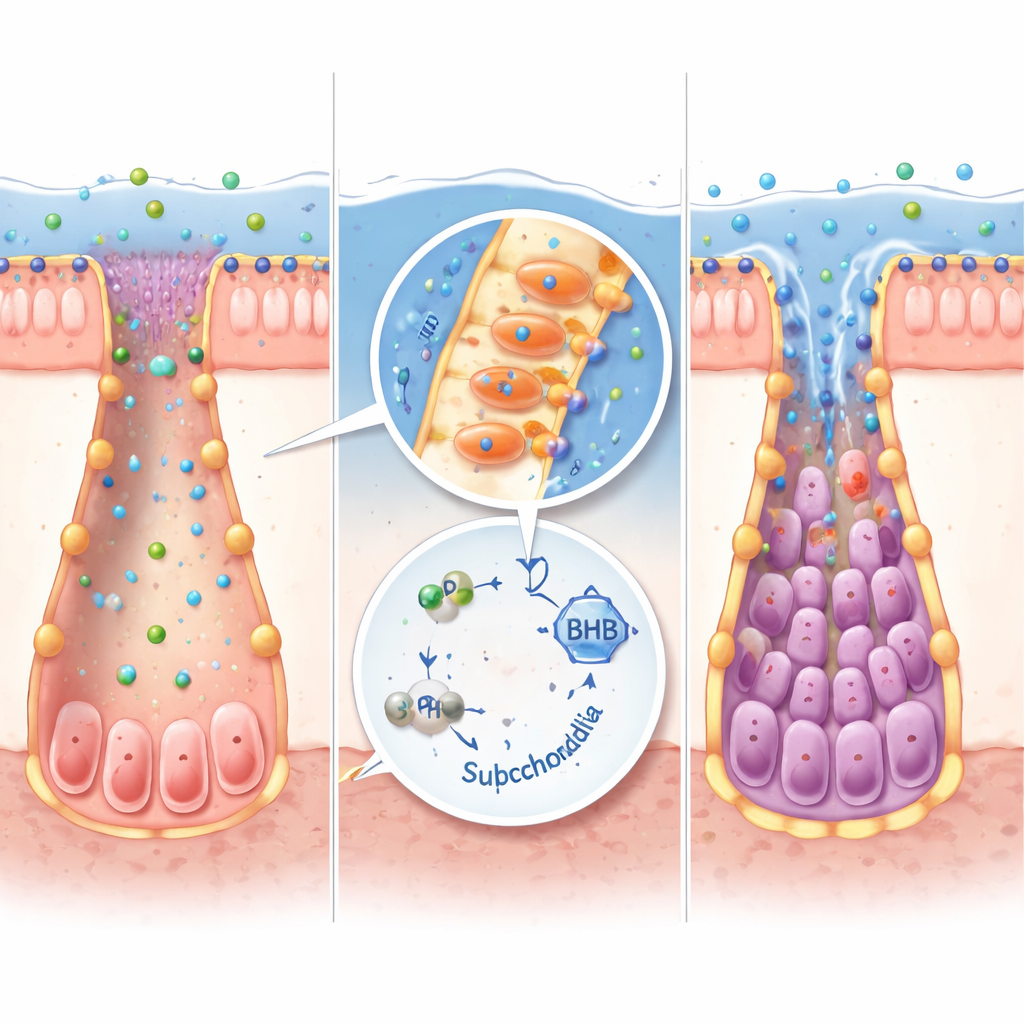
De sleutel van IPA’s werking lag diep in de intestinale “crypten”, de kleine zakjes waar stamcellen zitten en continu het slijmvlies vernieuwen. De auteurs toonden aan dat IPA een eiwit genaamd PPARα in intestinale epitheelcellen activeert. Dit verhoogt op zijn beurt de productie van een enzym genaamd HMGCS2, dat ketogenese aandrijft—het proces waarbij de energierijke molecule β-hydroxybutyraat (BHB) wordt gemaakt. Verhoogde BHB binnen de darmwand stimuleerde LGR5-positieve stamcellen om uit te zetten en beschadigd weefsel sneller te regenereren. Wanneer het HMGCS2-enzym of PPARα selectief uit intestinale cellen van muizen werd verwijderd, kon IPA de stamcelactiviteit of bescherming tegen colitis niet meer verbeteren, wat bevestigt dat deze ketonproducerende route essentieel is.
Van bacteriële fabrieken naar menselijk weefsel
Niet alle darmbacteriën kunnen IPA maken. Door grote microbiome-datasets opnieuw te analyseren, identificeerden de onderzoekers Peptostreptococcus russellii als een belangrijke IPA-producent die in meerdere IBD-cohorten is afgenomen. In laboratoriumkweek zette deze bacterie tryptofaan efficiënt om in IPA. Toen kiemvrije muizen werden gekoloniseerd met P. russellii, stegen hun IPA-niveaus, werden ketonproducerende genen aangezet, namen stamcelmarkers toe en nam de ernst van colitis af in vergelijking met muizen die een generieke microbiele transplantatie kregen. Dezelfde IPA–ketonroute werkte in mini-darmorganoïden gekweekt uit muis- en menselijk weefsel, waar toevoeging van IPA of BHB stamcellen hielp herstellen na ontstekingsschade terwijl pro-inflammatoire signalen werden teruggedraaid.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat beschrijft het werk een eenvoudige maar krachtige keten van gebeurtenissen: bepaalde darmbacteriën zetten voedings-tryptofaan om in IPA; IPA activeert een metabole schakelaar in intestinale cellen; deze schakelaar verhoogt de productie van BHB; en BHB, op zijn beurt, wekt stamcellen die het darmslijmvlies herbouwen. Voor mensen met IBD of andere aandoeningen die de intestinale barrière beschadigen, kunnen behandelingen die IPA herstellen of veilig de effecten ervan nabootsen—via voeding, gerichte probiotica of speciaal ontworpen medicijnen—echte mucosale genezing bevorderen zonder brede immuunsuppressie. Hoewel er meer studies bij patiënten nodig zijn, biedt deze microbe–metaboliet–stamcel-as een veelbelovende nieuwe invalshoek om de darm van binnenuit te repareren.
Bronvermelding: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Trefwoorden: darmmicrobioom, intestinale stamcellen, inflammatoire darmziekte, microbiële metabolieten, mucosale genezing