Clear Sky Science · nl
CD38 degradeert MAVS via mitofagie om type I-interferonsecretie in nasofaryngeale kankercellen te remmen en verzwakt CD8+ T‑celgemedieerde antitumorimmuniteit
Waarom dit belangrijk is voor kankerbehandeling
Nasofaryngeaal carcinoom is een kanker die achter de neus ontstaat en komt vooral voor in Oost- en Zuidoost-Azië. Immunotherapieën die de eigen T‑cellen van het lichaam vrijmaken hebben voor sommige patiënten het vooruitzicht veranderd, maar de meeste profiteren nog steeds niet. Deze studie onthult een verborgen rem binnen de tumorcellen zelf: een molecuul genaamd CD38 dat stilletjes een intern alarmsysteem uitschakelt en de aanval van kanker-dodende CD8 T‑cellen verzwakt. Het begrijpen en uitschakelen van deze rem zou bestaande immunotherapieën voor veel meer mensen effectief kunnen maken.
Een verborgen schakelaar op tumorcellen
De onderzoekers richtten zich op CD38, een eiwit dat op veel immuuncellen voorkomt maar ook aanwezig is op nasofaryngeale kankercellen. Eerder onderzoek had CD38 in verband gebracht met resistentie tegen veelgebruikte checkpoint-remmers die PD-1 en PD-L1 targeten. Hier vroegen de onderzoekers of CD38 binnen tumorcellen direct beïnvloedt hoe goed CD8 T‑cellen die cellen kunnen herkennen en vernietigen. Door humane kankercellen met of zonder CD38 te kweken naast geactiveerde menselijke CD8 T‑cellen, ontdekten ze dat het verwijderen van CD38 uit de kankercellen de T‑cellen veel krachtiger maakte: ze scheidden hogere niveaus van belangrijke aanvalsmoleculen uit, overleefden beter en doodden meer tumorcellen. Wanneer CD38 werd teruggeplaatst, verslechterde de T‑celfunctie weer, wat wijst op CD38 als een tumor-intrinsieke rem op immuunaanvallen.
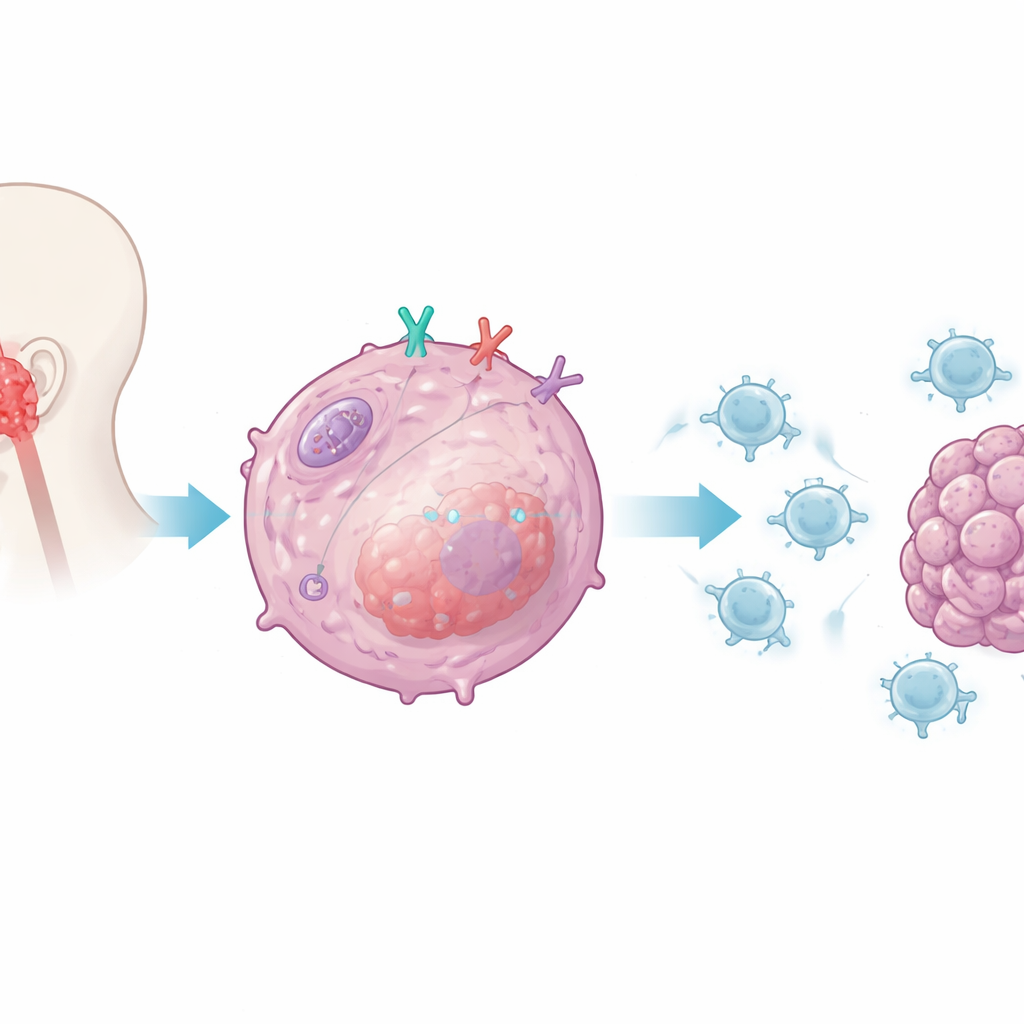
Het interne alarm van de cel dempen
Het team onderzocht vervolgens hoe CD38 dit onderdrukkende signaal veroorzaakt. Ze concentreerden zich op het aangeboren alarmsysteem van de tumorcel, dat normaal gesproken virusachtig genetisch materiaal detecteert en type I‑interferonen activeert — krachtige immuunstimulerende boodschappers. In tumorcellen zonder CD38 zagen de onderzoekers een sterke toename van interferon‑beta en van chemokines die CD8 T‑cellen naar tumoren lokken. Ze toonden aan dat CD38 specifiek het pad dempt dat wordt gecontroleerd door een interne sensor genaamd RIG‑I en zijn adaptorproteïne MAVS, dat op mitochondriën zit, de energiefabrieken van de cel. Wanneer CD38 aanwezig was, werd de activatie van dit pad en van de downstream signaalmoleculen afgezwakt; bij afwezigheid van CD38 stegen de signalering en interferonproductie sterk, waardoor de tumor beter zichtbaar werd voor het immuunsysteem.
Hoe CD38 een belangrijk signaalcentrum vernietigt
Dieper gravend vonden de wetenschappers dat CD38 fysiek geassocieerd is met MAVS op mitochondriën en de samenwerking tussen MAVS en RIG‑I verstoort, waardoor de signaaloverdracht verzwakt. Veel opvallender was dat hogere CD38‑niveaus leidden tot een vermindering van MAVS‑eiwit zonder de genetische code te veranderen, wat wijst op actieve afbraak. Tests met verschillende remmers toonden aan dat dit verlies afhankelijk was van het recyclingsysteem van de cel, bekend als autofagie, en specifiek van een vorm die mitochondriën op doelwit heeft. CD38 verhoogde markers van mitochondriale "zelf‑opname", verlaagde meerdere mitochondriale eiwitten en bevorderde het verpakken van MAVS in autophagosoomstructuren die later worden afgebroken. Het blokkeren van mitochondriale autofagie bewaarde MAVS en herstelde interferonsignalering, wat erop wijst dat CD38 het alarm uitschakelt door MAVS naar het afvalsysteem van de cel te leiden.
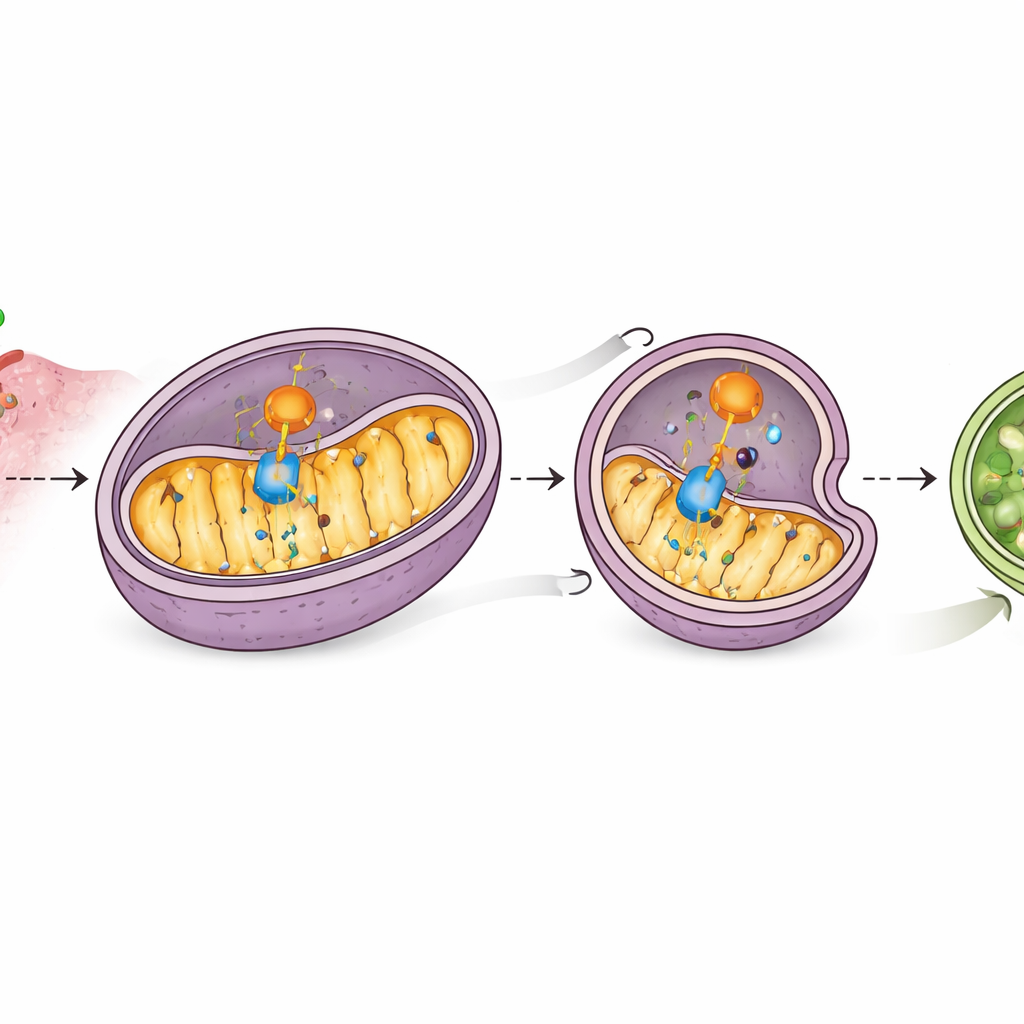
Een hulpje dat mitochondriën naar zelfvernietiging leidt
De studie identificeerde een andere speler, PHB2, een eiwit in mitochondriën dat fungeert als receptor voor gerichte mitochondriale verwijdering. Massaspectrometrie en bindingsexperimenten toonden aan dat CD38 interageert met PHB2 en PHB2’s aanwezigheid in mitochondriën vergroot, waar PHB2 op zijn beurt het kernautofagie-machinery rekruteert. PHB2 bindt ook MAVS, en CD38 versterkt dit contact. Wanneer PHB2 werd verminderd, kon CD38 mitochondriale autofagie niet meer effectief op gang brengen, herstelden MAVS‑niveaus zich en werden interferon-gerelateerde genen opnieuw geactiveerd. Dit onthult een keten van gebeurtenissen: CD38 betrekt PHB2, PHB2 betrekt MAVS, en samen voeren ze MAVS af naar mitochondriën die bestemd zijn voor degradatie, waarmee het interferonalarm wordt gedempt.
Bewijs uit diermodellen
Om de impact in levende organismen te testen, gebruikten de onderzoekers muizentumoren die zo waren geconstrueerd dat ze geen CD38 bevatten. In immuuncompetente muizen groeiden deze tumoren langzamer, bevatten ze meer CD8 T‑cellen en hadden ze een hoger aandeel van cellen die interferon‑gamma produceerden, een kenmerk van actieve antitumorresponsen. Het blokkeren van de receptor voor type I‑interferonen nam dit voordeel weg, wat bevestigt dat interferonsignalering essentieel is voor de verbeterde immuniteit. In gehumaniseerde muizen met nasofaryngeale tumoren remde vermindering van CD38 de groei op vergelijkbare wijze en verhoogde de infiltratie van CD8 T‑cellen, maar dit voordeel verdween wanneer MAVS ook in de tumorcellen werd verlaagd. Deze in vivo‑bevindingen bevestigen dat de CD38–PHB2–MAVS‑as binnen tumorcellen de sterkte van de T‑celrespons van het lichaam bepaalt.
Wat dit betekent voor toekomstige therapieën
Alles bij elkaar laat het werk zien dat CD38 in nasofaryngeale kankercellen fungeert als een interne saboteur van antitumorimmuniteit. Door een selectieve vorm van mitochondriale recycling aan te jagen, put CD38 MAVS uit, verzwakt het de productie van type I‑interferonen, vermindert het antigeenpresentatie en dempt uiteindelijk de aanval door CD8 T‑cellen. Huidige CD38‑blokkers richten zich voornamelijk op de enzymatische activiteit en verwijderen het eiwit niet of herstellen MAVS niet. De auteurs betogen dat nieuwe strategieën gericht op het verlagen van CD38‑niveaus of het verstoren van zijn partnerschap met PHB2 of MAVS het interferonalarm binnen tumoren zouden kunnen heractiveren. In combinatie met bestaande checkpointremmers zouden zulke benaderingen meer nasofaryngeale — en mogelijk andere — kankers van immuunkoud naar immuunresponsief kunnen veranderen.
Bronvermelding: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Trefwoorden: nasofaryngeaal carcinoom, tumorimmunotherapie, type I-interferon, CD8 T‑cellen, mitofagie