Clear Sky Science · nl
Loss-of-function varianten in de CAPN1-activator CD99L2 veroorzaken X-gebonden spastische ataxie
Waarom dit belangrijk is voor families met onverklaarde bewegingsproblemen
Veel mensen leven jaren met onverklaarde loopstoornissen, stijfheid van de spieren of problemen met balans en spraak, zonder ooit de werkelijke oorzaak te achterhalen. Deze studie laat zien hoe moderne DNA-tests sommige van deze families eindelijk antwoorden kunnen geven. De onderzoekers vergeleken niet alleen verschillende genetische tests voor zeldzame bewegingsstoornissen, ze ontdekten ook een voorheen onbekende oorzaak van een aandoening die X-gebonden spastische ataxie wordt genoemd, en wezen daarmee op biologische routes die mogelijk ook belangrijk zijn bij meer voorkomende hersenziekten.
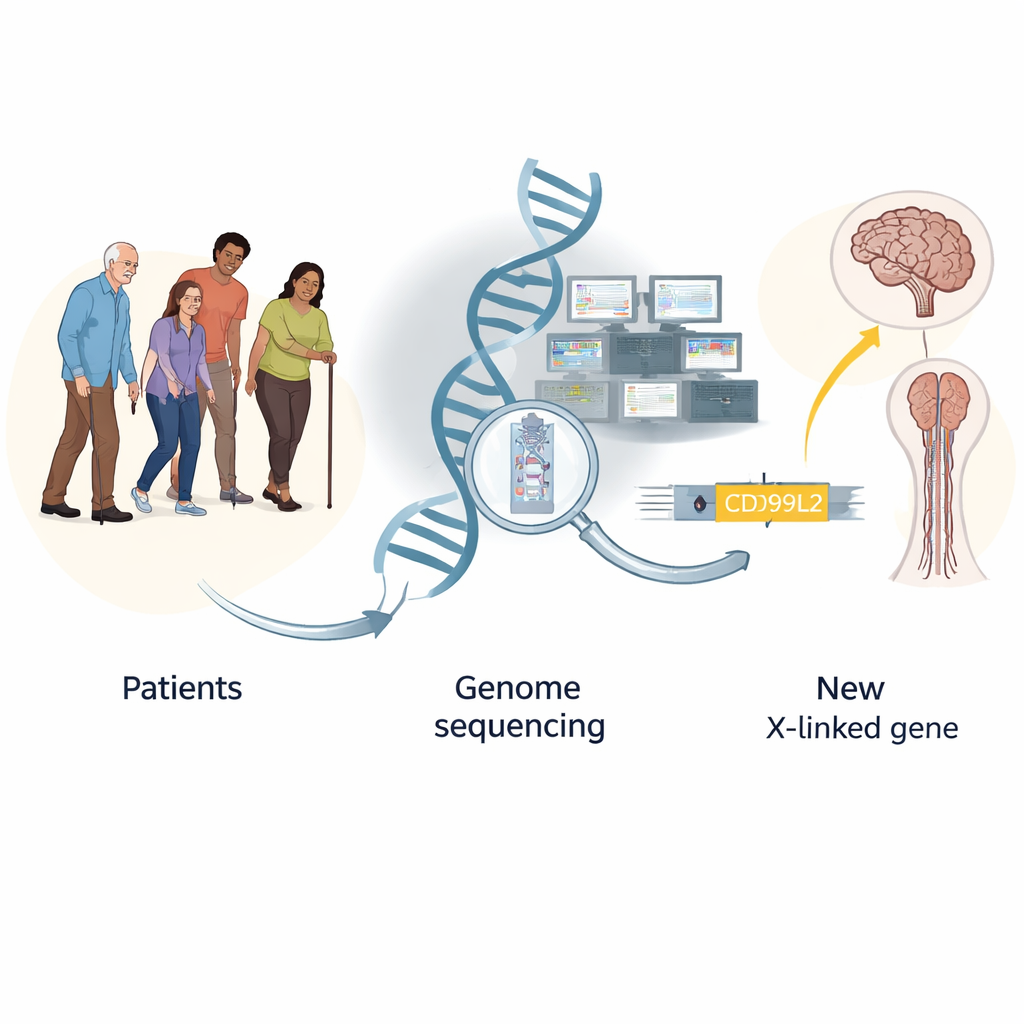
De genetische naalden vinden in een hooiberg van zeldzame ziektes
Zeldzame bewegingsstoornissen, zoals ataxie (onzekere bewegingen) en spastische paraparese (stijve, zwakke benen), worden vaak als erfelijk vermoed, maar bij de meeste patiënten blijven standaardtests zonder resultaat. Het team volgde 2.811 mensen in Duitsland en door heel Europa die gedurende zes jaar werden verwezen met verdenking op een zeldzame bewegingsstoornis. Eerst vergeleken ze traditionele gerichte tests die zoeken naar bekende repeatexpansies in een handvol genen; die gaven in ongeveer 11% van de gevallen een verklaring. Vervolgens gebruikten ze exoomsequencing, die alleen de eiwitcoderende delen van het genoom leest, en vonden daarmee duidelijke genetische verklaringen bij ongeveer 19% van de patiënten, vooral bij degenen met spasticiteit.
Voorbij standaardtests kijken met genoomsequencing
Om verder te gaan, gebruikten de wetenschappers whole-genome sequencing, waarmee vrijwel al het DNA van een persoon wordt gelezen, inclusief regio’s die standaardtests en exomen kunnen missen. Bij 486 personen die deze meer uitgebreide test ondergingen, steeg het diagnostische rendement met ongeveer 7,5 procentpunt, grotendeels omdat genoomsequencing beter is in het opsporen van complexe veranderingen zoals structurele herschikkingen en repeatexpansies. De studie toonde ook aan dat zorgvuldig vastgelegde klinische informatie—vooral specifieke symptoombeschrijvingen, jongere leeftijd bij testen en de combinatie van spasticiteit met andere bewegingsproblemen—hielp voorspellen wie het meest waarschijnlijk een duidelijke genetische diagnose zou krijgen.
Een nieuwe X-gebonden oorzaak van spastische ataxie blootleggen
Zelfs na deze uitgebreide tests bleven veel patiënten zonder diagnose. De onderzoekers bundelden genetische gegevens van meer dan 13.000 personen en gebruikten een "gene-burden"-benadering, waarbij ze onderzochten welke genen vaker verdachte varianten droegen bij patiënten dan bij niet-aangedane controles. Deze analyse wees niet alleen op bekende ziektegenen, maar benadrukte ook sterk een eerder over het hoofd gezien gen op het X-chromosoom genaamd CD99L2. Door resultaten van meerdere families in Europa te combineren, identificeerden ze 25 aangedane mannen uit 20 families die schadelijke varianten in dit gen droegen. Deze mannen ontwikkelden doorgaans loopproblemen, stijfheid van de benen, onduidelijke spraak en soms evenwichtsmoeilijkheden in midden- tot latere volwassenheid, terwijl vrouwelijke dragers grotendeels ongevoelig bleken—patronen die passen bij een X-gebonden aandoening. De varianten vernietigden meestal het normale eiwit of verwijderden cruciale delen ervan, wat sterk suggereert dat verlies van functie de ziekte veroorzaakt.
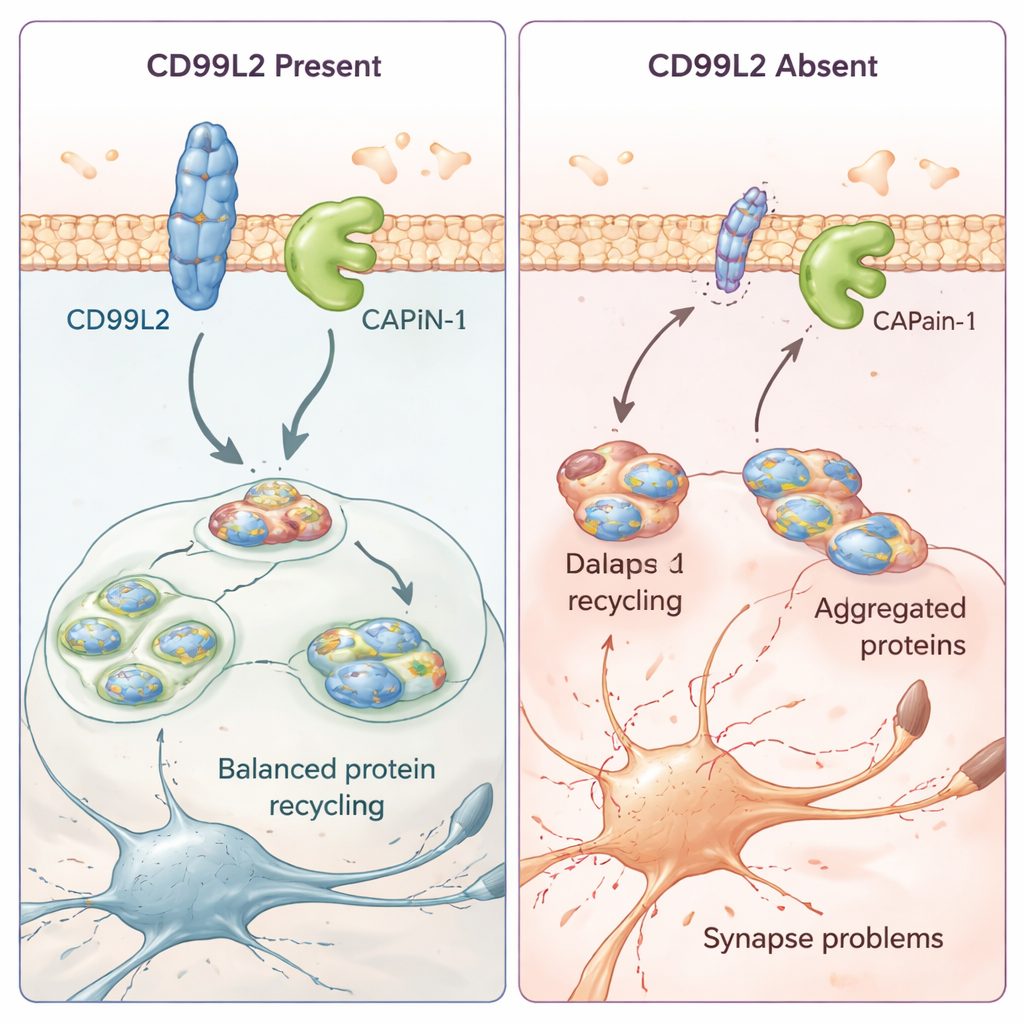
Hoe een klein membraaneiwit helpt hersencellen te beschermen
Om te begrijpen wat CD99L2 eigenlijk in cellen doet, werkte het team met celmodellen en door patiënten afgeleide huidcellen. Ze ontdekten dat het CD99L2-eiwit in het celmembraan zit en meestal wordt gemarkeerd met kleine "ubiquitine"-labels die bepalen hoe lang het overleeft voordat het wordt afgebroken. CD99L2 bindt fysiek aan calpain-1 (CAPN1), een calcium-geactiveerd enzym dat andere eiwitten inkort en helpt synapsen—de contactpunten tussen zenuwcellen—gezond te houden. Wanneer CD99L2 aanwezig en intact is, helpt het calpain-1 gecontroleerd aan- en uit te zetten, en wordt het zelf vervolgens geknipt en gerecycled. Als CD99L2 ontbreekt of structureel veranderd is, raakt de activatie van calpain-1 verstoord. In cellen van patiënten gaat dit samen met verstoorde activiteit van veel genen die met synapsen en zenuwcelcommunicatie te maken hebben, wat erop wijst dat subtiele maar wijdverspreide veranderingen in hersencircuits ten grondslag kunnen liggen aan de geleidelijke bewegingsproblemen.
Wat dit vandaag en morgen betekent voor patiënten
Voor families met onverklaarde spastische ataxie of spastische paraparese biedt dit werk twee soorten vooruitgang. Ten eerste laat het zien dat vroegtijdig whole-genome sequencing, gecombineerd met zorgvuldige klinische beschrijving, de kans op een definitieve genetische diagnose merkbaar kan vergroten. Ten tweede voegt het CD99L2 toe aan de lijst van genen die calpain-activiteit regelen, een route die al in verband is gebracht met andere zeldzame ataxieën en met veelvoorkomende aandoeningen zoals Alzheimer en Parkinson. In alledaagse termen onthult de studie een nieuwe "aan-uit"-schakelaar die helpt het onderhoud van hersencellen in balans te houden; als die schakelaar kapotgaat, verslechteren zenuwcellen langzaam, wat leidt tot stijfheid en slechte coördinatie. Inzicht in deze schakelaar kan uiteindelijk de deur openen naar behandelingen die calpain-activiteit fijnregelen en hersencellen beschermen bij een reeks neurologische ziekten.
Bronvermelding: Menden, B., Incebacak Eltemur, R.D., Demidov, G. et al. Loss-of-function variants in the CAPN1 activator CD99L2 cause X-linked spastic ataxia. Nat Commun 17, 1698 (2026). https://doi.org/10.1038/s41467-026-69337-9
Trefwoorden: spastische ataxie, zeldzame bewegingsstoornissen, genoomsequencing, CD99L2, calpain-1