Clear Sky Science · nl
Benchmarking van EGF-signaleringspadinferentie met behulp van fosfoproteomica en kinase-substraatinteracties
Waarom dit buiten het laboratorium ertoe doet
Onze cellen luisteren voortdurend naar signalen uit hun omgeving en reageren daarop. Een van de belangrijkste van deze signalen is epidermale groeifactor (EGF), die helpt te regelen hoe cellen groeien, zich delen en overleven. Als dit communicatiesysteem fout gaat, kan het kanker en andere ziekten aansturen. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: als we de krachtige meettechnologieën en computermodellen van vandaag gebruiken, hoeveel beter kunnen we het EGF-signaleringspad echt begrijpen dan wat in leerboekdiagrammen staat?
Van rechte lijnen naar realistische bedradingstekening
Traditionele “signaleringspaden” worden vaak als nette, bijna lineaire ketens van eiwitten getekend die een bericht van het celoppervlak naar de celkern doorgeven. Die kaarten zijn in de loop van decennia opgebouwd met langzame, gerichte experimenten die telkens maar een paar eiwitten tegelijk konden bestuderen. De auteurs betogen dat dat ons een beperkte, ‘straatlantaarn’-achtige blik heeft opgeleverd: we weten veel over de paar eiwitten die eenvoudig te bestuderen waren, en veel minder over het bredere netwerk van verbindingen dat waarschijnlijk in echte cellen bestaat.
Luisteren naar duizenden moleculaire schakelaars tegelijk
Om voorbij dat beperkte beeld te komen, gebruikte het team fosfoproteomica, een massaspectrometrie-techniek die tienduizenden kleine chemische tags, fosfaatgroepen, op eiwitten in één experiment kan volgen. Deze tags worden geplaatst door enzymen die kinase heten en fungeren als snelle aan/uit-schakelaars voor signalering. De onderzoekers stelden eerst de meest uitgebreide kaarten van “wie-kan-wie-fosforyleren” tot nu toe samen door drie soorten informatie te combineren: gecureerde bevindingen uit de literatuur, voorspellingen van een kunstmatig-intelligentie model dat eiwitsequenties leest, en grootschalige experimentele screens van kinase-voorkeuren. Dit vergrootte de dekking van bekende of vermoedelijke kinase–substraatrelaties van ongeveer 5% van de meetbare plaatsen tot wel 70–80%.
Het stress-testen van EGF-signaleringsresponsen in veel experimenten
Vervolgens concentreerden ze zich op de EGF-respons, een klassiek pad en belangrijke speler bij kankers van long, borst, huid en hersenen. De groep combineerde drie geavanceerde gepubliceerde datasets met drie nieuwe, zeer diepe tijdsafhankelijke metingen in nieren-afgeleide cellen, plus twee controles waarbij verschillende stimuli werden gebruikt. Samen maten deze experimenten meer dan 40.000 fosforyleringsplaatsen per dataset en volgden hoe die in de minuten na EGF-stimulatie stegen of daalden. Hoewel de algemene patronen enigszins verschilden tussen celtypen en technologieën, werden sleutel-fosforyleringsplaatsen in het EGF-pad herhaaldelijk geactiveerd, wat bevestigt dat het kernsignaal robuust is zelfs over diverse experimenten heen.
Het reconstrueren van het verborgen gesprek tussen kinasen
Nadat ze hadden afgeleid welke kinasen meer of minder actief werden, probeerden de auteurs het onderliggende “gesprek” tussen hen te herbouwen: welke kinasen activeren of beïnvloeden waarschijnlijk welke anderen. Ze zetten hun kinase–substraatkaarten om in kinase–kinase-netwerken en pasten drie computationele strategieën toe, variërend van eenvoudige rangschikkingsschema’s tot een complexere benadering die het resultaat dwingt eruit te zien als een gerichte boom geworteld in de EGF-receptor. Ze vergeleken de resulterende afgeleide paden met verschillende vormen van “grondwaarheid”: een zorgvuldig gecureerde EGF-kaart uit een database, grootschalige experimenten waarbij individuele kinasen werden overgeëxprimeerd, en paren kinaseplaatsen waarvan het gedrag sterk gecorreleerd was in de tijd.
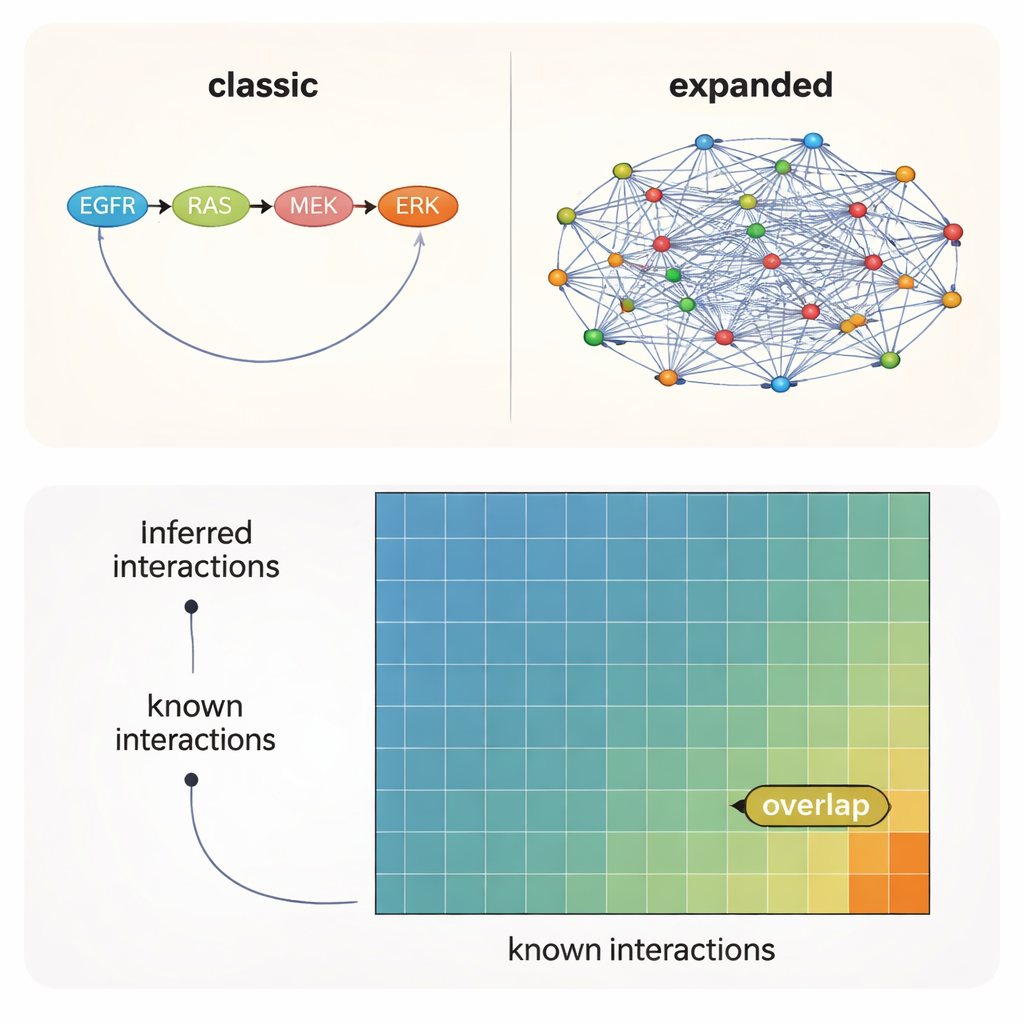
De meest aannemelijke verbindingen staan nog steeds buiten de officiële kaart
Over alle tests heen was één boodschap duidelijk: de keuze van de voorkennis — welk beginnetwerk je in het algoritme stopt — deed er meer toe dan de specifieke methode of zelfs de experimentele context. Netwerken gebouwd uit literatuur herstelden het grootste aantal bekende interacties, terwijl bredere predictieve bronnen naar veel aanvullende, plausibele verbindingen wezen die nog niet formeel zijn gedocumenteerd. Zelfs onder de beste omstandigheden was echter slechts ongeveer 10–12% van de interacties die door de data en modellen werden voorgesteld aanwezig in een van de referentiesets. Met andere woorden: ruwweg 90% van de ondersteunde kinase–kinase-verbindingen bevindt zich in onontgonnen gebied.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de conclusie dat het bekende EGF-paddiagram in leerboeken waarschijnlijk slechts het topje van de ijsberg is. Moderne fosfoproteomica gecombineerd met geavanceerde computationele methoden onthult een veel rijker en complexer signaleringsnetwerk. Veel van deze nieuw voorgestelde verbindingen kunnen wijzen op over het hoofd geziene manieren waarop kankercellen signalen omleiden om aan medicijnen te ontsnappen, of op nieuwe kansen om slimmer samengestelde medicijncombinaties te ontwerpen. De studie bewijst niet dat elke nieuwe verbinding echt is, maar biedt een routekaart en open tools voor onderzoekers om deze ideeën te testen, met als uiteindelijk doel preciezere en effectievere therapieën bij ziekten waarbij EGF-signalerings een centrale rol speelt.
Bronvermelding: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Trefwoorden: EGF-signalerings, fosfoproteomica, proteïnekinasen, celsignaleringsnetwerken, kankerbiologie