Clear Sky Science · nl
Mycobacterium tuberculosis moduleert fosforylering van gastheer-ATP6V1E1 om intracellulair overleven te bevorderen
Waarom dit belangrijk is voor de bestrijding van tuberculose
Tuberculose blijft een van de dodelijkste infectieziekten ter wereld en eist elk jaar meer dan een miljoen levens. Onze immuuncellen beschikken over krachtige “zuurvaste recyclebakken” die normaal binnendringende microben verteren. Dit artikel onthult hoe de tuberculosebacterie, Mycobacterium tuberculosis (Mtb), dat verzuringssysteem binnen onze cellen saboteert, en laat zien dat een geneesmiddel dat deze truc aanvalt geïnfecteerde dieren helpt de infectie effectiever te klaren.
Het zure bad van de cel voor ziekteverwekkers
Wanneer tuberculosebacteriën worden ingeademd in de longen, worden ze snel opgenomen door immuuncellen die macrofagen worden genoemd. De bacteriën belanden in membraanzakjes die eigenlijk moeten versmelten met lysosomen—kleine blaasjes gevuld met spijsverteringsenzymen die het beste werken in een sterk zure omgeving. Die zuurgraad wordt gecreëerd door een moleculaire pomp, de vacuolaire ATPase (V-ATPase), die cellulaire energie gebruikt om protonen in lysosomen te pompen en de interne pH te verlagen. Een correcte verzuring is cruciaal om Mtb af te breken, maar decennia van onderzoek hebben aangetoond dat deze ziekteverwekker op de een of andere manier de compartimenten minder zuur houdt en hierdoor overleeft.
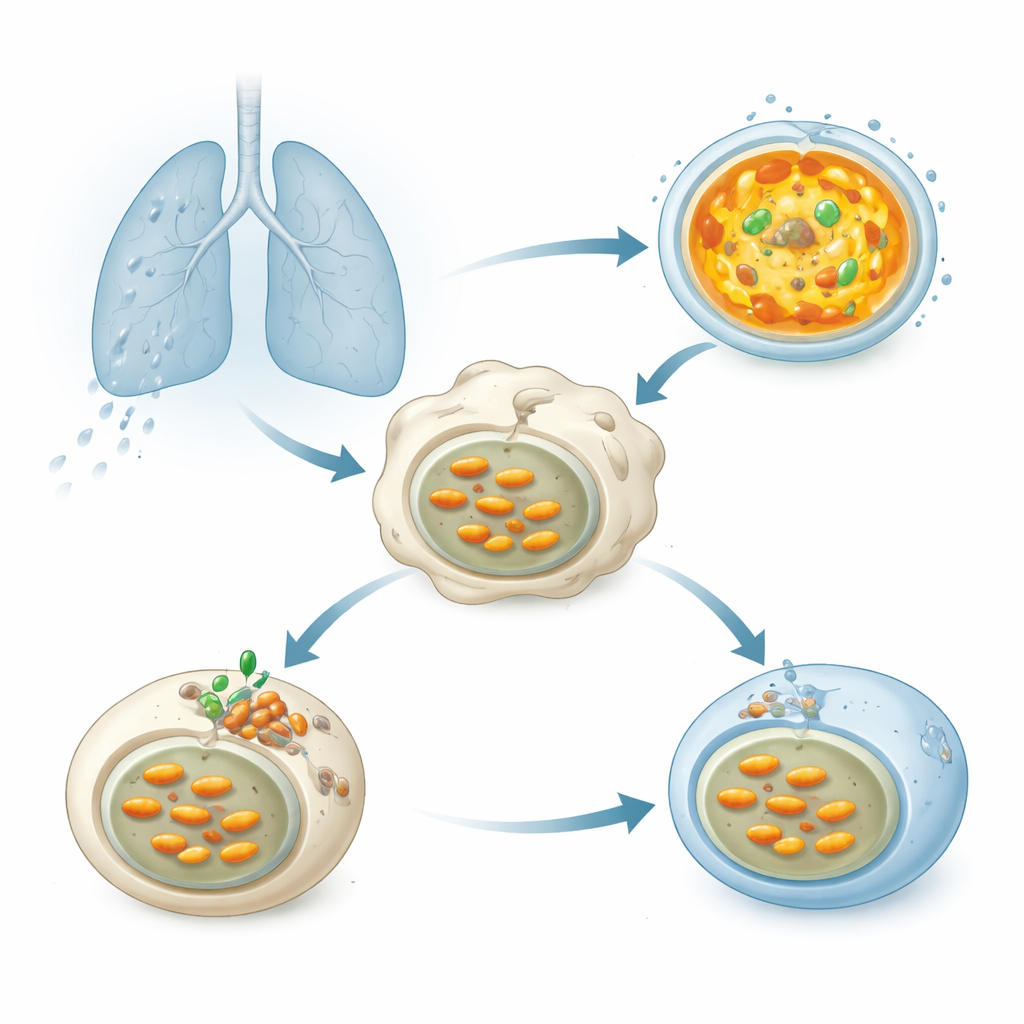
Een verborgen bacterieel hulpje dat verzuring blokkeert
De onderzoekers screeneden meer dan 200 eiwitten die Mtb kan afscheiden om te zien welke de lysosomale verzuring in menselijke cellen verzwakken. Eén eiwit stak er bovenuit: een enzym genaamd Chp2 (ook bekend als Rv1184). Wanneer cellen Chp2 produceerden, gaven hun lysosomen zwakkere signalen met zuurgevoelige kleurstoffen, wat duidt op een hogere, minder vijandige pH. Mtb-stammen die zodanig waren gemodificeerd dat ze Chp2 misten onderdrukten de verzuring niet langer; in geïnfecteerde macrofagen en in muizen werden deze mutantbacteriën efficiënter opgeruimd en veroorzaakten ze minder ernstige longschade. Het herstellen van Chp2 in de mutantstam bracht zowel de blokkade van verzuring als de hogere bacteriële belasting terug, waarmee Chp2 werd geïdentificeerd als een virulentiefactor die Mtb helpt in gastheercellen te blijven bestaan.
De pompsubeenheid van de gastheer die als schakelaar fungeert
Om te begrijpen hoe Chp2 interferentie veroorzaakt met verzuring, zocht het team naar gastheercomponenten waaraan het zou kunnen binden. Ze ontdekten dat Chp2 rechtstreeks hecht aan een specifiek onderdeel van de V-ATPase, een subeenheid genaamd ATP6V1E1 (kortweg E1), die helpt de structuur van de pomp te stabiliseren. Het verhogen van de hoeveelheid E1 in cellen versterkte lysosomale verzuring en bemoeilijkte het overleven van Mtb, terwijl het verminderen van E1 het omgekeerde effect had. Muizen die slechts één werkende kopie van het E1-gen droegen, hadden minder zure lysosomen, hogere bacteriële aantallen in hun longen en ernstiger weefselschade na infectie, wat aantoont dat E1 een belangrijke gastheerverdediger tegen tuberculose is.
Een kinase-etiket op de pomp dat de zuurgraad verlaagt
De auteurs vroegen zich vervolgens af of chemische “labels” op E1 de activiteit van de pomp zouden kunnen bijstellen. Zij ontdekten dat het toevoegen van fosfaatgroepen aan twee specifieke tyrosines (Tyr56 en Tyr57) op E1 fungeert als een rem: het nabootsen van fosforylering verminderde de verzuring en verhinderde de volledige assemblage van de V-ATPase, terwijl het voorkomen van fosforylering het tegenovergestelde effect had. Door een panel van enzymen te screenen identificeerden ze een kinase genaamd BMX als het gastheireiwit dat dit label aanbrengt. Wanneer BMX genetisch of met een klein-molecuulremmer werd geblokkeerd, daalde E1-fosforylering, assembleerde de pomp efficiënter op lysosomale membranen, werden lysosomen zuurder en nam het Mtb-overleven in macrofagen af.
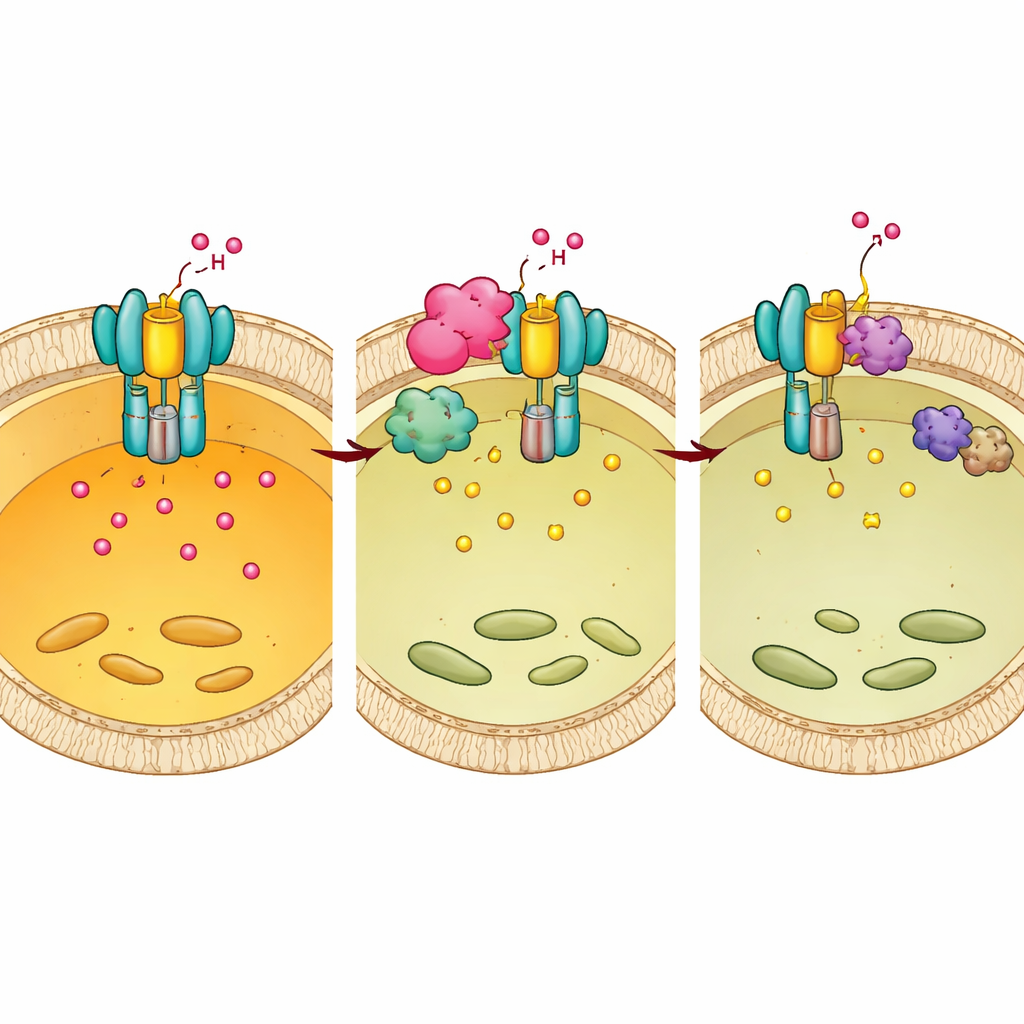
Hoe Mtb de gastheerschakelaar in zijn voordeel herschakelt
Chp2 en BMX blijken samen te werken. Structurele en biochemische experimenten toonden aan dat Chp2 fungeert als een steiger die E1 en BMX dicht bij elkaar op het lysosomale oppervlak brengt, waardoor de fosforylering van E1 op Tyr56/57 wordt versterkt. Deze extra markering verstoort de volledige pompassemblage, verhoogt de lysosomale pH en creëert een mildere omgeving waarin Mtb kan overleven. Wanneer BMX werd geremd, verdween het overlevingsvoordeel dat Chp2 bood, zowel in gekweekte cellen als in geïnfecteerde muizen. Belangrijk is dat behandeling van muizen met de BMX-remmer na infectie de bacteriële aantallen en longpathologie in normale dieren verminderde, maar niet in muizen met verzwakt E1, wat aangeeft dat het middel werkt door effectieve E1-gedreven verzuring te herstellen.
De truc van de ziekteverwekker omzetten in een behandelidee
In eenvoudige bewoordingen laat deze studie zien dat tuberculosebacteriën een hulpstof in onze cellen sluizen die knoeit met de “zuurpomp” van de afvalverwerking en die net genoeg wordt teruggedraaid zodat de microben de vernietiging kunnen doorstaan. Door de pompsubeenheid te identificeren die als de belangrijke regelknop fungeert (E1) en het gastheer-enzym dat deze schakelt (BMX), onthullen de auteurs een precies aangrijpingspunt waar een geneesmiddel kan interveniëren. Het remmen van BMX bij muizen activeert in feite het interne zure bad van de cel opnieuw en verbetert de bacteriële klaring. Deze bevindingen openen de deur naar gastheer-gerichte therapieën die onze eigen cellen vijandiger maken voor Mtb, mogelijk aanvullend op antibiotica en behulpzaam in de strijd tegen medicijnresistente tuberculose.
Bronvermelding: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Trefwoorden: tuberculose, lysosomen, gastheer-gerichte therapie, Mycobacterium tuberculosis, V-ATPase