Clear Sky Science · nl
Ontwikkeling van een krachtige monoklonale antilichaam voor de behandeling van humane metapneumovirusinfecties
Waarom een verborgen wintervirus ertoe doet
Elk griep- en verkoudheidsseizoen stuurt een weinig bekend virus, het humane metapneumovirus (HMPV), stilletjes miljoenen jonge kinderen, ouderen en mensen met een verzwakt immuunsysteem naar klinieken en ziekenhuizen. In tegenstelling tot zijn verwant, het respiratoir syncytieel virus (RSV), bestaan er geen vaccins of gerichte behandelingen voor HMPV. Deze studie rapporteert de ontdekking van een krachtig in het laboratorium gemaakt antilichaam, genaamd 4F11, dat HMPV in cellen kan stoppen en geïnfecteerde dieren kan beschermen, en daarmee wijst op een broodnodig nieuw middel voor sommige van de meest kwetsbare patiënten.
Het virus dat onder de radar vliegt
HMPV is een veelvoorkomend luchtwegvirus wereldwijd en is verantwoordelijk voor naar schatting 14 miljoen lagere luchtweginfecties bij kinderen onder vijf jaar per jaar; het legt ook een zware tol bij volwassenen ouder dan 60. Voor patiënten met ernstig verzwakte immuunsystemen — zoals ontvangers van stamceltransplantaties — kan het sterftecijfer door HMPV-longinfecties alarmerend hoog zijn. Vaccins verschijnen slechts langzaam voor verwante virussen zoals RSV, en zelfs als er een HMPV-vaccin bestond, zouden veel sterk immuungecompromitteerde patiënten slecht reageren. Vanwege deze leemte wenden onderzoekers zich tot monoklonale antilichamen — precies gerichte immuuneiwitten die als geneesmiddel gegeven kunnen worden — om ernstige infecties te voorkomen of te behandelen.
Een uitblinkend beschermend antilichaam vinden
Het team ging op zoek naar een antilichaam met drie belangrijke eigenschappen: het moest extreem krachtig zijn, werken tegen veel verschillende HMPV-stammen en het virus weinig ruimte laten om resistentie te ontwikkelen. Ze concentreerden zich op het fusie-eiwit van het virus, een veerbeladen structuur op het virale oppervlak die van vorm moet veranderen om het virus te laten samensmelten met en binnendringen in longcellen. Met een ‘aas- en wissel’-strategie gingen ze op zoek naar zeldzame menselijke B-cellen uit bloed- en miltmonsters die één stam van HMPV konden herkennen maar een andere konden neutraliseren, waarmee ze antistoffen met brede werkzaamheid enrichten. Uit meer dan duizend kandidaatcellen isoleerden ze drie veelbelovende antilichamen en vonden dat één — 4F11 — uitzonderlijk krachtig was: het blokkeerde infectie van cellen bij concentraties die bijna 50 keer lager lagen dan bij een eerder toonaangevend antilichaam en werkte tegen alle vier grote wereldwijde HMPV-subtypes.
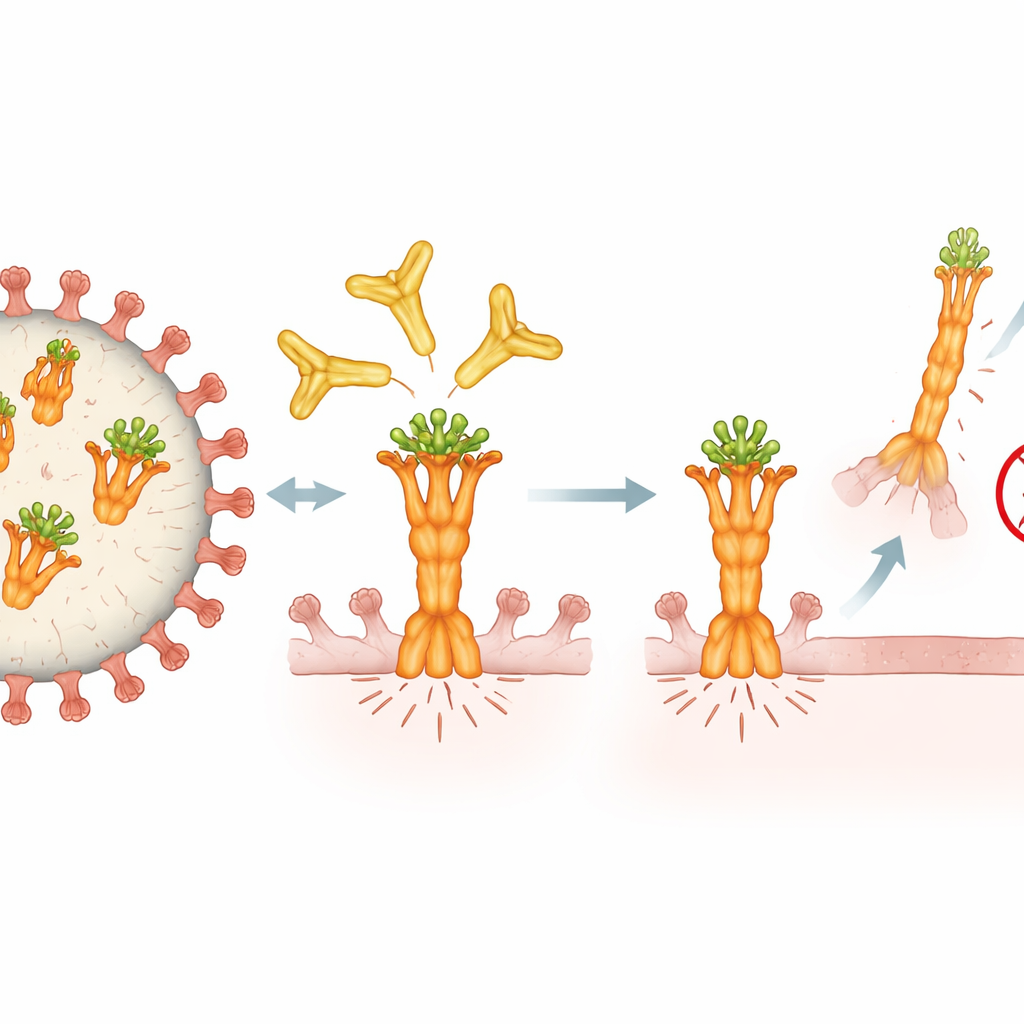
Hoe 4F11 het zwakke punt van het virus vastgrijpt
Om te begrijpen waarom 4F11 zo effectief is, gebruikten de onderzoekers cryo-elektronenmicroscopie met hoge resolutie om te visualiseren hoe het aan het fusie-eiwit vastklampt. Ze ontdekten dat 4F11 een klein, geconserveerd stukje aan de bovenkant van de prefusie-vorm van het eiwit target — de veer voordat hij losschiet. In tegenstelling tot andere antilichamen die drie exemplaren per fusie-eiwit binden, zit 4F11 alleen aan de top in een één-op-één-orde, reikt recht naar beneden en grijpt zelfs een suikerdecoratie vast die het oppervlak afschermt. Deze ongewone bindingshoek en de afhankelijkheid van die suiker maken 4F11 tot een uniek type antilichaam. Het herkent alleen de prefusie-vorm, die aanwezig is op het infectieuze virus, en voorkomt waarschijnlijk dat het eiwit zich hervouwt in de vorm die nodig is om een gastheercel te doorboren en te fuseren.
Kan het virus ontsnappen — en tegen welke prijs?
Het team dwong het virus daarna om in celkweek te groeien in de constante aanwezigheid van 4F11 om te zien hoe gemakkelijk het zou kunnen ontsnappen. Vergeleken met een ander antilichaam als controle, dat snel de verschijning van meerdere ontsnappingsmutaties aandreef, had HMPV veel meer moeite om langs 4F11 heen te glippen. Slechts één enkele verandering in het fusie-eiwit, waarbij één aminozuur op positie 179 werd gewijzigd, verstoorde volledig de binding van 4F11. Virussen die deze mutatie droegen, groeiden echter veel slechter dan het normale virus, wat wijst op een ernstige aantasting van de virale fitness. Doorzoekingen in databases met honderden HMPV-sequenties toonden aan dat deze schadelijke wijziging nooit in de natuur is waargenomen, wat suggereert dat hoewel het virus in principe in het laboratorium aan 4F11 kan ontsnappen, het daarvoor een zulke hoge groeikosten betaalt dat verspreiding in de echte wereld onwaarschijnlijk is.
Bescherming testen in een diermodel
Laboratoriumkracht moet zich nog vertalen naar echte bescherming. Om dit te testen, infecteerden de onderzoekers gouden Syrische hamsters met HMPV en behandelden ze een dag later met 4F11 — waarmee vroege therapie in plaats van preventie werd nagebootst. Een enkele injectie met een lage dosis 4F11 verlaagde de virusniveaus sterk in zowel de longen als de neusholtes, en bij de hogere dosis verdween het detecteerbare virus uit de longen bij de meeste dieren volledig. Opmerkelijk was dat deze doses lager waren dan die gebruikt voor verschillende monoklonale antilichamen die al voor RSV bij mensen zijn goedgekeurd. Ter vergelijking bood een eerder beschreven antilichaam dat kruisreageert met meerdere virussen bij dezelfde dosis weinig bescherming, wat de bijzondere kracht van 4F11 als gerichte HMPV-therapie onderstreept.
Wat dit voor patiënten zou kunnen betekenen
Gezamenlijk positioneren deze bevindingen 4F11 als een sterke kandidaat voor klinische ontwikkeling. Het combineert hoge potentie, brede dekking van circulerende HMPV-stammen, een onderscheidende manier om een kwetsbare regio van het fusie-eiwit vast te grijpen, en een resistentielandschap waarin de voor de hand liggende ontsnappingsroute voor het virus gepaard gaat met een aanzienlijke zelftoegebrachte handicap. Voor zuigelingen, oudere volwassenen en immuungecompromitteerde patiënten met een hoog risico op ernstige HMPV-ziekte zou een op 4F11 gebaseerd geneesmiddel op den duur zowel noodbehandeling na infectie als extra bescherming naast of in plaats van vaccins kunnen bieden.
Bronvermelding: Harris, E.D., McGovern, M., Pernikoff, S. et al. Development of a potent monoclonal antibody for treatment of human metapneumovirus infections. Nat Commun 17, 2714 (2026). https://doi.org/10.1038/s41467-026-69328-w
Trefwoorden: human metapneumovirus, monoklonaal antilichaam, ademhalingsinfectie, fusie-eiwit, antivirale therapie