Clear Sky Science · nl
Preoptisch kisspeptine-nNOS-GnRH (KiNG) neuronennetwerk reguleert LH‑ritmiek via activeren‑remmen bij muizen
Waarom dit hersenonderzoek belangrijk is voor vruchtbaarheid
Ovulatie en vruchtbaarheid hangen af van een kleine groep hersencellen die een sleutelhormoon in pulsen en af en toe in een grote piek vrijgeven. Als de timing hiervan verstoord raakt, kan voortplanting mislukken. Deze studie onthult hoe twee soorten signaalmoleculen in de muizenhersenen — één die activiteit aanzet en een andere die die activiteit stilletjes weer uitschakelt — samen deze hormonale ritmes vormgeven. Inzicht in dit verborgen tijdschakelingcircuit kan uiteindelijk helpen bepaalde vormen van onvruchtbaarheid te verklaren en nieuwe behandelrichtingen voor voortplantingsstoornissen suggereren.
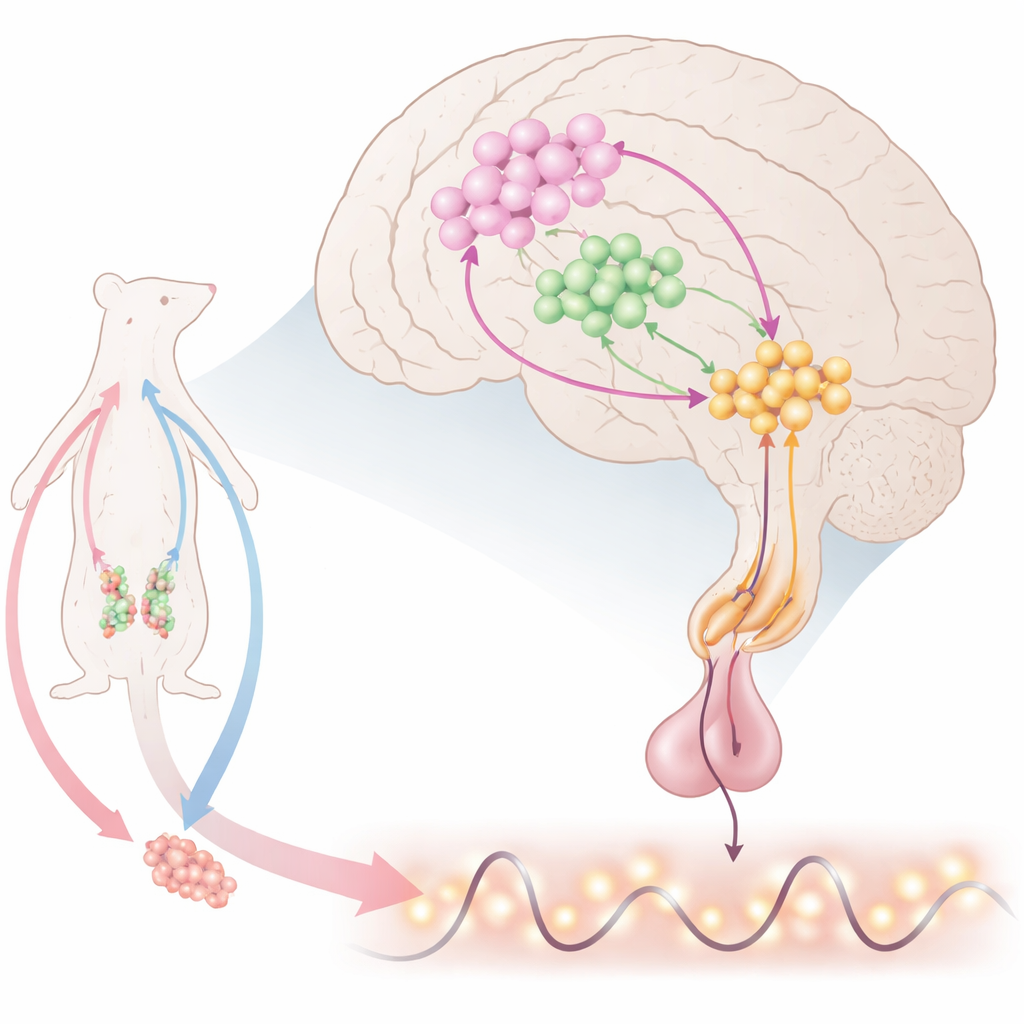
De interne klok van de hersenen voor voortplanting
Diep in de hersenen geven gespecialiseerde zenuwcellen gonadotropine‑vrijmakend hormoon (GnRH) af, dat de hypofyse aanzet tot het uitscheiden van luteïniserend hormoon (LH) en follikelstimulerend hormoon. Deze hormonen regelen op hun beurt de eierstokken en testes. GnRH komt niet constant vrij; het verschijnt als regelmatige pulsen en, bij vrouwen, als een grote pre‑ovulatorische piek. Wetenschappers weten dat veel signalen op GnRH‑cellen inwerken, maar de precieze combinatie die zowel pulsen als pieken voortbrengt bleef onduidelijk. Dit werk richt zich op een klein gebied voor in de hypothalamus, waar GnRH‑cellen samenkomen met twee andere belangrijke spelers: kisspeptine‑producerende neuronen die GnRH opwekken, en neuronen die stikstofoxide (NO) maken, een gasvormig signaal dat over korte afstanden kan diffunderen.
Een aan‑uit partnerschap tussen twee signalen
De onderzoekers stellen een driedelig “KiNG”-netwerk voor, bestaande uit kisspeptine, NO‑producerende (nNOS) neuronen en GnRH‑cellen. Kisspeptine is een krachtige activator die GnRH‑ en LH‑afgifte kan stimuleren, maar constante stimulatie leidt juist tot uitputting van het systeem, wat suggereert dat er een interne rem nodig is. Met behulp van zeer gevoelige moleculaire markers, genetische instrumenten en hersenplakopnames in muizen laat het team zien dat kisspeptine meer doet dan alleen GnRH‑neuronen direct te activeren. Het activeert ook nabije nNOS‑neuronen in het preoptische gebied, vooral in een regio die OV/MePO wordt genoemd. Wanneer kisspeptineniveaus stijgen, produceren deze nNOS‑cellen bursts van NO, die de productie van een tweede boodschapper, cGMP, in omliggende cellen — waaronder GnRH‑neuronen zelf — op gang brengen. Dit NO–cGMP‑signaal dempt de vuurgewoonte van GnRH, en vormt zo een ingebouwde uit‑schakelaar voor de kisspeptine‑drive.
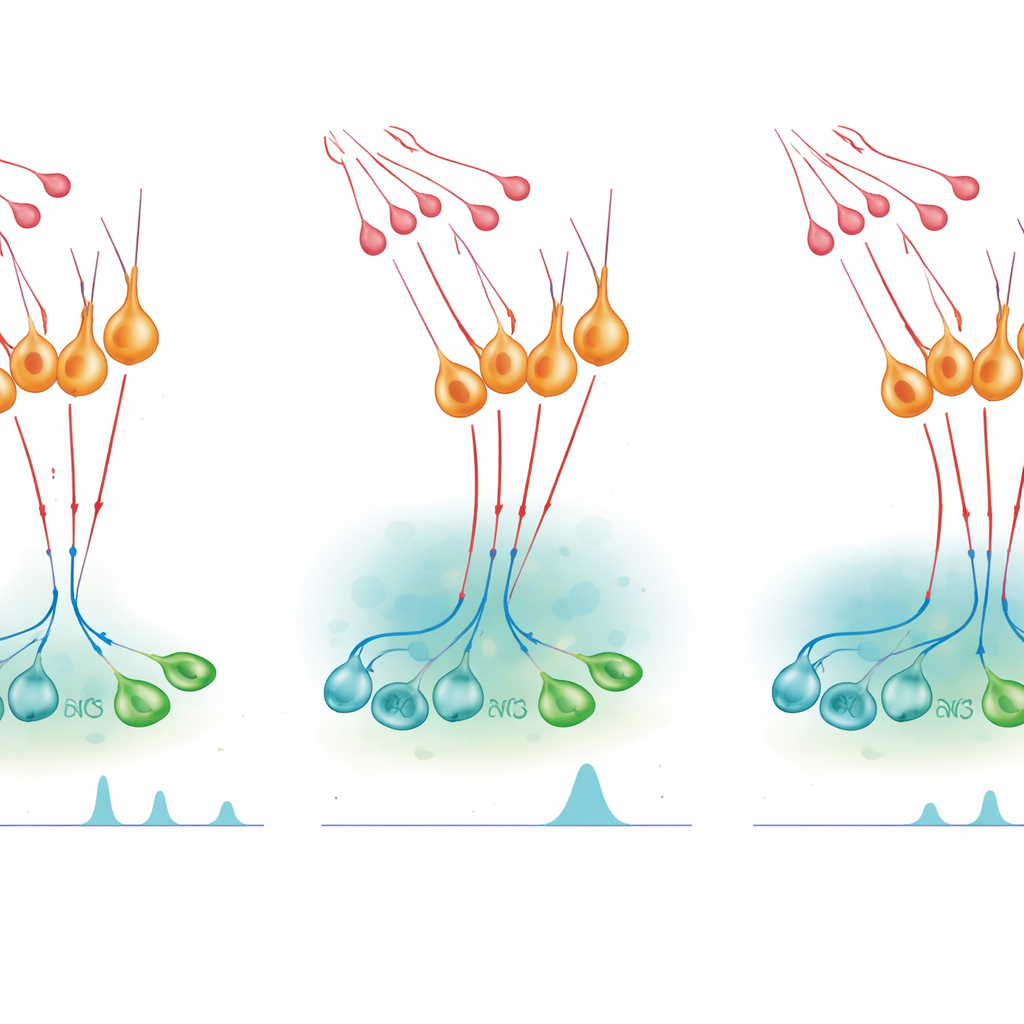
Hormoonpieken aanzetten en terugschakelen
Om te testen hoe dit microcircuit hormoonafgifte beïnvloedt, gebruikten de onderzoekers chemogenetische schakelaars — ontworpen receptoren die door een verder inerte stof worden geactiveerd — om nNOS‑neuronen in levende muizen aan of uit te zetten. Kunstmatige activatie van nNOS‑cellen tijdens een normaal rustige fase van de vrouwelijke cyclus was voldoende om een piekachtige stijging van LH in het bloed te veroorzaken; hetzelfde gold voor mannelijke dieren. Het blokkeren van NO‑productie maakte dit effect ongedaan, wat toont dat NO van deze neuronen noodzakelijk is voor de piek. Toch leverde het remmen van nNOS‑neuronen of het verminderen van hun kisspeptinegevoeligheid een overdreven en verlengde LH‑stijging op na een dosis kisspeptine. Farmacologische middelen die NO‑synthese blokkeren hadden een vergelijkbaar versterkend effect, terwijl een middel dat cGMP‑signaal verlengt de kisspeptinerespons inkortte en latere LH‑afgifte verminderde. Samen wijzen deze experimenten erop dat NO zowel helpt GnRH‑neuronen te synchroniseren om pieken te creëren als de duur beperkt waarin kisspeptine ze kan laten vuren.
Een flexibele ritmiek door de ovariumcyclus heen
De studie laat ook zien dat deze aan‑uit balans verschuift gedurende de vrouwelijke cyclus. Met een gevoelige RNA‑detectiemethode vonden de auteurs dat meer nNOS‑neuronen de kisspeptinereceptor tot expressie brengen op de dag vóór de ovulatie, wanneer oestrogeenspiegels hoog zijn en de LH‑piek optreedt. Tijdens de rustiger fasen reageren minder nNOS‑neuronen op kisspeptine, waardoor slechts kleine, lokale hoeveelheden NO ontstaan die de GnRH‑pulsen zachtjes remmen zonder ze te stoppen. Op de piekdag zorgen sterkere kisspeptine‑input en verhoogde receptorexpressie voor een grote toename van NO‑output, waardoor NO zich verder kan verspreiden en kortstondig veel GnRH‑neuronen tegelijk kan stilleggen. Wanneer het NO‑signaal wegvalt, veren deze cellen gezamenlijk terug en genereren ze de grote, gecoördineerde LH‑piek die nodig is voor ovulatie.
Wat dit betekent voor de menselijke gezondheid
In eenvoudige bewoordingen laat dit werk zien dat hetzelfde signaal dat GnRH‑neuronen activeert — kisspeptine — ook een vertraagd remsysteem via NO inroept, waardoor hormonale uitbarstingen krachtig maar niet ongecontroleerd zijn. Het KiNG‑netwerk fungeert dus zowel als gaspedaal als rem voor reproductieve timing: het stemt GnRH‑pulsen af tijdens het grootste deel van de cyclus en vormt de piek die de ovulatie op gang brengt. Omdat genetische veranderingen in kisspeptine‑ en NO‑paden bij mensen met voortplantingsproblemen zijn aangetroffen, kan begrip van dit fijn afgebalanceerde circuit nieuwe inzichten geven om onvruchtbaarheid en verwante aandoeningen te diagnosticeren en behandelen.
Bronvermelding: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Trefwoorden: voortplantingshormonen, hypothalamus, kisspeptine, stikstofoxide, timing van ovulatie