Clear Sky Science · nl
Histonlactylering verhoogt CXCL1-expressie voor neutrofielinfiltratie en immuunontsnapping bij alvleesklierkanker
Waarom deze kankerstudie ertoe doet
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, deels omdat deze vaak bestand is tegen moderne immunotherapieën die bij andere tumoren werken. Deze studie onthult hoe alvleeskliertumoren hun eigen suikermetabolisme herschakelen om het immuunsysteem stilletjes uit te schakelen, en hoe het blokkeren van dat proces mogelijk de deur opent voor de verdedigingsreacties van het lichaam — en voor bestaande middelen — om terug te slaan.
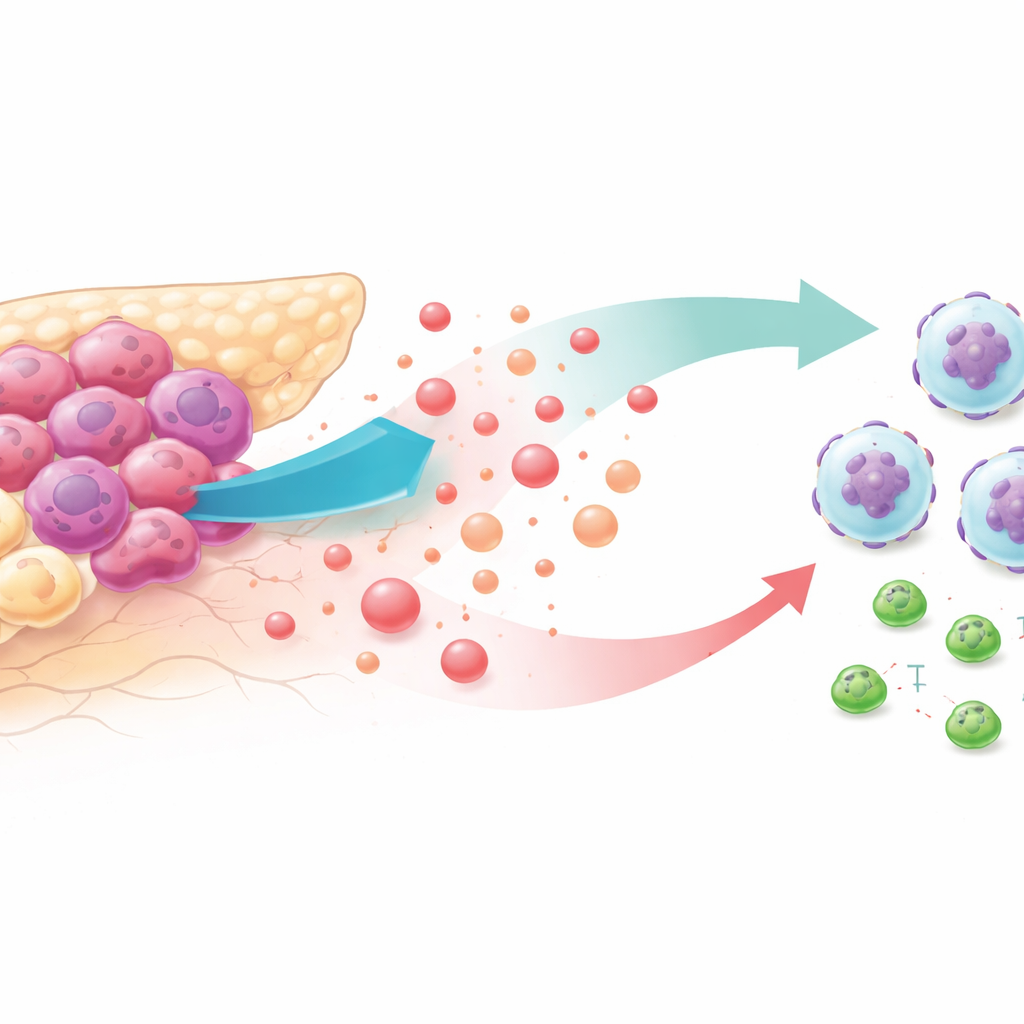
Suikerhongerige tumoren en een vijandige omgeving
Kankercellen staan bekend om het razendsnel verbranden van glucose, zelfs wanneer er voldoende zuurstof aanwezig is. Deze "hoog-glycolyse" levensstijl overspoelt de tumoromgeving met lactaat, een bijproduct dat ooit werd afgedaan als metabolisch afval. Door patiëntentumordatabases en muismodellen te analyseren, vonden de onderzoekers dat alvleesklierkankers met de meest intense glycolyse vol zaten met neutrofielen — witte bloedcellen die in deze context tumorgroei ondersteunen — en minder kanker-dodende CD8 T-cellen hadden. Patiënten wier tumoren dit profiel vertoonden, leefden doorgaans korter, wat suggereert dat veranderd metabolisme en immuunontsnapping nauw verbonden zijn.
Hoe tumoren lactaat gebruiken om de verkeerde hulp in te roepen
Om te begrijpen hoe glycolyse neutrofielen aantrekt, schakelde het team tumor-glycolyse omlaag met geneesmiddelen of genetische ingrepen in cellijnen van alvleesklierkanker en bij muizen. Wanneer suikervetrekking werd geblokkeerd, gaven tumorcellen veel minder van een chemisch signaal vrij dat CXCL1 heet, en de circulerende niveaus van dit signaal daalden bij muizen en in patiëntmonsters. In laboratoriummigratietests bewogen neutrofielen gretig richting medium van sterk glycolytische kankercellen, maar niet richting medium van glycolyse-geblokkeerde cellen — tenzij de onderzoekers zuiver CXCL1 toevoegden. In levende muizen bracht het herstellen van CXCL1 in tumoren met verminderde glycolyse het aantal neutrofielen weer omhoog en verzwakte het het antitumoreffect van glycolyse-inhibitie.
Een nieuwe epigenetische schakel aangedreven door lactaat
De studie zoomde vervolgens in op het niveau van DNA-verpakking. Onze genen zijn gewikkeld rond spoelachtige eiwitten die histonen heten, waarvan de chemische tags fungeren als aan/uit-schakelaars voor genactiviteit. De auteurs tonen aan dat in alvleesklierkanker door glycolyse geproduceerd lactaat een specifieke "lactyl"-tag toevoegt op één histonpositie, bekend als H3K18. Deze modificatie, histon H3K18-lactylering genoemd, was duidelijk hoger in tumorweefsel dan in normaal pancreas. Wanneer glycolyse werd geblokkeerd, nam de lactylering op H3K18 af, vooral nabij de regelregio van het CXCL1-gen, en daalde de CXCL1-productie. Het teruggeven van lactaat herstelde zowel het histontag als de CXCL1-expressie. Over patiëntmonsters laten tumoren met meer H3K18-lactylering ook hogere CXCL1-waarden zien, wat dit moleculaire kenmerk koppelt aan een pro-tumorale immuunsamenstelling.
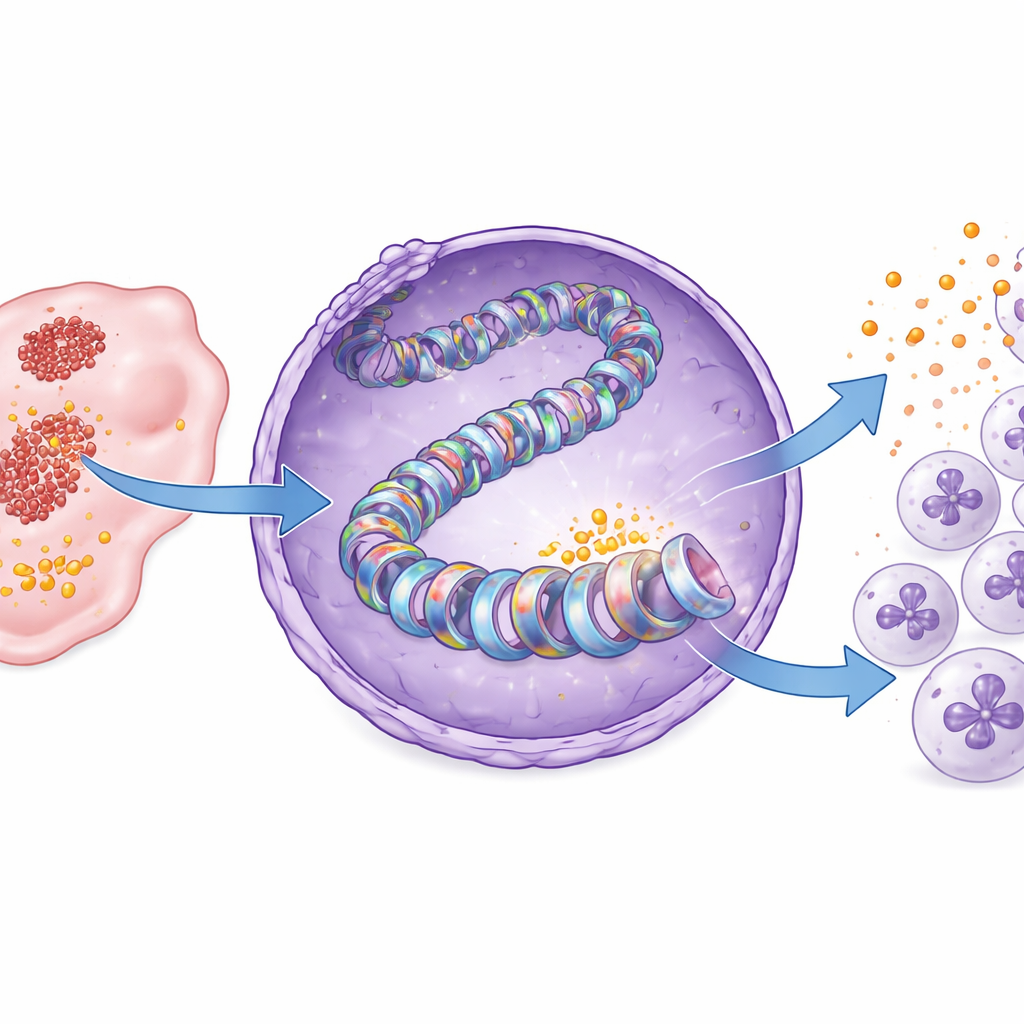
Het identificeren van het enzym en een geneesmiddelbaar zwak punt
Histontags worden geschreven door gespecialiseerde enzymen. Door remmers van bekende histon-modificerende eiwitten te screenen, identificeerden de onderzoekers een enzym genaamd PCAF als belangrijke schrijver van het H3K18-lactylatiemerk in alvleesklierkanker. Structurele modellering suggereerde dat PCAF lactyl-CoA kan binden, de geactiveerde vorm van lactaat die wordt gebruikt voor het taggen, en biochemische assays bevestigden dat gezuiverd PCAF direct lactylgroepen aan histon H3 kan toevoegen. Het blokkeren van PCAF met een klein molecuul, bromosporine, verlaagde H3K18-lactylering en CXCL1-productie in kankercellen en in muizentumoren. Als gevolg drongen minder neutrofielen de tumoren binnen, stapelden meer CD8 T-cellen zich op en vertraagde de tumorgroei, allemaal zonder duidelijke gewichtsverlies of toxiciteit bij de muizen.
Een koude tumor verhitten met combinatietherapie
Aangezien standaard immuuncheckpointrmiddelen zoals anti–PD-1-antilichamen beperkte successen hebben laten zien bij alvleesklierkanker, testte het team of het ontmantelen van de lactaat–PCAF–CXCL1-route deze tumoren beter vatbaar kon maken. In zowel subcutane als orthotopische pancreasmuismodellen krimpte combinatiebehandeling met bromosporine en anti–PD-1 de tumoren meer dan een van beide behandelingen alleen, verminderde neutrofielinfiltratie, versterkte actieve CD8 T-cellen en verlengde de overleving significant. Dit suggereert dat het doorknippen van de metabolische "siren" van de tumor voor neutrofielen helpt een immunologisch "koude" tumor om te zetten in een "warmere" tumor die checkpointherapie beter kan aanspreken.
Wat dit betekent voor toekomstige behandeling
In eenvoudige woorden onthult de studie een kettingreactie: alvleeskliertumoren verbranden suiker, scheiden lactaat uit, gebruiken dat lactaat om een epigenetische schakel op hun DNA-verpakkingsproteïnen om te zetten, zetten CXCL1 hoger en roepen daarmee neutrofielen die hen helpen verbergen voor doder-T-cellen. Het onderbreken van deze keten bij de PCAF-stap met een geneesmiddel vertraagt niet alleen tumoren maar maakt bestaande immunotherapie ook krachtiger in muizen. Hoewel er meer werk nodig is om de veiligheid te waarborgen en de beste manier te vinden om deze route bij mensen te richten, benadrukken deze bevindingen een veelbelovende strategie: het herprogrammeren van het tumormetabolisme en de genregelaars om het immuunsysteem een eerlijke kans te geven.
Bronvermelding: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Trefwoorden: alvleesklierkanker, tumormetabolisme, histonlactylering, tumormicro-omgeving, kankerimmunotherapie