Clear Sky Science · nl
Het gebruik van voorspelbare bindingskinetiek van DNA-PAINT om superresolutiebeelden te ontbruisen
Scherpere blik op de kleine wereld
Moderne microscopen kunnen nu individuele moleculen in cellen “zien”, maar deze beelden zitten vaak vol misleidende achtergrondpuntjes. Deze studie introduceert een manier om zulke beelden op te schonen door gebruik te maken van hoe stukjes DNA van nature aan elkaar binden en loslaten in de tijd. Het resultaat zijn duidelijkere beelden van het moleculaire apparaatwerk in cellen, wat van belang is voor alles van fundamentele biologie tot geneesmiddelenontwikkeling.
Hoe een knippertruc verborgen details onthult
Een krachtige beeldgevingsmethode, DNA-PAINT genoemd, zet het toevallige hechten van korte DNA-strengen om in een superresolutiemicroscoop. Eén DNA-streng is aan het eiwit bevestigd dat een onderzoeker wil zien; een overeenkomende streng met een fluorescerende kleurstof zweeft in de oplossing. Wanneer de zwevende streng kort bindt aan zijn partner, geeft dat een klein lichtflitsje. Door veel van zulke knipperingen vast te leggen en hun locaties precies te bepalen, kunnen onderzoekers de posities van eiwitten reconstrueren met nanometernauwkeurigheid—veel scherper dan bij conventionele lichtmicroscopie.
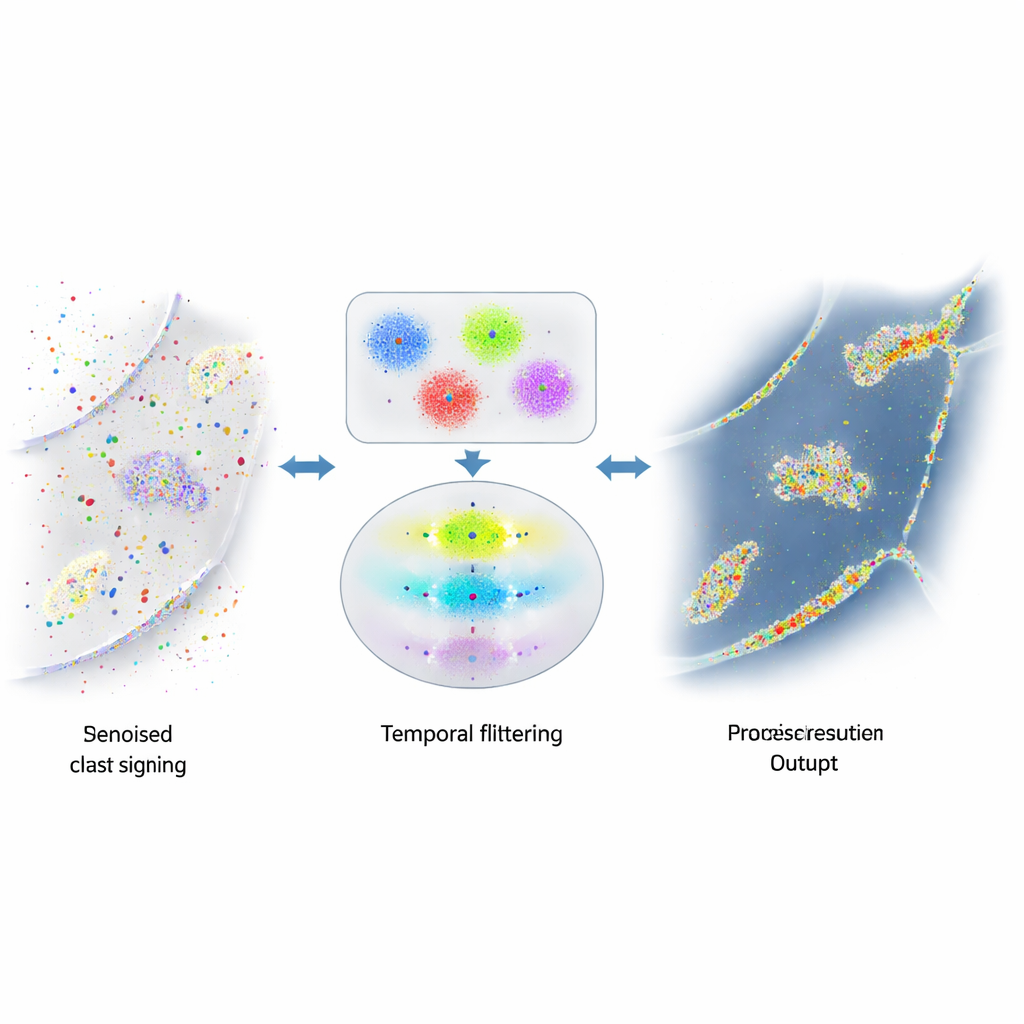
Wanneer nuttige signalen ondergesneeuwd raken door ruis
De kracht van DNA-PAINT—veel vrij bewegende fluorescerende strengen—schept ook een probleem. Deze strengen hechten zich soms op plaatsen waar ze niet zouden moeten hechten, bijvoorbeeld aan willekeurige celoppervlakken of aan het overvloedige DNA in de kern. Die toevallige flitsen zijn in uiterlijk niet te onderscheiden van de echte en verontreinigen het eindbeeld met valse stippen en clusters. Eerdere pogingen om deze ruis te verminderen richtten zich op het aanpassen van de chemie om ongewenst hechten zeldzamer te maken, of op ruwe regels om duidelijke uitschieters te vinden. Toch bleef een aanzienlijk deel van het misleidende signaal over, wat beperkte hoe betrouwbaar wetenschappers eiwitnummers of ruimtelijke relaties konden meten.
De tijd gebruiken om waarheid van bedrog te onderscheiden
De auteurs realiseerden zich dat echte DNA-paren in DNA-PAINT een eenvoudige timingregel volgen: de pauzes tussen echte bindingsevenementen volgen een voorspelbaar, exponentieel patroon. Daarentegen volgen willekeurige hechtgebeurtenissen dat niet. Ze bouwden een meerstapsalgoritme dat eerst nabijgelegen knipperingen groepeert in kleine clusters op basis van hun locatie, met een combinatie van dichtheidsgebaseerde clustering en k-means om complexe vormen te splitsen in lokalisatiegroottes. Voor elke cluster construeren ze vervolgens een "tijdbaan" van bindingsevenementen, waarbij snel aan- en uitknipperen van dezelfde binding zorgvuldig wordt samengevoegd tot enkele gebeurtenissen. Ten slotte passen ze een statistische toets toe om te onderzoeken of de intervallen tussen gebeurtenissen in elke cluster overeenkomen met het verwachte exponentiële gedrag. Clusters die slagen worden als echt behandeld; clusters die falen worden als ruis verworpen.
De methode testen in echte cellen
Om hun aanpak te testen, beeldde het team het celhechteiwit E-cadherine af in eitjes van vruchtvlieg, waar sommige cellen het gemarkeerde eiwit produceerden en aangrenzende cellen dat niet deden. Dit creëerde naast elkaar gebieden die rijk waren aan echt signaal en gebieden die alleen achtergrond zouden moeten bevatten. Door af te stemmen hoeveel bindingsevenementen een cluster moet vertonen voordat deze wordt getest, vonden ze instellingen die meer dan 90% van de valse clusters verwijderden terwijl meer dan 98% van de echte clusters bij celranden behouden bleef. In de ontbruikte beelden werden fijne structuren zoals dunne buisvormige structuren en vesikels veel duidelijker. Dezelfde strategie werkte in andere systemen, waaronder mitochondriën en microtubuli, en zelfs bij eiwitten met diffuusere, amorfe verdelingen waarbij ruimtelijke patronen op zichzelf geen aanwijzing geven over wat echt is.
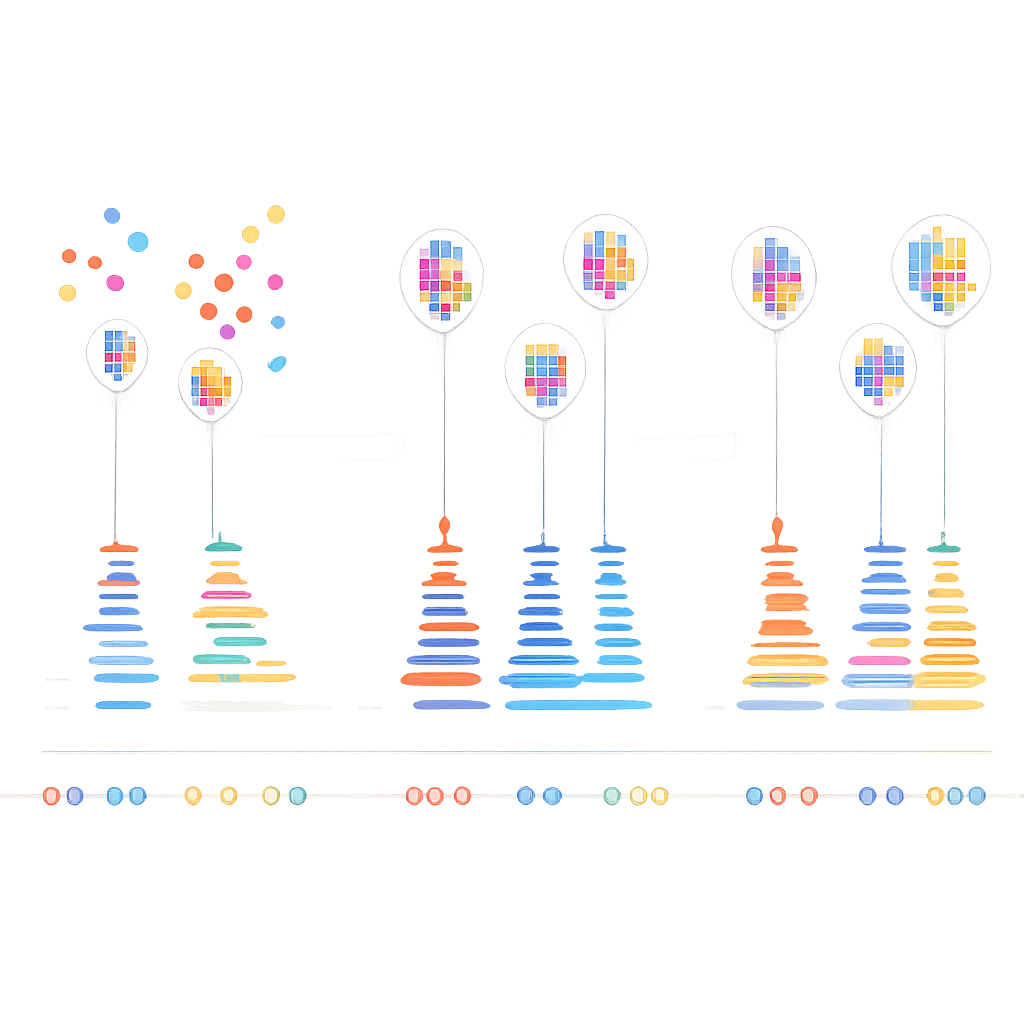
Helderdere moleculaire kaarten voor toekomstige studies
Door te luisteren naar het “ritme” van DNA-binding in plaats van alleen te kijken waar knipperingen voorkomen, haalt deze methode betrouwbaar misleidende achtergrond uit DNA-PAINT-gegevens. Voor niet-specialisten is de belangrijkste uitkomst eenvoudig: scherpere, betrouwbaardere moleculaire kaarten binnen cellen. Dit maakt het veiliger om te tellen hoeveel proteïnemoleculen aanwezig zijn, om te beoordelen hoe dicht verschillende eiwitten naast elkaar zitten, en om nauwkeurigere afbeeldingen van het innerlijk van cellen te construeren. Naarmate DNA-gebaseerde beeldvorming blijft groeien, zal dit soort slimme ontruising essentieel zijn om ruwe gespikkelde beelden om te zetten in solide biologische inzichten.
Bronvermelding: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Trefwoorden: DNA-PAINT, superresolutiemicroscopie, beeldontruising, single-molecule imaging, eiwitmapping