Clear Sky Science · nl
Uitlegbare AI-analyse van menselijke alvleeskliersecties identificeert kenmerken van type 2-diabetes
Waarom dit onderzoek belangrijk is voor alledaagse gezondheid
Type 2-diabetes treft honderden miljoenen mensen, maar artsen hebben nog steeds moeite om duidelijke, fysieke aanwijzingen van de ziekte in de alvleesklier te zien — het orgaan dat insuline maakt. Deze studie gebruikt krachtige kunstmatige intelligentie, gecombineerd met geavanceerde microscopie, om subtiele patronen in menselijk alvleesklierweefsel te lezen die onzichtbaar zijn voor het blote oog. Daardoor komen nieuwe structurele kenmerken aan het licht die verbonden zijn met type 2-diabetes en ontstaan nieuwe ideeën voor diagnose, preventie en behandeling.
De alvleesklier in ongekende detail bekijken
Traditioneel hebben wetenschappers alvleesklierweefsel van overleden donoren onderzocht op veranderingen die met type 2-diabetes geassocieerd zijn, zoals littekenvorming, vetafzettingen of verlies van insulineproducerende cellen. Deze studies hebben een lange lijst van mogelijke afwijkingen opgeleverd, maar geen enkele was betrouwbaar genoeg om een patholoog op basis van een preparaat met zekerheid te laten vaststellen of iemand diabetes had. In dit werk stelden de onderzoekers een unieke verzameling ultra-hoge-resolutiebeelden samen van alvleeskliermonsters die tijdens operaties van 100 levende donoren werden genomen, 35 met type 2-diabetes en 65 zonder. Elk monster werd op meerdere manieren gekleurd om verschillende celtypen te benadrukken: hormoonproducerende cellen in de eilandjes, bloedvaten, vetcellen en zenuwvezels. Deze rijke visuele dataset, veel te complex om volledig door een mens te verwerken, is precies het terrein waarin kunstmatige intelligentie uitblinkt. 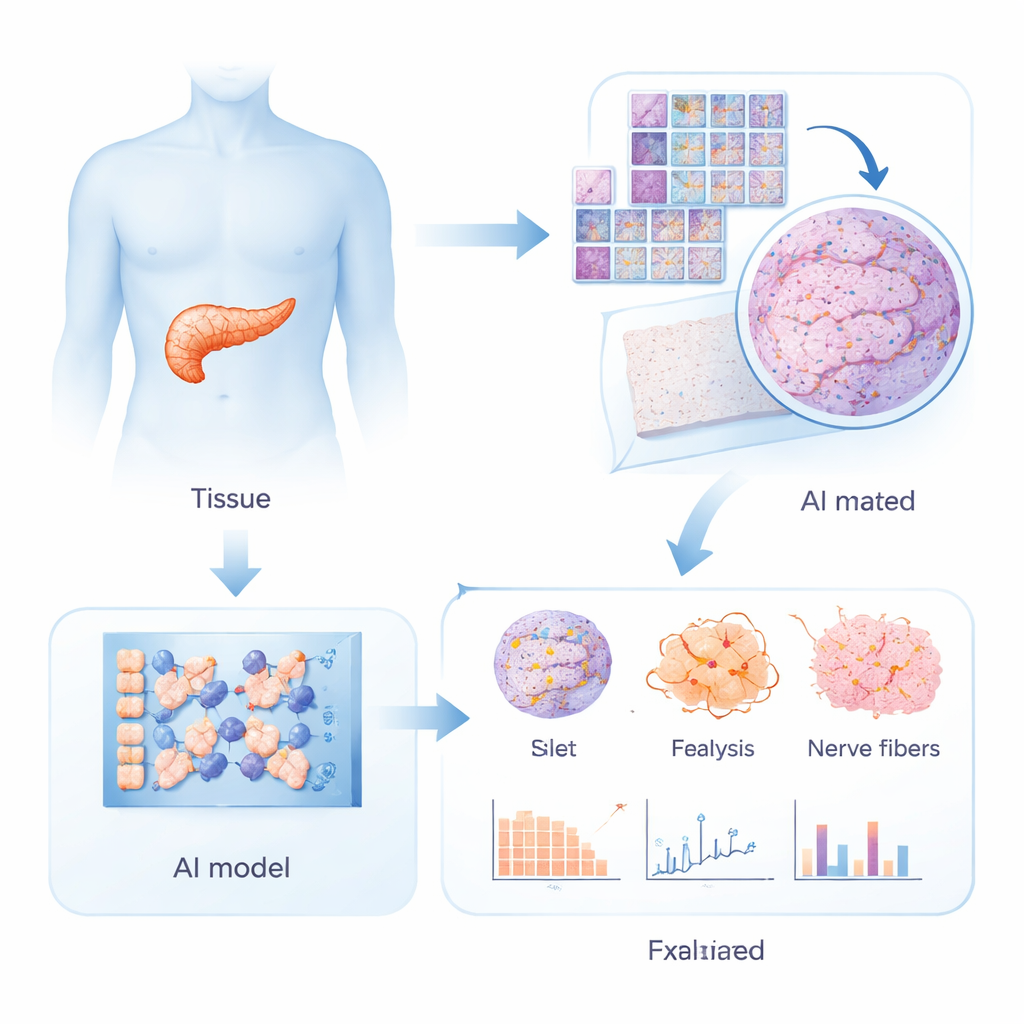
AI trainen om de diabetische alvleesklier te herkennen
Het team trainde deep-learningmodellen om weefsel van mensen met en zonder type 2-diabetes te onderscheiden. Omdat elke hele-slide afbeelding miljarden pixels bevat, deelden ze de platen eerst op in vele kleine patches. Een voorgetrainde vision transformer extraheerde kenmerken uit elk patch, en een gespecialiseerde "multiple instance learning"-classifier combineerde vervolgens informatie over alle patches van een slide om te beslissen of die van een donor met of zonder diabetes kwam. Om overfitting te voorkomen gebruikten ze herhaalde cross-validatie en gemiddeldes van de voorspellingen van 15 afzonderlijke modellen. De beste prestaties werden behaald met multiplex fluorescentiebeelden die gelijktijdig alfa‑cellen, delta‑cellen en zenuwvezels markeerden, met een area-under-the-curve van 0,956 — sterk bewijs dat de AI betrouwbaar diabetesgerelateerde patronen kon "zien" die pathologen nog niet hadden kunnen formaliseren.
De zwarte doos zichzelf laten uitleggen
Voorspelling alleen was echter niet het doel; de auteurs wilden biologische inzichten. Daarom pasten ze uitlegbare-AI-technieken toe die laten zien welke regio's en pixels het model gebruikte bij zijn beslissingen. Attention-kaarten benadrukten de meest invloedrijke gebieden over hele slides, terwijl attributiemethoden tot op het niveau van individuele cellen en structuren inzoomden. Om deze kleurrijke warmtekarten in cijfers om te zetten, trainde het team aparte segmentatienetwerken die automatisch eilandjes, vetcelclusters en bindweefsel (fibrotisch weefsel) konden omlijnen. Vervolgens kwantificeerden ze kenmerken zoals eilandgrootte, totale vetoppervlakte, aantal vetclusters, afstand tussen eilandjes en nabijgelegen vet, en de omvang van fibrotisch weefsel, en analyseerden hoe deze "histologische biomerkers" verband hielden met diabetesstatus en insulinesecretie, rekening houdend met leeftijd, geslacht, BMI en andere klinische factoren. 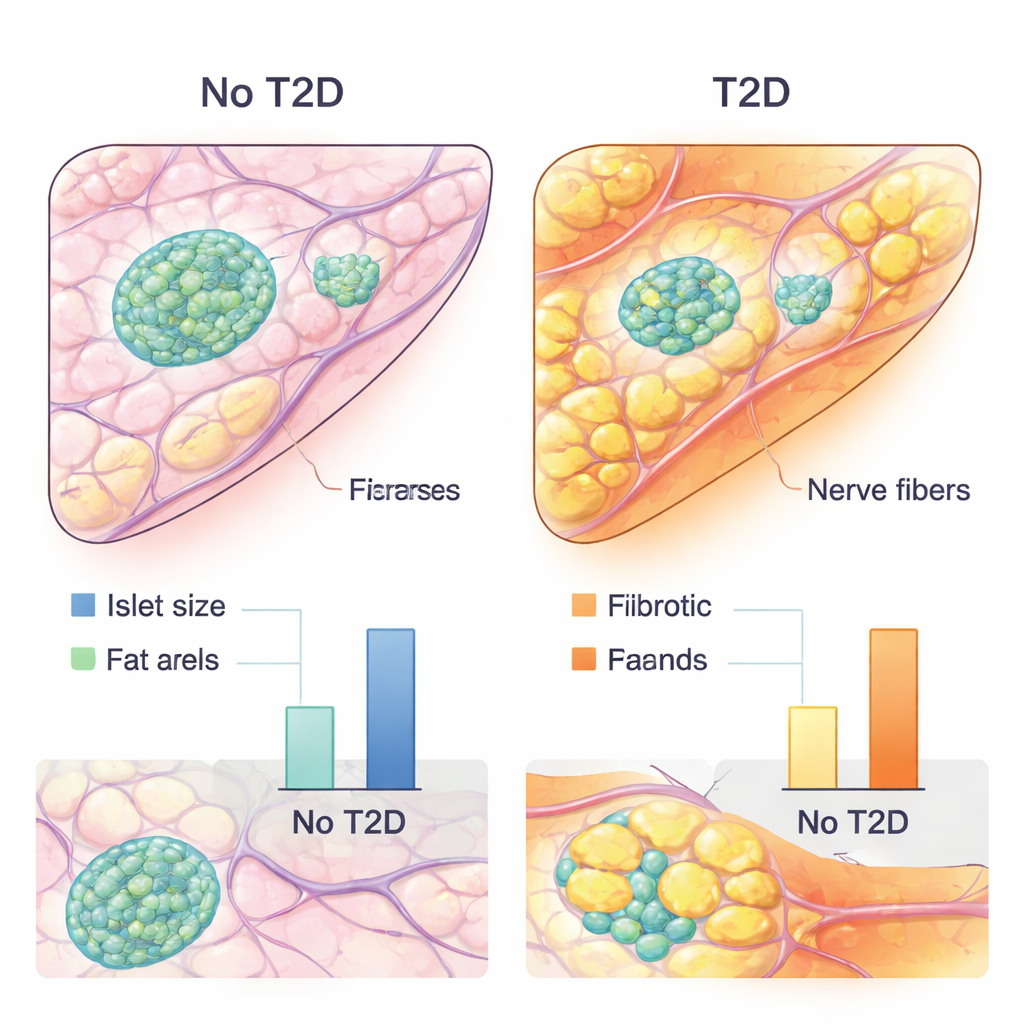
Nieuwe aanwijzingen: vet, zenuwen, littekens en krimpende eilandjes
De AI-gebaseerde analyse onthulde meerdere consistente kenmerken van de diabetische alvleesklier. Mensen met type 2-diabetes hadden geneigd kleinere eilandjes en grotere clusters vetcellen binnen de alvleesklier te hebben. Belangrijk is dat eilandjes bij diabetische donoren dichter bij deze vetafzettingen lagen, wat wijst op een directere lokale invloed van vetweefsel op hormoonproducerende cellen. De hoeveelheid bindweefsel, littekenachtig van aard, was ook hoger bij diabetes en hing samen met slechtere insulineafgifte. Tegelijkertijd gaven de AI-modellen verrassend veel gewicht aan structuren die voor tubuline beta 3 waren gekleurd, een merker voor zenuwvezels, vooral wanneer deze vezels door of nabij eilandjes liepen. Dit wijst op veranderingen in de innervatie van de alvleesklier — hoe zenuwen contact maken met eilandcellen — als een mogelijk belangrijke en ondergewaardeerde bijdrage aan type 2-diabetes. Samen suggereren deze bevindingen dat niet alleen de bètacellen zelf van belang zijn, maar ook hun omgeving: nabijgelegen vetcellen, littekenvorming, bloedvaten en zenuwen lijken allemaal de gezondheid van de eilandjes te beïnvloeden.
Wat dit betekent voor toekomstige zorg
Voor niet-specialisten is de kernboodschap dat type 2-diabetes een subtiele maar detecteerbare afdruk in de architectuur van de alvleesklier achterlaat. Door hoge-resolutiebeelden te combineren met uitlegbare AI, vertaalt deze studie die patronen naar meetbare kenmerken — zoals eilandgrootte, vetverdeling, aanwezigheid van zenuwen en fibrose — die correleren met diabetes en met hoe goed het lichaam nog insuline kan produceren. Hoewel deze benadering nog geen routine-diagnostisch hulpmiddel is, biedt ze een krachtig stappenplan voor het ontdekken van nieuwe medicijntargets en het verfijnen van ons begrip van hoe diabetes ontstaat. Op de lange termijn kunnen inzichten uit dergelijke AI-gestuurde weefselanalyses artsen helpen beter te voorspellen wie risico loopt, de ziekteprogressie te monitoren en therapieën te ontwerpen die niet alleen bètacellen beschermen, maar ook de omliggende alvleesklieromgeving.
Bronvermelding: Klein, L., Ziegler, S., Gerst, F. et al. Explainable AI-based analysis of human pancreas sections identifies traits of type 2 diabetes. Nat Commun 17, 1558 (2026). https://doi.org/10.1038/s41467-026-69295-2
Trefwoorden: type 2 diabetes, alvleesklier, kunstmatige intelligentie, histopathologie, biomerkers