Clear Sky Science · nl
Adgrg6/Gpr126 is vereist voor de integriteit van de compacte wand en het vaststellen van trabeculaire identiteit tijdens cardiale trabeculatie
Waarom de architectuur van de hartwand ertoe doet
Elke hartslag berust op een nauwkeurig gevormde binnenwand van het hart. Bij zich ontwikkelende embryo’s vormt deze wand zich eerst als een gladde laag en groeit vervolgens uit tot een netwerk van spierige richels, de trabeculae, die het hart helpen efficiënt te pompen. Als dit proces misgaat, kunnen kinderen en volwassenen ernstige cardiomyopathieën ontwikkelen. Deze studie onderzoekt hoe een weinig bekend receptor, Gpr126, hartcellen helpt beslissen of ze in de gladde buitenwand blijven of deel gaan uitmaken van die binnenste richels.
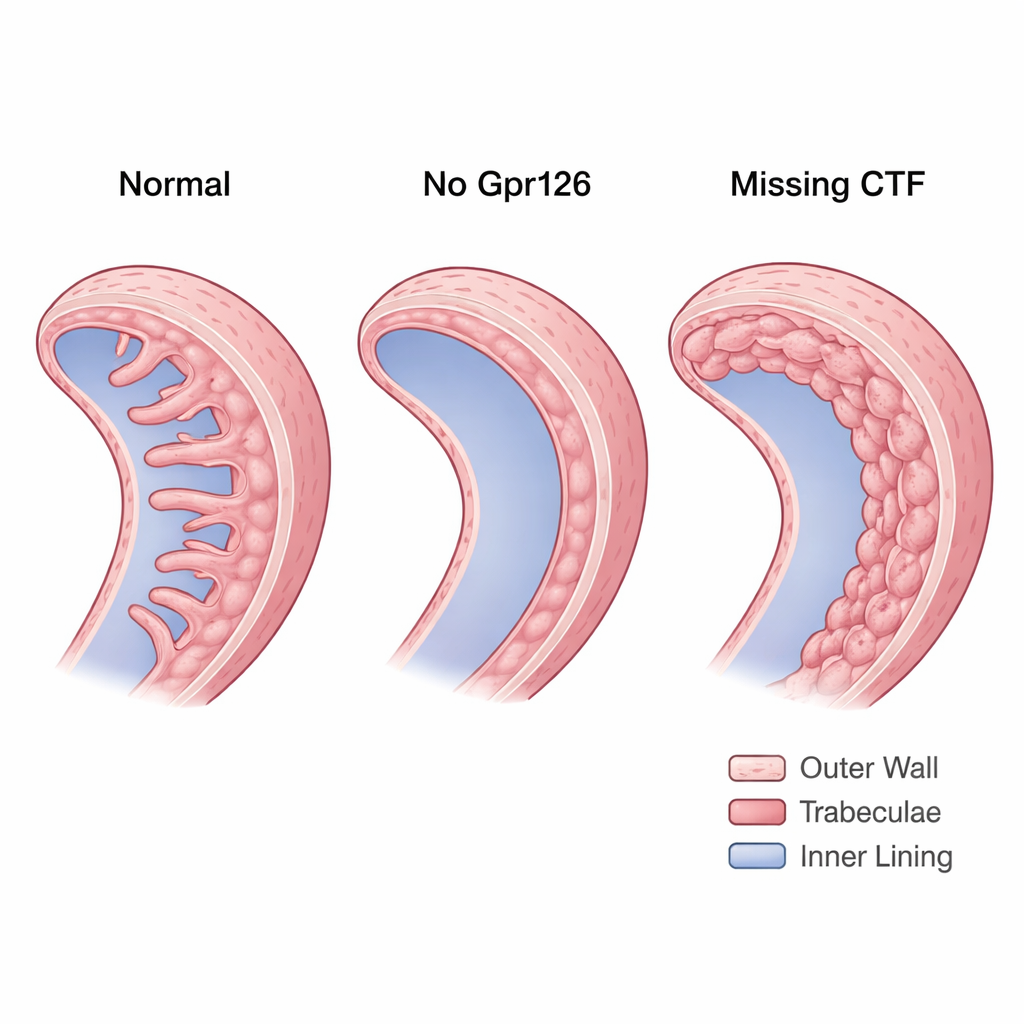
Een receptor met gesplitste functies in het hart
Gpr126 behoort tot een familie van adhesion G-eiwitgekoppelde receptoren die in het celmembraan zitten en de omgeving van de cel waarnemen. Deze receptoren zijn bijzonder interessant omdat veel bestaande geneesmiddelen al verwante receptoren targeten, wat ze aantrekkelijke therapeutische kandidaten maakt. Gpr126 is ongebruikelijk omdat het van nature in twee hoofdonderdelen wordt gesplitst: een N-terminaal fragment (NTF) dat uit de cel steekt en kan helpen bij cel–celadhesie, en een C-terminaal fragment (CTF) dat het membraan overspant en intracellulaire signalering activeert. Eerder werk koppelde Gpr126 aan hartontwikkeling, maar het was onduidelijk wat elk fragment precies doet tijdens de vorming van trabeculae.
Zebravissen gebruiken om het hart te zien vormen
De onderzoekers gebruikten zebravissen, waarvan de transparante embryo’s realtime beeldvorming van het kloppende hart mogelijk maken. Ze bestudeerden twee genetische varianten van gpr126. De ene (stl47) produceert alleen een heel klein, sterk ingekort eiwit; de andere (st49) maakt een stabiel, uitgescheiden NTF-fragment dat het CTF-signaandeel mist. Door deze mutanten te combineren met fluorescerende rapporterlijnen kon het team individuele hartcellen zien, de vorming van trabeculae volgen en belangrijke moleculen monitoren zoals N-cadherine (dat helpt cellen aan elkaar te laten plakken) en Notch (een signaleringspad dat cellen vertelt welke identiteit ze moeten aannemen).
De wand bij elkaar houden versus de richels vormen
De stl47-mutanten, die in wezen beide functionele fragmenten missen, toonden aan dat Gpr126 nodig is om normale trabeculae te vormen. In maternale-zygotische stl47-embryo’s—waar geen gezond Gpr126 van een van beide ouders aanwezig is—ontwikkelden veel harten met ontbrekende of sterk gereduceerde trabeculae. N-cadherine, dat in gezonde harten keurig geconcentreerd zit aan de zijkanten van compacte-wand cardiomyocyten, leek verspreid over het celoppervlak te liggen. Deze desorganisatie suggereerde dat zonder het NTF de cel–celadhesie in de compacte wand instabiel wordt, waardoor de fundering waarop trabeculae zouden moeten bouwen ondermijnd raakt.
Te veel wand, te weinig identiteit
De st49-mutanten, die nog wel het NTF maken maar het CTF missen, toonden het omgekeerde probleem. In plaats van ontbrekende trabeculae vormden hun harten een dikke, meerlagige binnenwand. De extra lagen waren geen echte trabeculae: de cellen bleven gepolariseerd zoals compacte-wandcellen en slaagden er niet in hun N-cadherine-contacten om te vormen tot het puntpatroon dat kenmerkend is voor richels-vormende cellen. Met een Notch-activiteitsreporter vond het team dat deze harten abnormaal hoge Notch-signalisatie in het myocard hadden. Hoge Notch is bekend om cellen in de compacte wand te houden en te voorkomen dat ze delamineren naar trabeculae. Belangrijk is dat wanneer de onderzoekers alleen het CTF opnieuw in endocardiale cellen introduceerden, trabeculae herstelden en de Notch-activiteit weer naar normalere waarden daalde, wat aantoont dat CTF-signaleringsfunctie cruciaal is om cardiomyocyten een trabeculaire identiteit te geven.
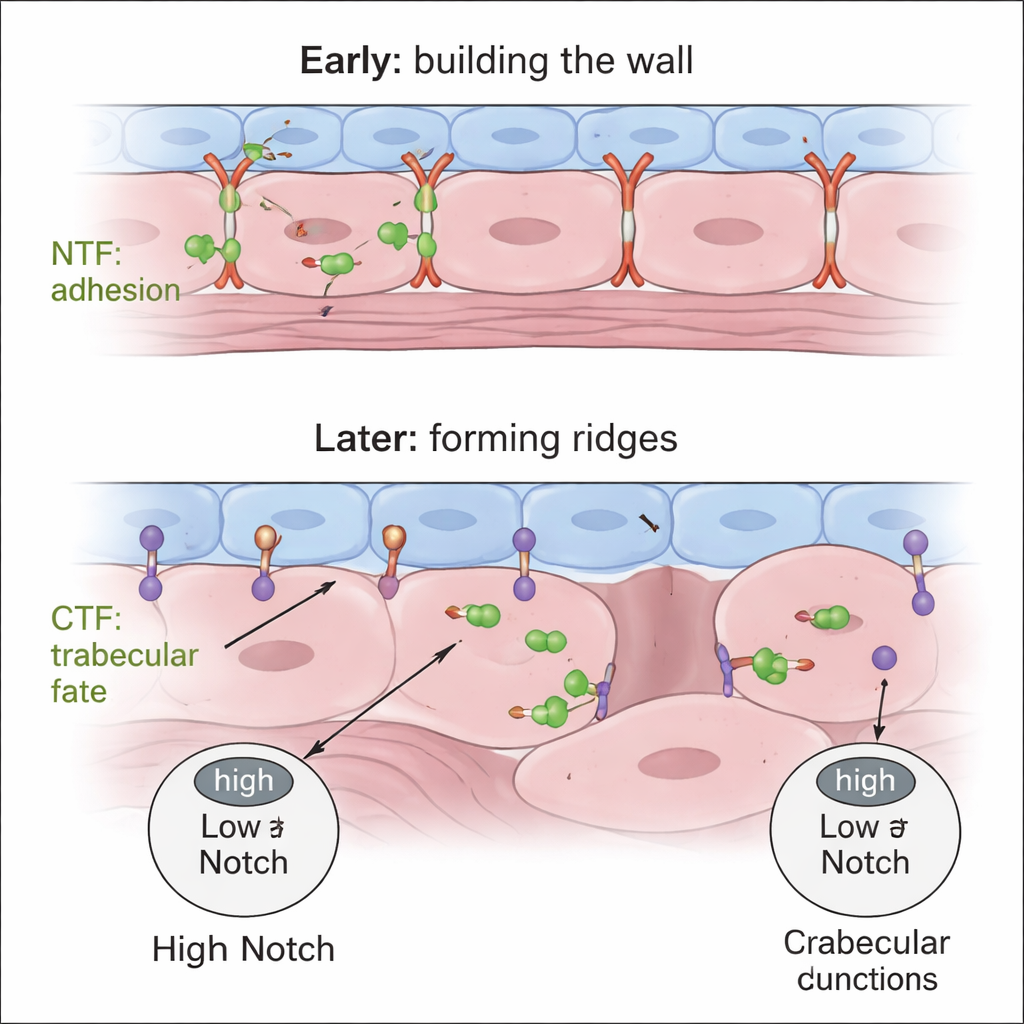
Signalen in balans voor een gezond hart
Gezamenlijk ondersteunen de bevindingen een tweestaps- en tweedelig model. Eerst helpt het uitgescheiden NTF van Gpr126 compacte-wand cardiomyocyten hun nauwe, correct gepositioneerde juncties te behouden, wat een stevige eendelige wand garandeert. Later reguleert het CTF—werkend vanuit endocardiale cellen—de myocardiale Notch-signalisatie zodat slechts sommige cardiomyocyten depolariseren, hun juncties versoepelen en naar binnen uitsteken om trabeculae te vormen, terwijl hun buren in de compacte wand blijven. Als het NTF ontbreekt, organiseert de wand zich nooit goed; als het CTF ontbreekt, groeit de wand te veel en slagen cellen er niet in een trabeculaire identiteit aan te nemen. Deze domeinspecifieke controle van de architectuur van de hartwand benadrukt Gpr126 als een potentiële schakel tussen celadhesie, signaleringspaden zoals Notch, en structurele hartziekten, en suggereert dat het afstemmen van verschillende delen van dezelfde receptor op termijn ontwikkelingsafwijkingen zou kunnen corrigeren.
Bronvermelding: Srivastava, S., Gunawan, F., Vergarajauregui, S. et al. Adgrg6/Gpr126 is required for compact wall integrity and establishing trabecular identity during cardiac trabeculation. Nat Commun 17, 1484 (2026). https://doi.org/10.1038/s41467-026-69292-5
Trefwoorden: cardiale trabeculatie, Gpr126, hartontwikkeling, Notch-signaleringspad, zebravis-model