Clear Sky Science · nl
De genetische drijver van acute necrotiserende encefalopathie, RANBP2, reguleert de ontstekingsreactie op infectie met influenzavirus A
Wanneer de griep de hersenen schaadt
De meeste mensen denken bij influenza aan een week met koorts, hoest en bedrust. Toch kan in zeldzame gevallen, vooral bij kinderen, een routinematige griepinfectie plotseling uitmonden in een levensbedreigende hersenaandoening genaamd acute necrotiserende encefalopathie (ANE). Families en artsen vermoeden al lang dat genen mede bepalend zijn voor wie deze catastrofale complicatie ontwikkelt. Deze studie onthult hoe een enkel cellulair poortwachterseiwit, RANBP2, normaal gesproken het griepvirus in toom houdt en voorkomt dat de eigen ontstekingsreactie van het lichaam ontspoort.
Een zeldzame maar verwoestende griepcomplicatie
ANE treedt abrupt op na een koortsende ziekte, vaak influenza, en kan snel leiden tot aanvallen, coma en blijvende neurologische schade. Ongeveer de helft van de bekende ANE‑episodes wereldwijd is gekoppeld aan influenzavirus A, met name het H1N1‑stam. Kinderen die bepaalde veranderingen in het RANBP2‑gen erven lopen veel meer risico; deze aandoening staat bekend als ANE1. Tot nu toe begrepen wetenschappers echter niet wat dit eiwit precies doet tijdens een griepinfectie, of waarom een wijziging ervan de ontsteking in de hersenen zo ernstig zou maken.
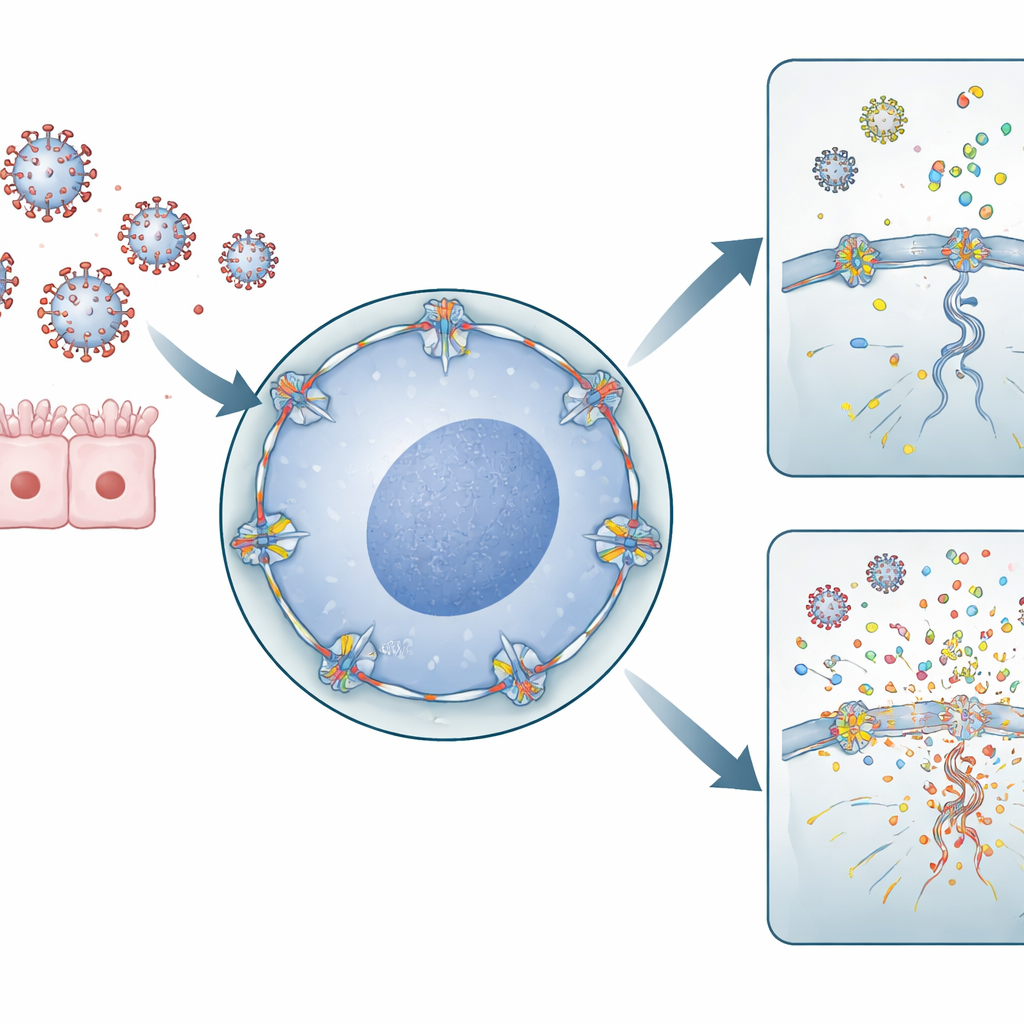
Cellulaire poorten en virale genomen
Influenzavirus A heeft een ongewoon levenspatroon voor een RNA‑virus: het moet de kern van de cel binnengaan om zijn genetisch materiaal te kopiëren. Hiervoor passeert het de nucleaire poriën—grote doorgangen in de kernmembraan die het verkeer tussen de kern en het omringende cytoplasma reguleren. RANBP2 is een belangrijk onderdeel aan de buitenzijde van deze poriën. De auteurs gebruikten menselijk, uit long afkomstig cellijnmateriaal en immuuncellen om RANBP2‑niveaus te verlagen of de ANE‑geassocieerde mutatie in te brengen. Zij ontdekten dat wanneer RANBP2 ontbrak of verkeerd gepositioneerd was, griepgemonen sterker werden gekopieerd in de kern en dat virale genetische segmenten op een onevenwichtige manier naar het cytoplasma werden geëxporteerd. Vreemd genoeg resulteerde deze overvloed aan viraal RNA niet in meer infectieuze deeltjes, maar veranderde het wel waar en hoe viraal materiaal zich in de cel ophoopte.
Wanneer viraal puin het alarmsysteem voedt
Het immuunsysteem vertrouwt op moleculaire sensoren die losse stukjes viraal RNA in het cytoplasma detecteren als gevaarseinen. Het team toonde aan dat in cellen zonder normaal RANBP2 extra virale RNA‑segmenten ophoopten in het cytoplasma, precies de patronen waarop deze sensoren zijn afgestemd. In uit longafkomstige cellen leidde dit tot hogere niveaus van ontstekingsmoleculen zoals IL‑6 en IL‑1β. In primaire humane macrofagen—eerste verdedigingslinie‑immuuncellen afkomstig van bloeddonoren—leidde verlies van RANBP2 tot een opvallende stijging van pro‑inflammatoire chemokinen, waaronder CXCL8, CXCL10, CCL2, CCL3 en CCL4. Deze chemische boodschappers rekruteren en activeren extra immuuncellen en versterken zo de algehele reactie op de infectie.
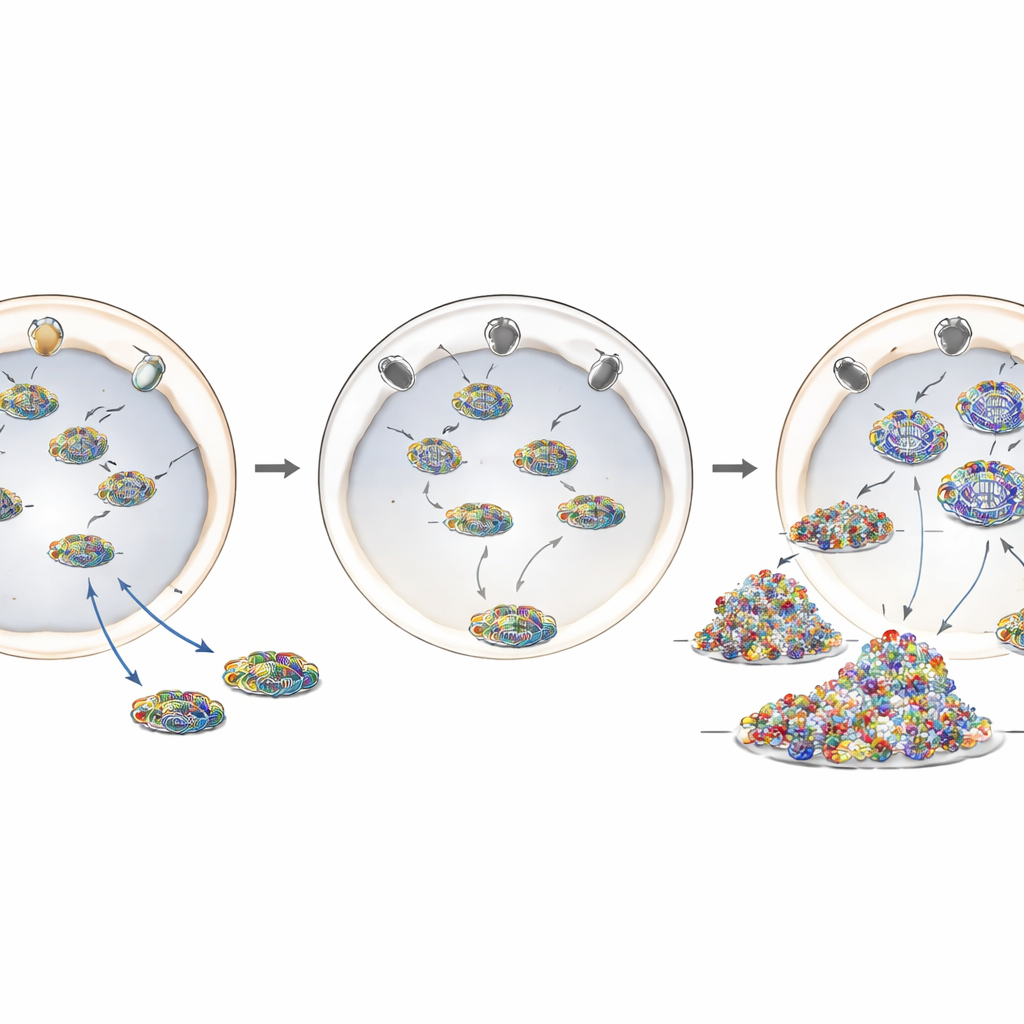
Een ziekte‑mutatie die een beschermer verplaatst
Om ANE1 nauwer te modelleren gebruikten de onderzoekers CRISPR‑Cas9 genbewerking om de meest voorkomende ziektegerelateerde verandering, T585M, in het menselijk RANBP2‑gen in te brengen. In deze gewijzigde cellen waren de RANBP2‑eiwitniveaus grotendeels normaal, maar de lokalisatie was dat niet: in plaats van een heldere rand rond de kernmembraan vormde veel van het eiwit zich in het binnenste van de cel. Cellen met deze mutatie, hetzij op één of beide genkopieën, gedroegen zich sterk zoals RANBP2‑uitgeputte cellen. Ze ondersteunden verhoogde replicatie van het influenzagenoom, toonden meer viraal materiaal in het cytoplasma en vertoonden na infectie een sterkere ontstekingsreactie. Dit suggereert dat het correct positioneren van RANBP2 bij nucleaire poriën—en niet zozeer de totale hoeveelheid—cruciaal is voor zijn beschermende rol.
Waarom dit belangrijk is voor kinderen met risico
Samengevat schetsen de bevindingen RANBP2 als een cellulaire beschermer die fijn afstelt hoe influenzagenetisch materiaal de kern in en uit beweegt. Wanneer RANBP2 afwezig of verkeerd geplaatst is, wordt viraal RNA overgerepliceerd en chaotisch geëxporteerd, waardoor het cytoplasma volraakt met moleculair puin dat de immuunsignalisatie sterk versterkt. Voor de meeste weefsels kan dit een zwaardere maar nog steeds te overleven griepinfectie betekenen. Bij kwetsbare kinderen met ANE1 kan zulke ongeremde ontsteking—vooral als deze de hersenen bereikt—helpen verklaren waarom na ogenschijnlijk gewone infecties plotseling ernstige neurologische schade optreedt. Inzicht in deze route kan toekomstige strategieën sturen om risicopatiënten vroeg te identificeren en ontstekingsremmende behandelingen af te stemmen voordat de immuunreactie van beschermend naar destructief omslaat.
Bronvermelding: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Trefwoorden: influenza, acute necrotiserende encefalopathie, RANBP2, hyperinflammatie, nucleair pore