Clear Sky Science · nl
MHC-klasse II functioneert als gastheerspecifieke toegangsreceptor voor representatieve humane en varkens H3N2-influenza A-virussen
Waarom deze griepstudie ertoe doet
Seizoensgriep voelt vertrouwd, maar het virus dat het veroorzaakt zoekt voortdurend naar nieuwe manieren om onze cellen binnen te dringen en tussen soorten over te springen. Deze studie laat zien dat een veelvoorkomende griepstam, H3N2, niet alleen de klassieke toegangspoort naar cellen kan gebruiken, maar ook een tweede, onverwachte route die verschilt tussen mensen en varkens. Inzicht in deze alternatieve instaproute helpt verklaren hoe griep zich aan nieuwe gastheren aanpast en kan verbeteren hoe we stammen met pandemisch potentieel opsporen en ons erop voorbereiden. 
De gebruikelijke manier waarop griep binnenkomt
Decennialang wisten wetenschappers dat influenza A-virussen gewoonlijk cellen binnendringen door zich te hechten aan suikermoleculen genaamd siaalzuren die het celoppervlak sieren. De virale "grijphaak", een eiwit genaamd hemagglutinine, herkent specifieke vormen en verbindingen van deze suikers, die verschillen tussen vogels, mensen en andere dieren. Kleine veranderingen in hemagglutinine kunnen de suikerpreferentie verschuiven en zo een vogelvirus helpen zich aan te passen aan zoogdieren. Onlangs werden echter ongebruikelijke vleermuis- en eendgriepvirussen gevonden die siaalzuren helemaal negeren en in plaats daarvan een eiwit gebruiken dat MHC klasse II heet als toegangspoort, wat erop wijst dat ons beeld van griepeingang onvolledig was.
Er verschijnt een tweede deur
Het nieuwe werk toont aan dat meer vertrouwde H3N2-virussen ook MHC klasse II kunnen gebruiken als alternatieve instaproute, naast siaalzuren. MHC klasse II helpt normaal gesproken immuuncellen fragmenten van ziekteverwekkers te presenteren om het immuunsysteem te waarschuwen. Het team concentreerde zich op twee nauw verwante virussen op hetzelfde genetische fundament: één die lijkt op een menselijke seizoens-H3N2-stam (hVIC/11) en een andere aangepast aan varkens (sOH/04). In varkenslongen bleek het varkens-geadapteerde virus nauw geassocieerd met cellen rijk aan varkens MHC klasse II, met name alveolaire macrofagen—vooraanstaande immuuncellen in de longblaasjes—wat suggereert dat dit molecuul als een handvat kan dienen waar het virus zich aan vastgrijpt.
Een deur uitschakelen om de andere te testen
Om te testen of MHC klasse II echt als een onafhankelijke toegangsreceptor fungeert, verwijderden de onderzoekers chemisch de siaalzuren van varkensmacrofagen en van geconstrueerde menselijke cellijnen. Toen alleen de klassieke suikers werden verwijderd, slaagden beide virussen er nog steeds in enige infectie te veroorzaken. Maar toen de siaalzuren werden verwijderd en MHC klasse II gelijktijdig met antilichamen werd geblokkeerd, daalde de infectie scherp, vooral voor het varkens-geadapteerde virus. In menselijke nier- en longcellen die genetisch waren verhinderd om enige siaalzuur te produceren, maakte het toevoegen van de menselijke versie van MHC klasse II efficiënte infectie door het mensachtige virus mogelijk, terwijl het toevoegen van de varkensversie het varkensvirus bevoordeelde. Het behandelen van cellen met medicijnen die de verzuring van interne compartimenten blokkeren, verhinderde ook deze MHC-gedreven infectie, wat aangeeft dat eenmaal binnen het virus dezelfde interne route volgt als bij de standaardgrieptoegang. 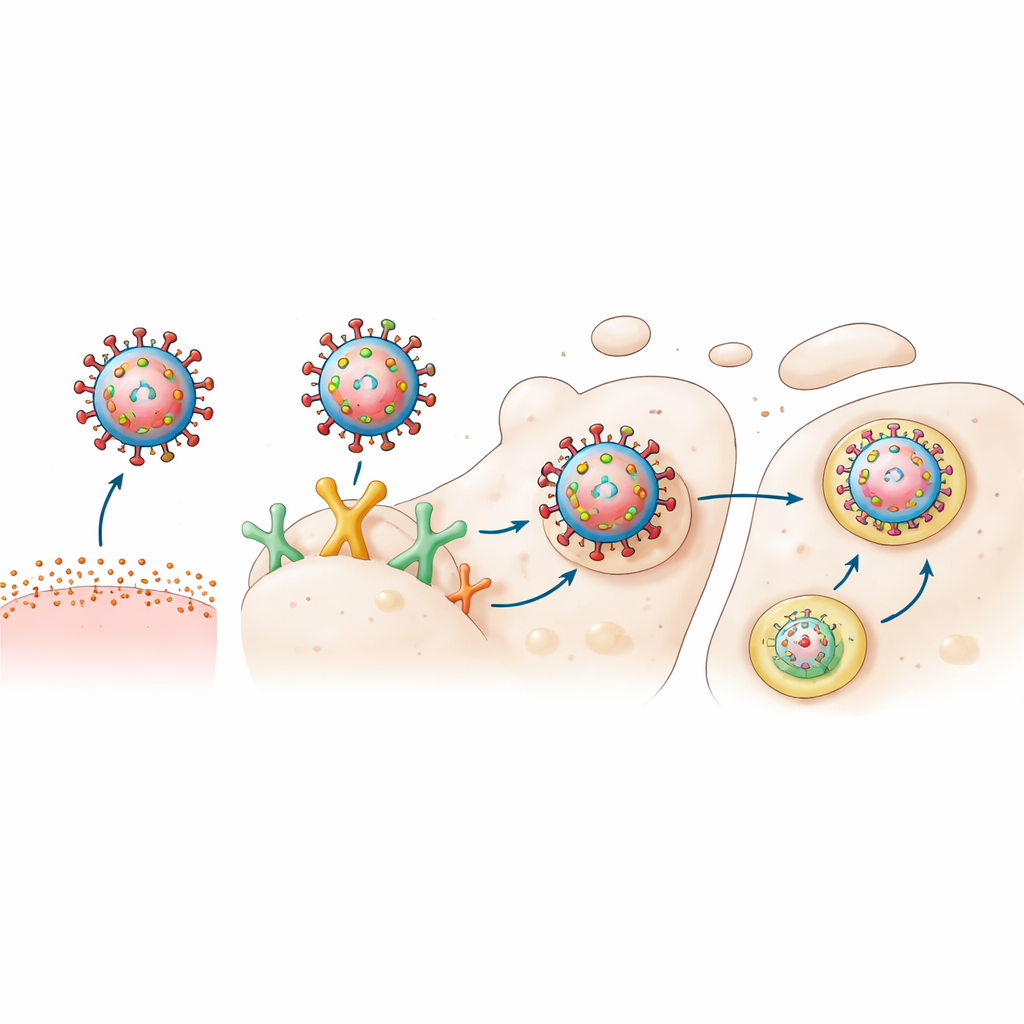
Hoe kleine veranderingen het virus helpen van gastheer te wisselen
De auteurs vroegen zich vervolgens af welke delen van het virale hemagglutinine deze nieuwe bindingswijze controleren. Eerder werk had laten zien dat wanneer een humaan H3N2-virus door varkens gaat, het vaak bepaalde één-lettermutaties nabij, maar niet direct in, het siaalzuurbindende zakje oppikt. Virussen met een van drie zulke veranderingen (op posities aangeduid als 138, 186 of 193 in het eiwit) werden getest. Deze gemuteerde virussen konden zowel menselijke als varkens MHC klasse II gebruiken om binnen te dringen in cellen die geen siaalzuur hadden, en in sommige proeven gaven ze zelfs de voorkeur aan de varkensvariant. Tegelijkertijd veranderden dezezelfde mutaties hoe sterk de virussen zich binden aan mens- of vogelachtige siaalzuren. Met andere woorden, aanpassingen nabij de gebruikelijke suikerbindingsplek kunnen zowel de klassieke als de nieuwe receptor tegelijk afstemmen, waardoor het virus flexibiliteit krijgt tijdens de aanpassing aan een nieuwe soort.
Wat dit betekent voor griep en toekomstige bedreigingen
Samengevat laten de bevindingen zien dat gewone H3N2-griepvirussen niet beperkt zijn tot één soort celoppervlaktehandvat: ze kunnen zowel siaalzuren als MHC klasse II gebruiken, en ze doen dat op een manier die weerspiegelt of het virus beter geschikt is voor mensen of varkens. Tijdens vroege aanpassing aan een nieuwe gastheer kan een virus tijdelijk MHC klasse II van beide soorten aanspreken, waardoor het doelbereik wordt vergroot en het helpt zich te vestigen. Omdat MHC klasse II overvloedig aanwezig is op belangrijke immuuncellen in de long, kan deze alternatieve route het virus in staat stellen cellen aan te vallen die ons zouden moeten verdedigen, wat mogelijk bijdraagt aan verspreiding en ziekte. Het herkennen van MHC klasse II als een gastheerspecifieke toegangsreceptor voegt een belangrijk stuk toe aan de puzzel van hoe griep soortenbarrières overschrijdt en benadrukt de noodzaak om niet alleen suikergbinding maar ook eiwitreceptoren te monitoren bij het beoordelen van het pandemische risico van opkomende stammen.
Bronvermelding: Cardenas, M., Compton, S., Caceres, C.J. et al. MHC class II functions as a host-specific entry receptor for representative human and swine H3N2 influenza A viruses. Nat Commun 17, 2560 (2026). https://doi.org/10.1038/s41467-026-69267-6
Trefwoorden: influenza A H3N2, virusingangsreceptoren, MHC klasse II, gashostadaptatie, zoönotische transmissie