Clear Sky Science · nl
Trifunctioneel flavo‑enzym-geëngineerde asymmetrische assemblage van 4‑alkyl‑butenoliden in de biosynthese van avenolide
Waarom kleine ringen in bacteriën voor ons van belang zijn
Veel levensreddende geneesmiddelen, van parasietdodende middelen tot gewasbeschermers, zijn afhankelijk van een klein chemisch motief dat een butenolide wordt genoemd. Tegenwoordig worden deze ringen grotendeels gemaakt uit op olie gebaseerde uitgangsstoffen via meerstaps industriële processen die energie verbruiken en afval produceren. Deze studie onthult hoe bodembacteriën zo’n ring opbouwen — een hormoon genaamd avenolide dat de productie van de zeer succesvolle antiparasitaire middelen avermectines aanzet. Inzicht in deze natuurlijke route wijst op schonere, goedkopere manieren om nuttige chemicaliën te maken en kan helpen nieuwe antibiotica te ontsluiten.
De bijzondere ring in het hart van veel geneesmiddelen
Butenoliden zijn compacte, vijf‑ledige ringen waar chemici dol op zijn omdat ze op veel verschillende manieren reageren en voorkomen in veel natuurlijke producten en moderne geneesmiddelen. Ze helpen moleculen vormen met antikanker-, schimmelwerende, ontstekingsremmende en insecticide activiteiten die in geneeskunde en landbouw worden gebruikt. Traditionele syntheseroutes naar deze ringen vereisen doorgaans meerdere zorgvuldig gecontroleerde stappen, dure katalysatoren en petrochemische grondstoffen. Die combinatie drijft kosten en milieubelasting omhoog, waardoor onderzoekers op zoek gaan naar biologische kortere routes die de natuur al heeft geperfectioneerd.
Een bacterieel hormoon dat een blockbuster geneesmiddel activeert
In de bodem-bacterie Streptomyces avermitilis fungeert het butenolide‑houdende molecuul avenolide als een klein hormoon. Bij extreem lage concentraties bindt het aan een regulerend eiwit en heft het een moleculaire rem op de genen die avermectines produceren, krachtige stoffen die parasitaire wormen en sommige insecten verlammen. Eerder genetisch werk suggereerde dat twee enzymen, SavA en SavB, avenolide opbouwen, maar de exacte stappen waren onbekend. Het team bracht eerst de relevante genen over in een beter meewerkende verwant, Streptomyces albidoflavus, en optimaliseerde de kweekcondities totdat de gemodificeerde stam milligramhoeveelheden zuiver avenolide produceerde — genoeg om de route in detail te ontleden. 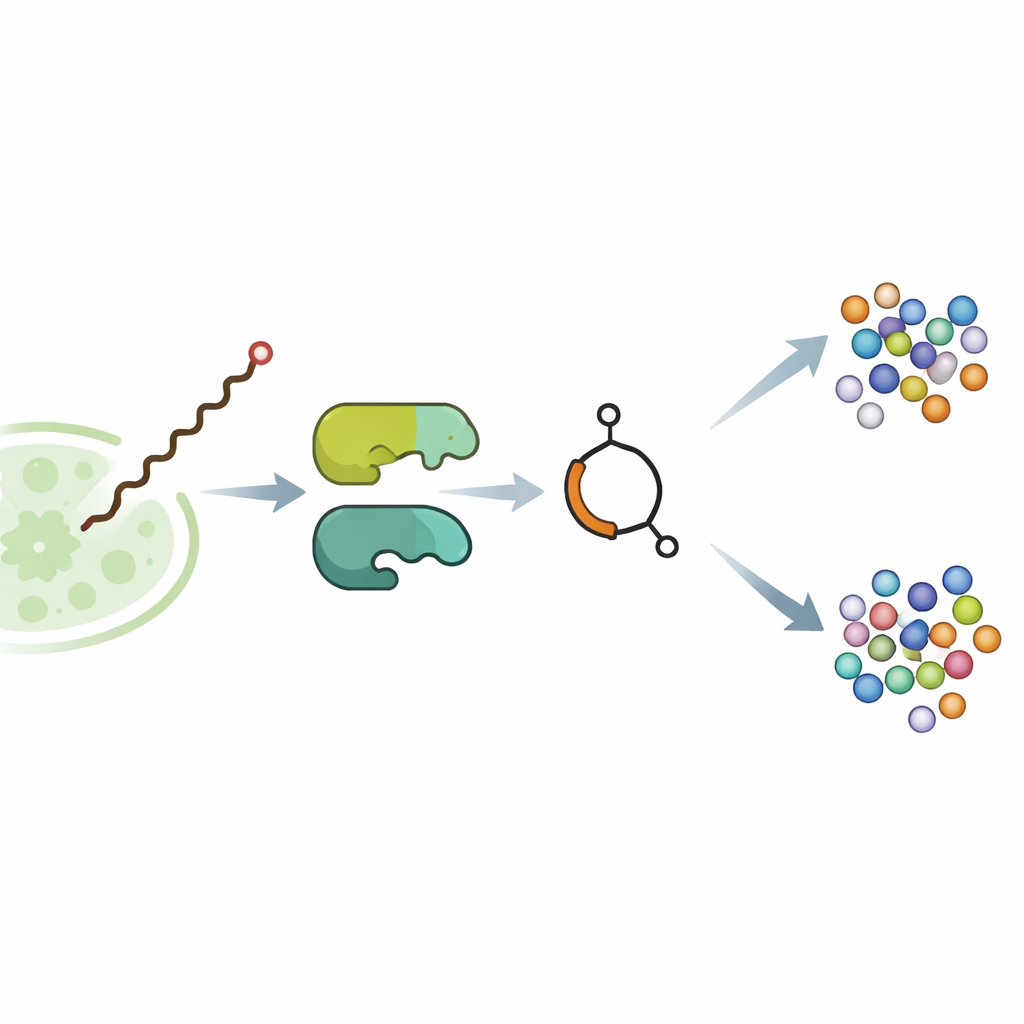
Één enzym dat drie opeenvolgende taken uitvoert
De belangrijkste verrassing van de studie is SavA, een flavine‑houdend enzym dat drie verschillende chemische transformaties uitvoert op een vetzuurachtig startblok afkomstig uit de normale stofwisseling van de cel. In proefbuisreacties met zorgvuldig gesynthetiseerde hartstikke-nabootsende substraten toonden de onderzoekers aan dat SavA eerst waterstofatomen verwijdert om een dubbele binding in te voeren, vervolgens een zuurstofhoudende groep op een specifieke positie toevoegt, en tenslotte de keten laat sluiten tot de butenolide‑ring. Isotoopexperimenten met zuurstofgas verrijkt in een zwaardere zuurstofisotoop bevestigden dat de ringzuurstof rechtstreeks uit de lucht afkomstig is. Structurele modellering en gerichte mutaties wezen op een enkel aminozuur als de base die de reactie op gang brengt, en toonden hoe het gebonden flavin‑cofactor heen en weer schakelt tussen geoxideerde en gereduceerde vormen zonder ooit verbruikt te worden.
Een afrondend enzym dat de zijketen fijn afstelt
Zodra SavA het chirale butenolide‑skelet heeft gevormd, neemt SavB — een cytochroom P450‑enzym — het over om de aangehechte koolstofketen te verfraaien. In aanwezigheid van zijn redoxpartners en een gebruikelijke cellulaire cofactor voert SavB een nauwkeurige reeks oxidaties uit op twee aangrenzende koolstofatomen. Tijdresolutie‑analyse onthulde twee tussenproducten: eerst een enkel gehydroxyleerd product, vervolgens een keto‑vorm, voordat het volledig functionele avenolide verschijnt. Nucleaire magnetische resonantie‑metingen bevestigden de posities en driedimensionale ordening van deze nieuwe groepen. Het werk laat zien dat SavB deze zuurstofatomen in een gedefinieerde volgorde en met strikte controle over oriëntatie introduceert, een belangrijke eigenschap voor de biologische activiteit van het hormoon. 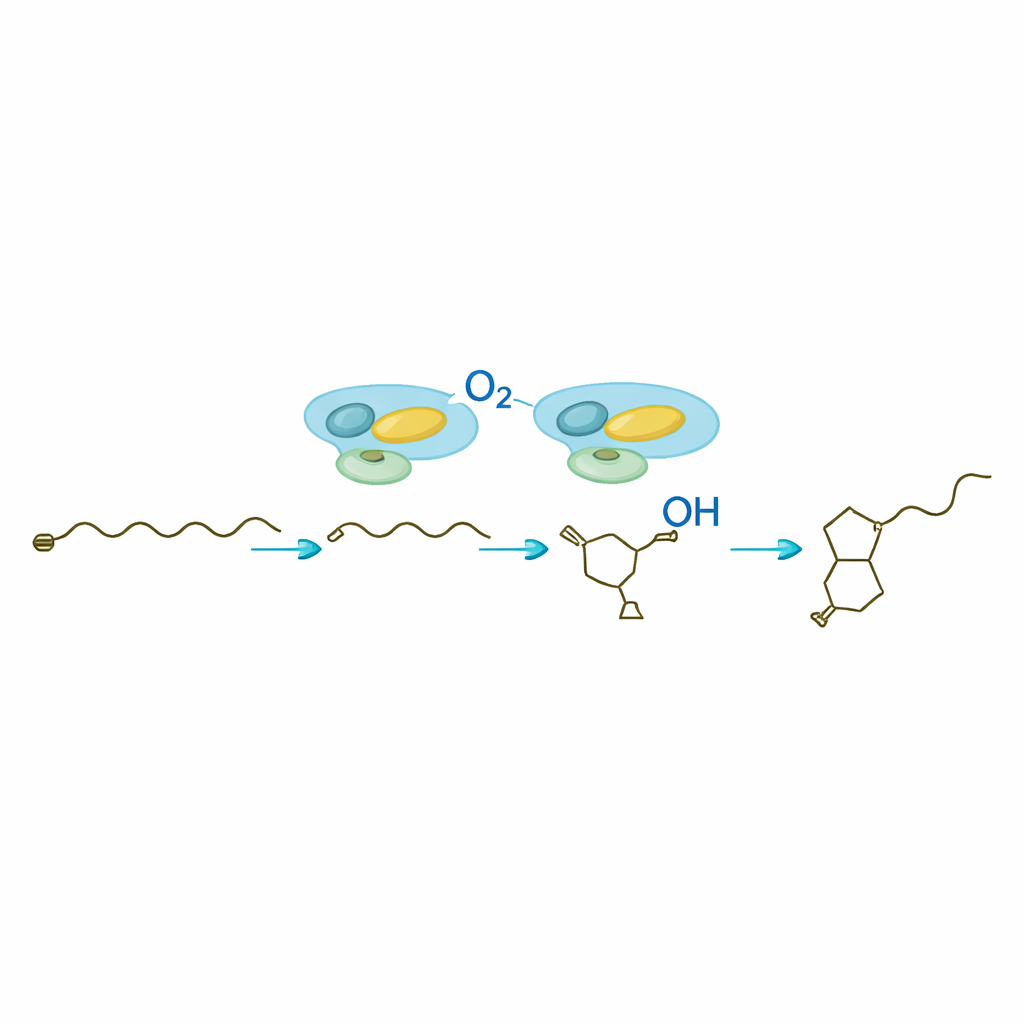
Groene chemie‑lessen van bacteriële enzymen
Samen zetten SavA en SavB een gewoon uit vetzuur afgeleid bouwblok om in een fijn afgestemd signaalmolecuul, waarbij ze alleen zuurstof uit de lucht en standaard cellulaire hulpstoffen gebruiken. In tegenstelling tot veel industriële processen heeft SavA geen extra reducerende middelen of offersubstraten nodig; zijn flavin‑cofactor transporteert eenvoudig elektronen terwijl het substraat zelf de aandrijvende kracht levert. De auteurs benadrukken SavA als een nieuw type veelzijdig flavo‑enzym met sterke potentie als biokatalysator voor duurzame productie van butenoliden en verwante motieven. In praktische termen kan het benutten of aanpassen van zulke enzymen op een dag fabrieken — of gemodificeerde microben — in staat stellen belangrijke geneesmiddelfragmenten en landbouwchemicaliën te maken uit hernieuwbare grondstoffen onder milde condities, wat zowel kosten als milieuvoetafdruk vermindert.
Bronvermelding: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Trefwoorden: butenolide‑biosynthese, flavo‑enzym SavA, avenolide‑hormoon, biokatalyse, Streptomyces‑signaalgeving