Clear Sky Science · nl
Afbrekers van het capsidproteïne van het denguevirus vertonen gedifferentieerde farmacologie ten opzichte van capsidremmers
Het omkeren van de viruskap
Dengue koorts infecteert jaarlijks honderden miljoenen mensen, maar artsen beschikken nog steeds niet over betrouwbare antivirale middelen om het te behandelen. Deze studie onderzoekt een nieuwe manier om het denguevirus onschadelijk te maken door een van zijn belangrijkste bouwstenen in geïnfecteerde cellen te vernietigen, in plaats van alleen diens activiteit te blokkeren. Het werk laat zien dat zorgvuldig ontworpen moleculen een sleutelviraal eiwit kunnen markeren voor verwijdering door het eigen afvalbeheersysteem van de cel, waardoor virusproductie afneemt en het vermogen van het virus om aan onze immuunafweer te ontsnappen wordt verzwakt.
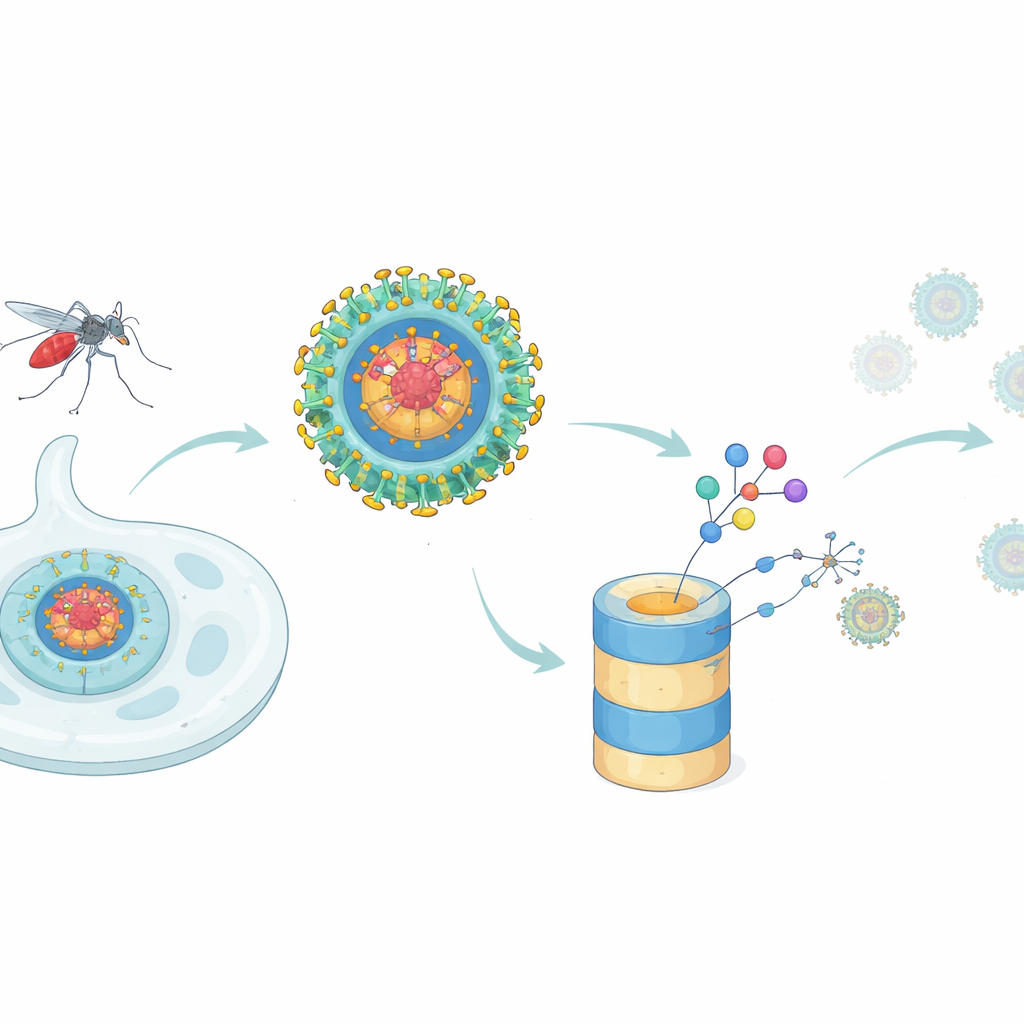
Een nieuwe tactiek om dengue te stoppen
De meeste antivirale middelen werken als stokjes in een machine: ze nemen plaats op één functionele plek van een viraal eiwit en proberen die te blokkeren. Die aanpak heeft moeite wanneer een enkel viraal eiwit veel verschillende taken heeft, of wanneer kleine mutaties de binding van het middel verzwakken. Het capsidproteïne van dengue is een goed voorbeeld. Het vormt de kernschil die het virale genetische materiaal verpakt in nieuwe deeltjes, maar het bemoeit zich ook met de gastheercel door met veel menselijke eiwitten te interageren en door de interferonrespons—een eerste antivirale alarmreactie—te onderdrukken. De auteurs vroegen zich af of een nieuwere medicijnstrategie—gerichte eiwitafbraak—bovengaat aan klassieke remmers door het capsidproteïne daadwerkelijk uit geïnfecteerde cellen te verwijderen.
Het ontwerpen van een moleculaire ‘premiejager’
Om zo’n degrader te bouwen, begonnen de onderzoekers bij ST148, een bekend klein molecuul dat aan het dengue‑capsid bindt en de assemblage van nieuwe virale deeltjes verstoort. Ze koppelden ST148 chemisch aan een tweede module die een menselijk enzymcomplex aantrekt dat verantwoordelijk is voor het markeren van eiwitten voor afbraak. De resulterende chimere moleculen, PROTACs genoemd, zijn zo gevormd dat ze het capsid aan het ene uiteinde grijpen en een E3‑ligasecomplex aan het andere, waardoor ze samenkomen en het capsid voorzien kan worden van ubiquitine‑labels en naar het proteasoom van de cel geleid kan worden, de belangrijkste eiwitvermaler. Door vele linkerlengtes en ligase‑rekruterende groepen te testen, identificeerden ze één opvallende verbinding, genoemd RPG‑01‑132, die betrouwbaar het capsidniveau in geïnfecteerde cellen verlaagde op een manier die afhankelijk was van de CRBN‑vorm van het ligase en van normale proteasoomfunctie.
Het stilleggen van virusproductie en immuunonderdrukking
Toen ze een werkende degrader hadden, onderzocht het team wat die daadwerkelijk deed voor de dengue‑infectie. In leverafgeleide cellen geïnfecteerd met denguevirus veroorzaakte RPG‑01‑132 een sterke daling van het aantal geïnfecteerde virussen dat vrijkwam, bij concentraties waarbij het alleen gedeeltelijk de totale capsidhoeveelheid verlaagde. Belangrijk is dat andere virale eiwitten en viraal RNA onveranderd bleven, wat aantoont dat de verbinding niet simpelweg de algemene replicatie vergiftigde maar specifiek handelde via verlies van het capsid. Elektronenmicroscopie gaf een visuele weergave: cellen behandeld met de oorspronkelijke remmer ST148 stapelden gedeeltelijk gevormde virusdeeltjes op in het endoplasmatisch reticulum, consistent met een blokkade van assemblage, terwijl cellen behandeld met de degrader vrijwel geen zichtbare virions toonden. De degrader herstelde ook het vermogen van het capsid om interferon‑β‑signaalvorming te onderdrukken in een reportersysteem, wat suggereert dat de niet‑structurele rol van het capsid bij het uitschakelen van de aangeboren immuniteit kan worden omgekeerd door het af te breken.
Het overwinnen van virusdiversiteit en geneesmiddelresistentie
Denguevirus komt in vier hoofdzakelijke serotypen die verschillen in hun gevoeligheid voor capsid‑gerichte remmers, en resistentie kan ontstaan door enkele mutaties. De auteurs vergeleken de degrader met ST148 over representatieve stammen van alle vier serotypen en tegen een virus dat een mutatie draagt (S34L in het capsid) waarvan eerder is aangetoond dat het ST148 ineffectief maakt. Zoals verwacht werkte ST148 het beste op één serotype en verloor het activiteit tegen de resistente mutant. RPG‑01‑132 daarentegen toonde vergelijkbare antivirale potentie over alle serotypen en behield activiteit tegen de S34L‑mutant, terwijl het nog steeds handelde via dezelfde CRBN‑afhankelijke degradatieweg. Dit illustreert een belangrijk voordeel van ‘event‑gedreven’ farmacologie: de degrader hoeft niet continu sterk aan elk capsidmolecuul vast te kleven, zolang hij genoeg afbraakevenementen kan triggeren om de balans te kantelen.
Wat dit betekent voor toekomstige dengue‑behandelingen
Deze studie toont aan dat het capsidproteïne van dengue niet alleen kan worden aangevallen als structureel onderdeel van het virus, maar ook als een verwijderbaar knooppunt dat meerdere stappen van infectie en immuunonderdrukking ondersteunt. Door een traditionele remmer om te zetten in een degrader, creëerden de onderzoekers een verbinding die virusproductie blokkeert, een deel van de virusgerelateerde onderdrukking van de aangeboren immuniteit opheft en effectief blijft over diverse virale stammen en een bekende resistentiemutatie. RPG‑01‑132 zelf zal optimalisatie nodig hebben—betere celopname, sterkere activiteit in diermodellen en zorgvuldige veiligheidscontroles—maar het levert een overtuigend proof of concept. Breder gezien suggereert het werk dat het kapen van het eigen verwijderingsapparaat van de cel nieuwe wegen kan openen naar antivirale middelen die moeilijker door virussen te omzeilen zijn en die eiwitten met veel verschillende rollen in geïnfecteerde cellen kunnen neutraliseren.
Bronvermelding: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Trefwoorden: denguevirus, capsidproteïne, gerichte eiwitafbraak, ontwerp van antivirale middelen, PROTACs