Clear Sky Science · nl
Coöperatieve anionactivatie bij een kobaltcentrum via ionparing en ligandontwerp
Waarom kleine partners rond metalen ertoe doen
Scheikundigen richten zich vaak op de hoofdrolspeler in een reactie — een metaalatoom dat helpt bindingen te breken en te vormen. Maar dit artikel laat zien dat de stille partners die in de nabijheid zweven, onzichtbaar voor het blote oog, het gedrag van het metaal volledig kunnen veranderen. Door de ruimte rond een kobaltatoom zorgvuldig te vormen, tonen de auteurs aan hoe twee vrijwel uitwisselbare anionen, die vaak als passieve toeschouwers in de chemie en batterijen worden gezien, tot scherp verschillende uitkomsten kunnen leiden. 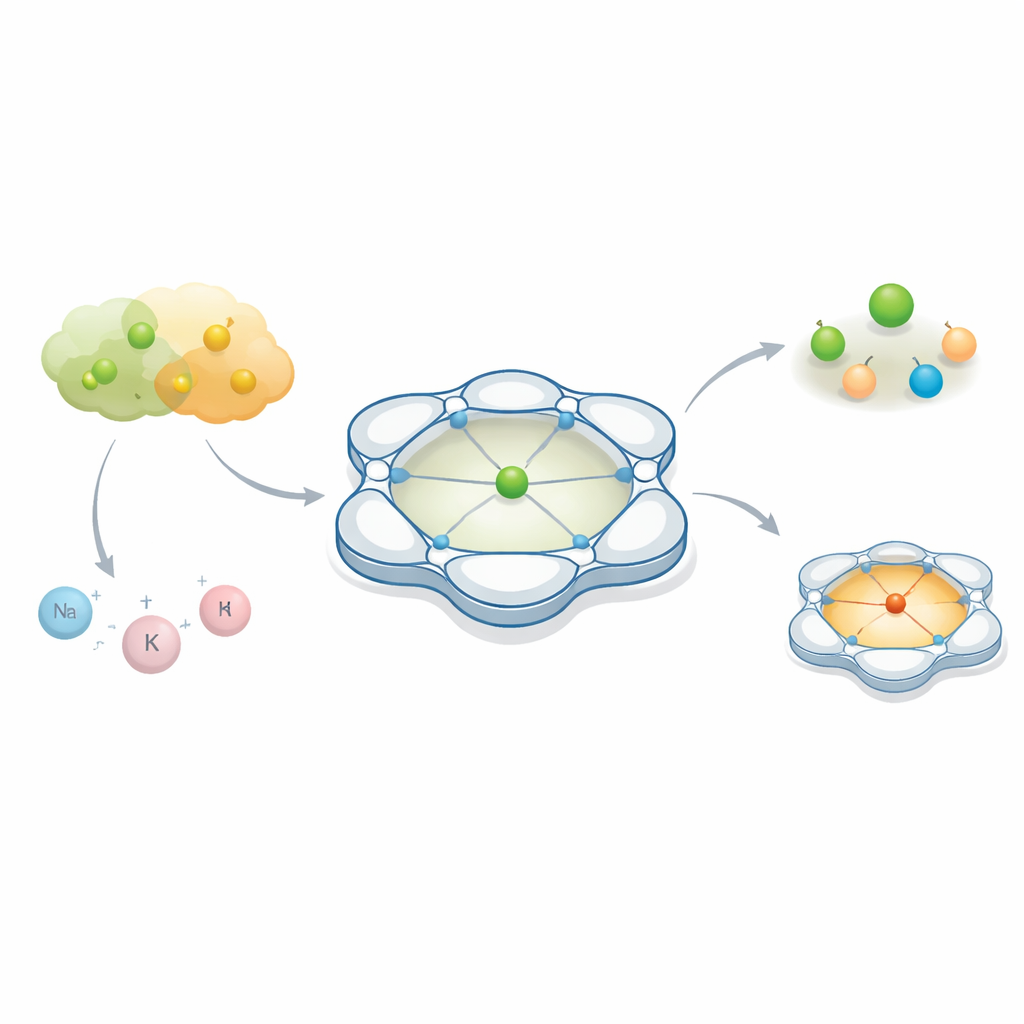
Een op maat gemaakte pocket rond kobalt bouwen
De onderzoekers ontwierpen een kooi‑achtig organisch raamwerk genaamd Py4Im dat zich strak om een kobaltion sluit. Dit raamwerk is opgebouwd uit meerdere gekoppelde pyridineringen en een imidazolidine‑eenheid, die samen een stijf, komvormig hol creëren met één N–H‑groep. Die kleine holte is ‘protisch’, wat betekent dat ze waterstofbruggen kan vormen, en ze wijst in een specifieke richting, als een klein dokje voor binnenkomende anionen. Wanneer kobalt met dit ligand wordt samengebracht, ontstaat een familie positief geladen complexen waarvan de algemene vorm en interne pocket gelijk blijven terwijl het tegenion — de negatief geladen partner — verwisselbaar is. Dat maakt het systeem tot een ideaal testveld om te zien hoe verschillende anionen zich in dezelfde gecontroleerde omgeving gedragen.
Twee gelijkende anionen, twee zeer verschillende gedragingen
Het team vergeleek twee veelgebruikte anionen, tetrafluorboraat (BF4−) en hexafluorfosfaat (PF6−), die vaak worden ingezet als zogenaamde zwak coördinerende anionen. Ze zijn populair omdat ze gewoonlijk afstand bewaren tot metaalcentra, en zo sterk geladen soorten stabiliseren zonder direct betrokken te raken. Verrassend genoeg gedragen ze zich binnen de Py4Im‑holte niet hetzelfde. Onder milde omstandigheden doneert PF6− een fluoride‑ion aan kobalt, waarbij een sterke P–F‑binding wordt verbroken en een goed gedefinieerd kobalt–fluoridecomplex ontstaat. In contrast weigert BF4−, dat doorgaans als het meer “fragiele” van de twee wordt gezien, in dezelfde omgeving fluoride af te staan. In plaats daarvan nestelt het zich in een stabiele ordening gebonden aan het kobaltcentrum zonder de stap van het breken van de binding te voltooien.
Ionparen zien vormen en bewegen
Om deze contrasterende gedragingen te begrijpen, gebruikten de auteurs een combinatie van hoogresolutie‑NMR‑technieken en quantumchemische berekeningen. Diffusie‑NMR‑experimenten maten hoe snel de positieve en negatieve soorten in oplossing bewegen, wat onthult hoe sterk ze gepaard zijn. Deze metingen toonden aan dat BF4− een nauwer, persistenter ionpaar vormt met het kobaltcomplex dan PF6−. De Py4Im‑holte positioneert het anion direct onder de imidazolidinering, waar waterstofbruggen van de N–H en nabijgelegen C–H‑groepen het op zijn plaats houden. Computerberekeningen bevestigden dat deze sterkere, directionele paring met BF4− de begintoestand zo sterk stabilizeert dat het breken van de B–F‑binding licht ongunstig wordt, zelfs al is die binding intrinsiek zwakker dan de P–F‑binding in PF6−. PF6−, dat losser paart, kan naderen, fluoride naar kobalt overdragen en vertrekken als PF5, wat leidt tot een fluoride‑dragend kobaltcomplex dat thermodynamisch toegankelijk is. 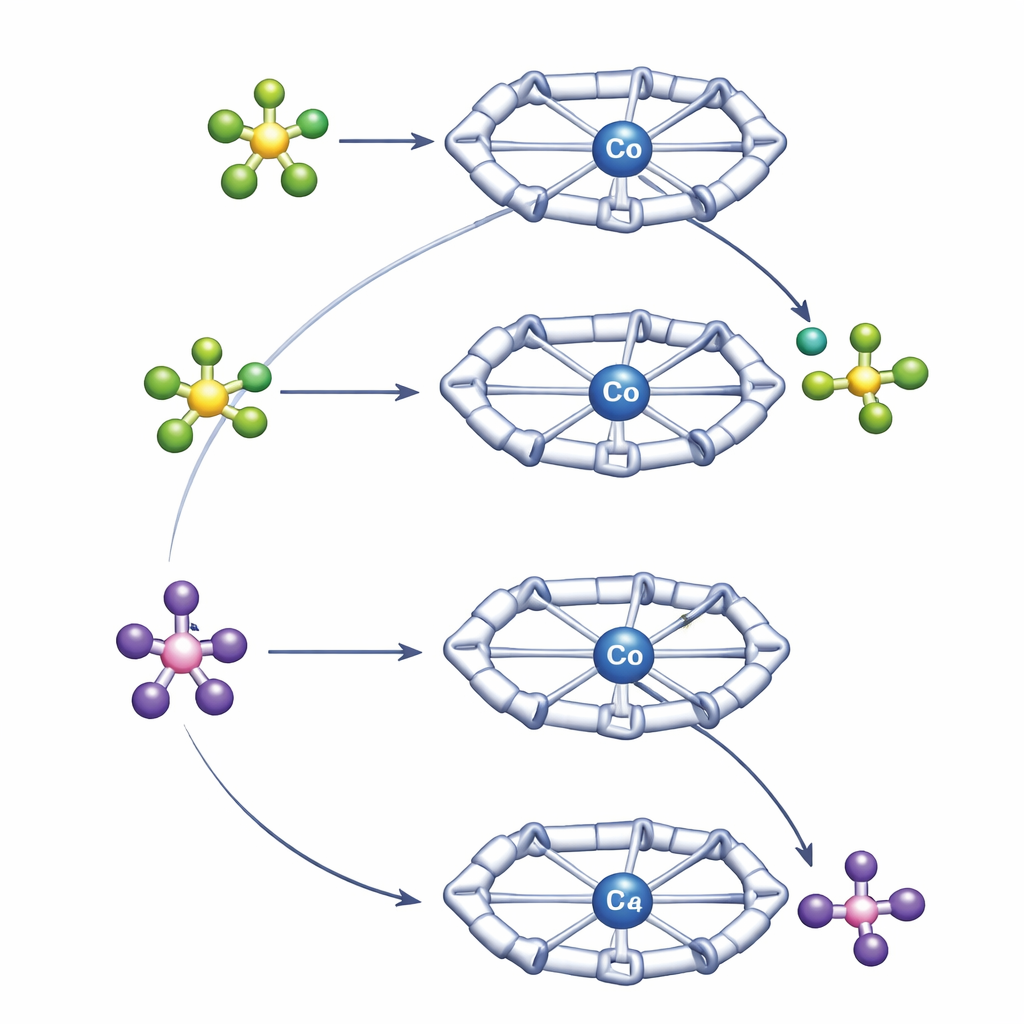
Een gebonden fluoride in een nuttig hulpmiddel veranderen
Zodra het kobalt–fluoridecomplex is gevormd, is het geen doodlopende weg. De auteurs tonen aan dat het fungeert als een nucleofiele fluoorbron — eenvoudiger gezegd, het kan fluoride afleveren aan positief geladen of elektronenarme partners. In oplossing draagt deze kobalt–fluoride‑soort schoon fluoride over aan reactieve koolstofcentra, aan siliciumatomen in chloorsilanen en aan acylchloriden, waarbij organische fluoriden worden gegenereerd terwijl het kobaltcomplex terugschakelt naar zijn chloorvorm of het nieuwe partnermolecuul bindt. In een slimme wending laten de onderzoekers ook zien dat BF4− kan worden overgehaald om fluoride af te staan als er een aparte base aanwezig is die het achterblijvende BF3‑fragment opvangt. Dit zet de anders onwillige BF4−‑route om in een die eveneens hetzelfde kobalt–fluorideproduct oplevert.
Wat dit betekent voor het ontwerpen van slimere katalysatoren
Voor niet‑specialisten is de kernboodschap dat ionen die ooit als inerte achtergrondzouten werden beschouwd, in feite reacties op krachtige wijze kunnen sturen. Door een precieze pocket rond een metaalcentrum te vormen en te beheersen hoe sterk anionen paaren met dat centrum, draaiden de auteurs de verwachte reactiviteit van twee bijna identieke soorten om. PF6−, doorgaans gezien als zeer robuust, wordt de makkelijkere bron van fluoride, terwijl BF4− wordt vastgehouden door sterkere paring tenzij het systeem wordt geholpen. Dit werk biedt een blauwdruk om ligandontwerp en keuze van tegenionen samen te gebruiken om de reactiviteit van een metaalcomplex te tunen — een idee dat invloed kan hebben op gebieden van homogeen katalyseren tot elektrolytontwerp voor geavanceerde batterijen, waar de “stille partners” in oplossing allesbehalve passief kunnen zijn.
Bronvermelding: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Trefwoorden: kobaltcomplexen, zwak coördinerende anionen, fluoridetransfer, ionparing, ligandontwerp