Clear Sky Science · nl
Metallisch molybdeensulfide katalyseert protometabole kooldioxide-reactienetwerken onder extreme omstandigheden
Hoe gesteente mogelijk de chemie van het leven op gang bracht
Lang voordat levende cellen enzymen ontwikkelden, moest de aarde al manieren hebben om eenvoudige gassen zoals kooldioxide om te zetten in de organische moleculen waar leven van afhankelijk is. Deze studie onderzoekt of bepaalde van nature voorkomende mineralen, vergelijkbaar met die in de buurt van onderzeese warmwaterbronnen, als primitieve "chemische motoren" hadden kunnen fungeren. Door aan te tonen dat een metallische vorm van molybdeensulfide kooldioxide kan omzetten in een verrassend rijk netwerk van organische verbindingen, biedt het werk een concreet scenario voor hoe de kernchemie van het leven op een levenloze planeet zou kunnen zijn begonnen.

Warmtebronnen en verborgen chemische motoren
Modern leven draait op ingewikkelde reactienetwerken die koolstof door cellen en ecosystemen verplaatsen. Deze netwerken vertrouwen op eiwitten die enzymen worden genoemd, die op hun beurt producten van evolutie zijn. De grote vraag is wat daaraan voorafging. De auteurs richtten zich op hydrothermale bronnen—natuurlijke, hete waterchimenes op de oceaanbodem, rijk aan metaalsulfiden en waterstofgas—als waarschijnlijke omgevingen voor de vroegste koolstofchemie. Op zulke plaatsen ontmoet heet, onder druk staand water gesteenten die metalen zoals ijzer, nikkel en molybdeen bevatten. Eerdere experimenten toonden aan dat sommige van deze metalen kooldioxide in kleine organische verbindingen kunnen omzetten, maar meestal slechts langs fragmenten van de metabole routes, niet volledige netwerken.
Een mineraal als nabootser van oude enzymen
Het team concentreerde zich op een specifieke vorm van molybdeensulfide, de zogenaamde 1T′-fase, waarvan de atomaire rangschikking de metaal-zwavelcentra nabootst die voorkomen in moderne enzymen die kooldioxide verwerken. Onder hoge temperatuur en druk in water, met waterstof als brandstof, katalyseerde dit mineraal de omzetting van opgelost kooldioxide (gemodelleerd als bicarbonaat) naar een onverwacht breed scala aan organische zuren. Door zorgvuldig temperatuur, reactietijd en gasdruk te variëren en producten te volgen met chromatografie, massaspectrometrie en NMR, identificeerden ze 32 verschillende tussenproducten en eindproducten die uit dezelfde eenvoudige koolstofbron ontstonden.
De kern-koolstofroutes van het leven herbouwen zonder enzymen
Die 32 verbindingen zijn niet willekeurig. Veel ervan zijn dezelfde moleculen die centraal staan in de moderne stofwisseling—zoals acetaat, pyruvaat, oxaloacetaat, succinaat en alfa-ketoglutaraat. Gezamenlijk corresponderen ze met vijf belangrijke koolstoffixeroutes die hedendaagse microben gebruiken: de acetyl–CoA-route en varianten van de Krebs-cyclus en aanverwante lussen. In de experimenten verschenen deze routes als een onderling verbonden netwerk: acetaat koppelde verschillende cycli; grotere moleculen vielen uiteen en werden opnieuw gevormd; en sleutelintermediairen verdwenen en kwamen later weer terug naarmate de omstandigheden veranderden. De productie van meerkoolstofzuren bereikte hoge efficiëntie, met tot ongeveer 70% van de omgezette koolstof die in moleculen met twee of meer koolstoffen terechtkwam. Het reactienetwerk vertoonde ook oscillaties waarbij de hoeveelheden van bepaalde producten in de loop van de tijd stegen en daalden, wat doet denken aan het dynamische gedrag van levende chemische systemen.
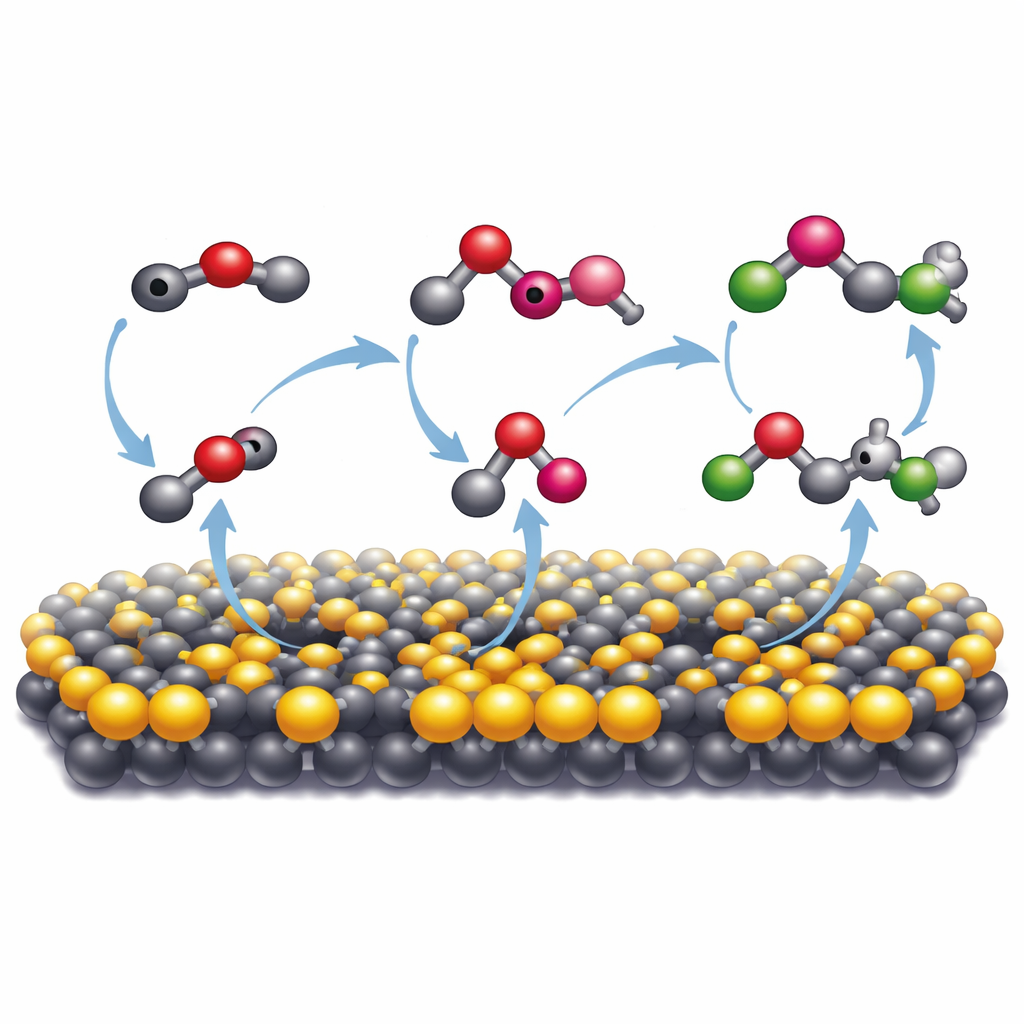
Hoe het mineraal koolstofatomen bijeenbrengt
Om te begrijpen waarom dit specifieke mineraal zo effectief was, vergeleken de onderzoekers het met een meer voorkomende vorm van molybdeensulfide die een andere atomaire structuur heeft. Alleen de metallische, vervormde vorm—met veel ontbrekende zwavelatomen—leidde tot uitgebreide vorming van grotere organische verbindingen. Spectroscopische technieken onthulden dat op dit oppervlak koolmonoxide, afgeleid van kooldioxide, sterk bindt en verder gereduceerd wordt tot zeer reactieve fragmenten, of radicalen. Deze radicalen worden op het mineraaloppervlak net genoeg gestabiliseerd om tegen elkaar aan te botsen en nieuwe koolstof–koolstofbindingen te vormen. Elektron-spinmetingen bevestigden de aanwezigheid van zulke radicalen, en het toevoegen van een radicalenvanger chemische stof onderdrukte de meerkoolstofproducten sterk. Computersimulaties ondersteunden dit beeld en toonden dat zwavelvacatures en de gewijzigde elektronische structuur van de 1T′-fase het eenvoudiger maken voor het oppervlak om elektronen te doneren en om koolstoffragmenten dichter bij elkaar te trekken zodat ze kunnen combineren.
Van gesteentechemie naar de eerste stofwisseling
Alles bij elkaar suggereren deze bevindingen dat bepaalde metaalsulfidemineralen op de vroege aarde complexe, zichzelf organiserende koolstofchemie zouden hebben kunnen draaien, lang voordat enzymen bestonden. In hydrothermale omgeving, waar hete, waterstofrijke vloeistoffen kooldioxide en metaalhoudende gesteenten ontmoeten, zou een mineraal zoals 1T′ molybdeensulfide continu anorganische koolstof kunnen omzetten in een web van onderling verbonden organische routes die lijken op moderne metabolische cycli. Voor niet-specialisten is de kernboodschap dat de centrale chemie van het leven mogelijk geen leven nodig had om te beginnen: onder de juiste omstandigheden kunnen eenvoudige stenen, water en gas spontaan veel van dezelfde moleculen en reactielussen opbouwen die levende cellen ook vandaag nog gebruiken.
Bronvermelding: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Trefwoorden: oorsprong van het leven, prebiotische chemie, hydrothermale bronnen, koolstoffixatie, molybdeensulfide