Clear Sky Science · nl
Interpreteerbare en generatieve deep learning-modellen verklaren fasegescheiden intrinsiek gedesorganiseerde motieven
Waarom kleine eiwitsegmenten ertoe doen
Binnen elke cel verzamelen vitale moleculen zich vaak in druppelachtige clusterings die biomoleculaire condensaten worden genoemd. Deze druppels helpen de chemie te organiseren zonder een membraan, en beïnvloeden hoe genen worden aangestuurd, hoe signalen worden doorgegeven en hoe cellen op stress reageren. Veel van deze druppels worden gevormd door flexibele reeksen van eiwitten die bekendstaan als intrinsiek gedesorganiseerde regio’s. Toch hebben biologen moeite om precies die korte sequenties te identificeren die daadwerkelijk de vorming van deze druppels aandrijven. Deze studie presenteert een deep learning-framework, PhaSeMotif, dat zowel deze sleutelstukken kan opsporen als nieuwe kan ontwerpen, en zo onderzoekers een krachtig middel biedt om cellulaire druppels te onderzoeken en te herprogrammeren.
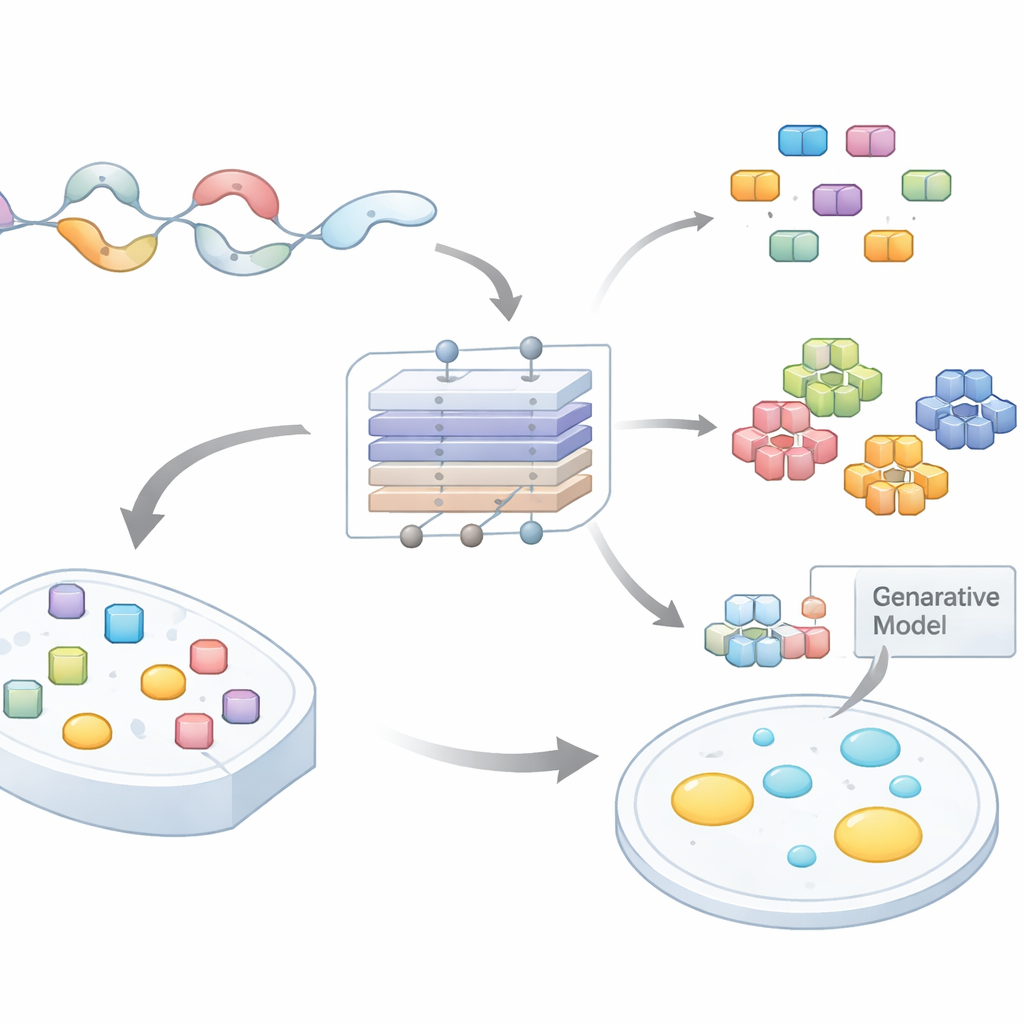
Van rommelige eiwitslierten naar toetsbare ideeën
Veel eiwitten bevatten lange, flexibele staarten die niet in vaste structuren vouwen. Deze gedesorganiseerde regio’s zijn verrijkt in bepaalde aminozuren en bevatten vaak herhaalde patronen of korte motieven. Steeds meer onderzoek wijst erop dat zulke motieven condensatie aandrijven door veel zwakke interacties tegelijk mogelijk te maken. Het scannen van volledige proteomen om te bepalen welke korte stukken belangrijk zijn — en waarom — is echter een grote bottleneck gebleven. Bestaande computationele hulpmiddelen beoordelen meestal hele eiwitten of grote regio’s en geven weinig aanwijzing waar te muteren of wat in het lab te testen. De auteurs wilden een model bouwen dat niet alleen voorspelt of een gedesorganiseerde regio druppels kan vormen, maar ook welke exacte subsequenties het zware werk doen.
Een deep learning-kaart van druppel-aandrijvende motieven
Het team stelde grote datasets samen van gedesorganiseerde regio’s uit meerdere soorten en labelde ze op basis van de kans dat hun gastheereiwitten fase-separatie ondergaan. Ze trainden vervolgens een op attention gebaseerd neuraal netwerk, PhaSeMotif, dat een aminozuursequentie van willekeurige lengte neemt en een score voor druppelvorming uitspuwt. Cruciaal is dat het netwerk een combinatie van convolutionele lagen en attention-mechanismen gebruikt om te beoordelen hoeveel elk kort venster van de sequentie bijdraagt aan die score. Door terug te traceren door het model (met technieken vergelijkbaar met guided backpropagation) extraheerden de auteurs hoogbelangrijke stukjes — korte motieven vaak kleiner dan 20 residuen — die het model als essentieel voor druppelvorming beschouwde.
Voorspellingen testen in levende cellen
Om te controleren of deze motieven echt van belang waren, gebruikten de onderzoekers een lichtgeactiveerd systeem in menselijke cellen. Ze fuseerden voorspelde druppelvormende gedesorganiseerde regio’s aan een lichtgevoelige oligomerisatiemodule en een fluorescente tag. Onder blauw licht condenseerden deze constructen snel tot felle puncta, waarmee fase-separatie in real time werd gerapporteerd. Het team verwijderde vervolgens individueel motieven door ze chirurgisch te vervangen door neutrale, flexibele linkers van dezelfde lengte. Bij 82% van de 17 gewijzigde sequenties die werden getest, werd druppelvorming sterk verzwakt of verdween volledig, terwijl controlemutaties buiten PhaSeMotif-segmenten vaak weinig effect hadden. Belangrijk is dat veel van deze sleutelmotieven overlapten met plaatsen waar ziektegerelateerde mutaties bekendstaan die condensatie verstoren, wat hun biologische relevantie onderstreept.
Het blootleggen van een woordenboek aan motieftypen
Met meer dan 17.000 motieven in handen vroegen de auteurs zich vervolgens af of er gemeenschappelijke «smaakjes» van druppel-aandrijvende segmenten bestonden. Ze analyseerden aminozuursamenstelling en patroonvorming en groepeerden de motieven in negen clusters. Sommige clusters waren rijk aan aromatische residuen en glycine, wat overeenkomt met kleverige π–π- en cation–π-interacties. Andere bevatten gescheiden patches van positieve en negatieve ladingen, die elektrostatische aantrekking en selectieve partitionering in bepaalde condensaten bevorderen. Aanvullende clusters werden gedomineerd door proline en glycine, die flexibiliteit ondersteunen, of door lange reeksen glutamine die dichte netwerken van waterstofbruggen kunnen vormen. Verschillende compartimenten en condensaattypen vertoonden kenmerkende mengsels van deze motiefklassen, wat suggereert dat motiefsamenstelling mede bepaalt waar en met welke partners een eiwit zal condenseren.
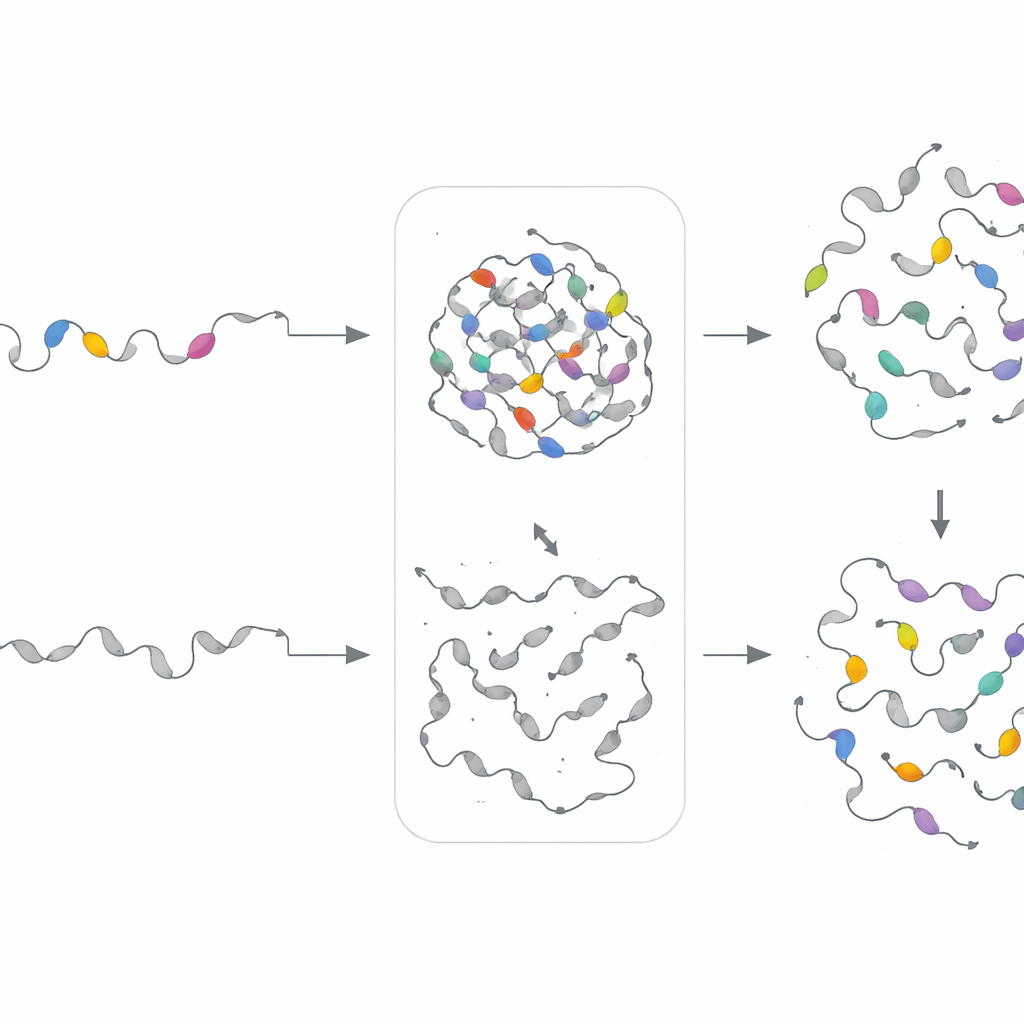
Nieuwe motieven ontwerpen om de regels te bewijzen
Om te testen of motief-«recepten» — in plaats van exacte sequenties — het druppelgedrag bepalen, bouwde het team afzonderlijke generatieve modellen voor elk motiefcluster. Deze variational autoencoders leerden de statistische patronen voor een gegeven cluster en genereerden vervolgens nieuwe, kunstmatige sequenties die dezelfde compositionele vingerafdrukken maar een andere exacte volgorde deelden. De onderzoekers vervingen experimenteel deze synthetische motieven in eiwitten waarvan de originele segmenten waren verwijderd. Opmerkelijk genoeg herstelden in 18 van de 21 gevallen de ontworpen motieven de fase-separatie in cellen, en soms werden ook de snelheid of dichtheid van druppelvorming bijgesteld. Dit toont aan dat PhaSeMotif onderliggende ontwerprichtlijnen vastlegt die hergebruikt kunnen worden om druppelvormende regio’s te bouwen of te repareren.
Wat dit betekent voor biologie en ziekte
Door interpreteerbare deep learning te koppelen aan generatief ontwerp en directe cellulaire testen, verandert dit werk de vage notie van «gedesorganiseerde druppelvormende regio’s» in een concreet stel korte, samenstelbare motieven. Voor niet-experts is de conclusie dat wetenschappers nu de kleine eiwitsegmenten kunnen lezen en schrijven die bepalen hoe cellulaire druppels zich vormen, mengen en verkeerd functioneren. Dit opent de deur naar snellere opsporing van ziekteveroorzakende mutaties in deze segmenten, helderder mechanistisch onderzoek naar hoe condensaten de celphysiologie organiseren, en uiteindelijk naar rationeel ontwerp van eiwitten die druppels sturen voor therapeutische of synthetische biologietoepassingen.
Bronvermelding: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Trefwoorden: biomoleculaire condensaten, intrinsiek gedesorganiseerde eiwitten, fase-separatie, deep learning, eiwitmotieven