Clear Sky Science · nl
Hepatocyten functioneel gereprogrammeerd door KIAA1199-hoog colorectale kankercellen bevorderen de ophoping van pro-metastatische Egr1+ neutrofielen
Wanneer darmkanker de lever op het oog heeft
De meeste mensen denken bij uitzaaiing aan kankercellen die zich losmaken en naar andere organen afdrijven. Deze studie vertelt een minder geruststellend verhaal: colorectale tumoren kunnen de lever geruisloos herschikken lang voordat enige kankercel arriveert, en zo een gastvrije “bodem” creëren waarin toekomstige tumoren gemakkelijk wortel schieten. Inzicht in deze verborgen voorbereidingsfase kan de weg openen naar behandelingen die levermetastasen — de belangrijkste doodsoorzaak bij colorectale kanker — stoppen nog voordat ze beginnen.
Een heimelijke voorbereiding voordat tumoren arriveren
Colorectale kanker zaait vaak naar de lever uit, maar niet alle tumoren doen dat even agressief. De auteurs concentreerden zich op een molecuul genaamd KIAA1199, dat overvloedig aanwezig is in hoog-risico colorectale kankers. In muismodellen en patiëntmonsters bleken tumoren met veel KIAA1199 niet alleen sneller te groeien; ze prepareerden ook de lever tot een “pre-metastatische niche”, een micro-omgeving die buitengewoon vriendelijk is voor binnenkomende kankercellen. Zelfs wanneer levertumoren experimenteel werden ingebracht vanuit een afzonderlijke bron, ontwikkelden dieren met KIAA1199-rijke colon tumoren veel meer levermetastasen en stierven ze eerder. Dit toonde aan dat signalen van de primaire tumor, en niet alleen ronddwalende kankercellen, de lever van tevoren hervormden.
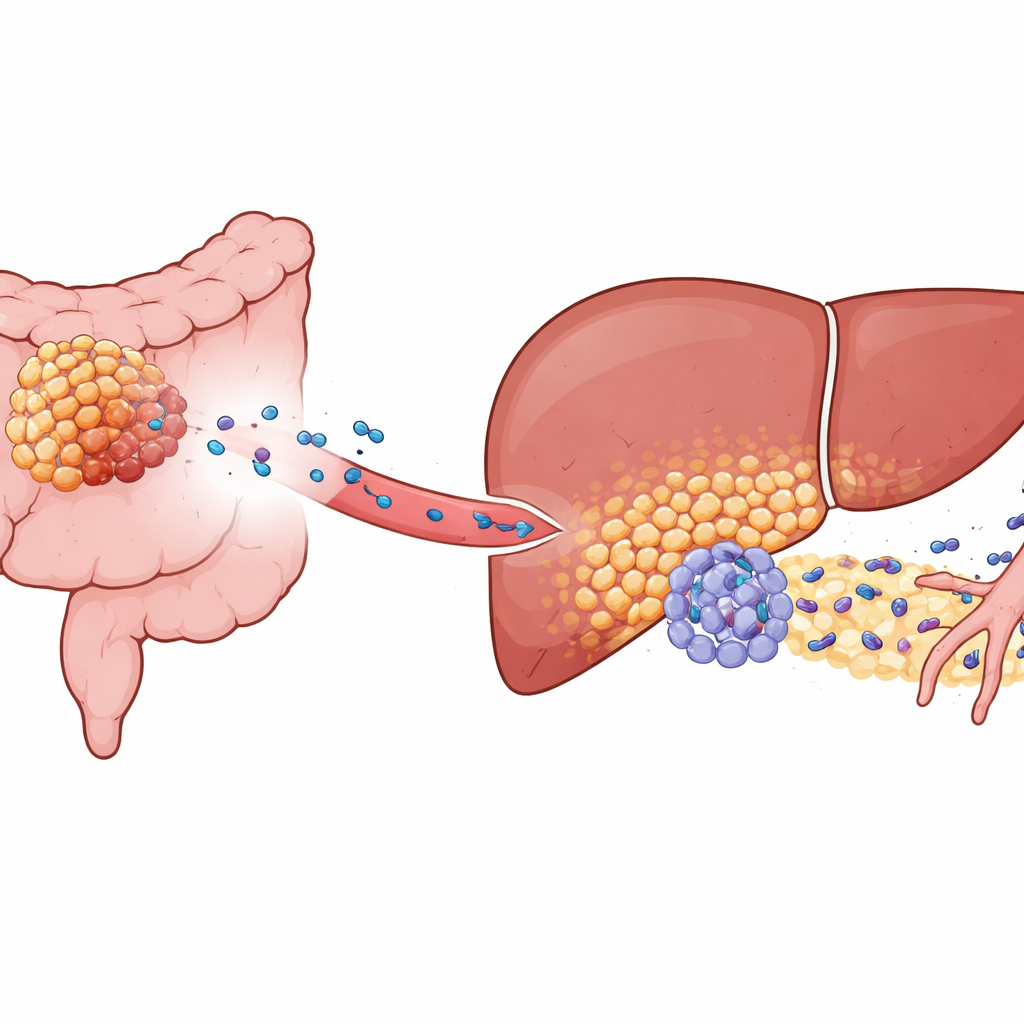
Levercellen gereprogrammeerd tot tumorhelpers
Dieper gravend gebruikten de onderzoekers single-cell sequencing en ruimtelijke mapping om leverweefsel op hoge resolutie te bekijken. Ze ontdekten een aparte subset hepatocyten — normaal gesproken de werkpaardcellen van de lever — die ‘‘functioneel gereprogrammeerd’’ leken te zijn. Deze cellen verschenen alleen wanneer KIAA1199-rijke tumoren aanwezig waren. In plaats van rustig het metabolisme te beheren schakelden de veranderde hepatocyten over naar een meer kwaadaardig-achtige metabole staat en dempten ze een beschermende regulator genaamd PPARγ, die gewoonlijk helpt ontsteking en stressreacties onder controle te houden. Met PPARγ onderdrukt begonnen deze hepatocyten hoge niveaus van een eiwit genaamd SAA2 te produceren, dat ze in hun omgeving vrijlieten, met name aan de rand waar leverweefsel de binnendringende tumorcellen ontmoet.
Gewone verdedigers omvormen tot pro-metastatische neutrofielen
Neutrofielen — witte bloedcellen die vooral bekend staan om het bestrijden van infecties — gedroegen zich ook afwijkend in deze geprepareerde lever. De auteurs vonden een speciale subset met een ‘‘Egr1+’’ signatuur, genoemd naar een transcriptiefactor die de functie van deze cellen hervormt. In plaats van al gemuteerd uit de bloedbaan te komen, leken neutrofielen lokaal te worden heropgevoed door de gereprogrammeerde hepatocyten. SAA2, vrijgegeven door hepatocyten, bond aan een receptor genaamd FPR2 op nabijgelegen neutrofielen en activeerde zo een intern PI3K‑AKT signaalcircuit dat de Egr1-activiteit stabiliseerde. Het resultaat was een langerlevende, zeer actieve neutrofiel die grote hoeveelheden VEGFA uitscheidde, een sterke stimulator van de groei van nieuwe bloedvaten. Deze Egr1+ neutrofielen clusteren bij de tumor–lever grens, precies daar waar nieuwe, fragiele bloedvaten ontspruiten.
Bloedvaten bouwen die tumorcellen verwelkomen
De studie toont aan dat deze heropgevoede neutrofielen geen bijstanders zijn — ze remodelleren actief de vasculatuur van de lever. In kweek zorgden factoren die door Egr1+ neutrofielen werden vrijgegeven ervoor dat endotheelcellen gingen groeien, migreren en buisachtige structuren vormden die deden denken aan nieuwe vaten. In muizen verhoogde de toevoeging van Egr1+ neutrofielen levermetastasen en versnelde het overlijden. Het blokkeren van sleutelstappen in de keten — hetzij het SAA2–FPR2-signaal naar neutrofielen, hetzij het downstream PI3K‑AKT‑pad — maakte een einde aan de overleving van neutrofielen en de VEGFA-productie, waardoor vaatgroei en metastatische verspreiding werden verminderd. Evenzo verlaagde het herstellen van PPARγ-activiteit in hepatocyten met het diabetesmiddel rosiglitazon de SAA2-niveaus, remde het ontstaan van Egr1+ neutrofielen en verminderde sterk de levermetastase in preklinische modellen.
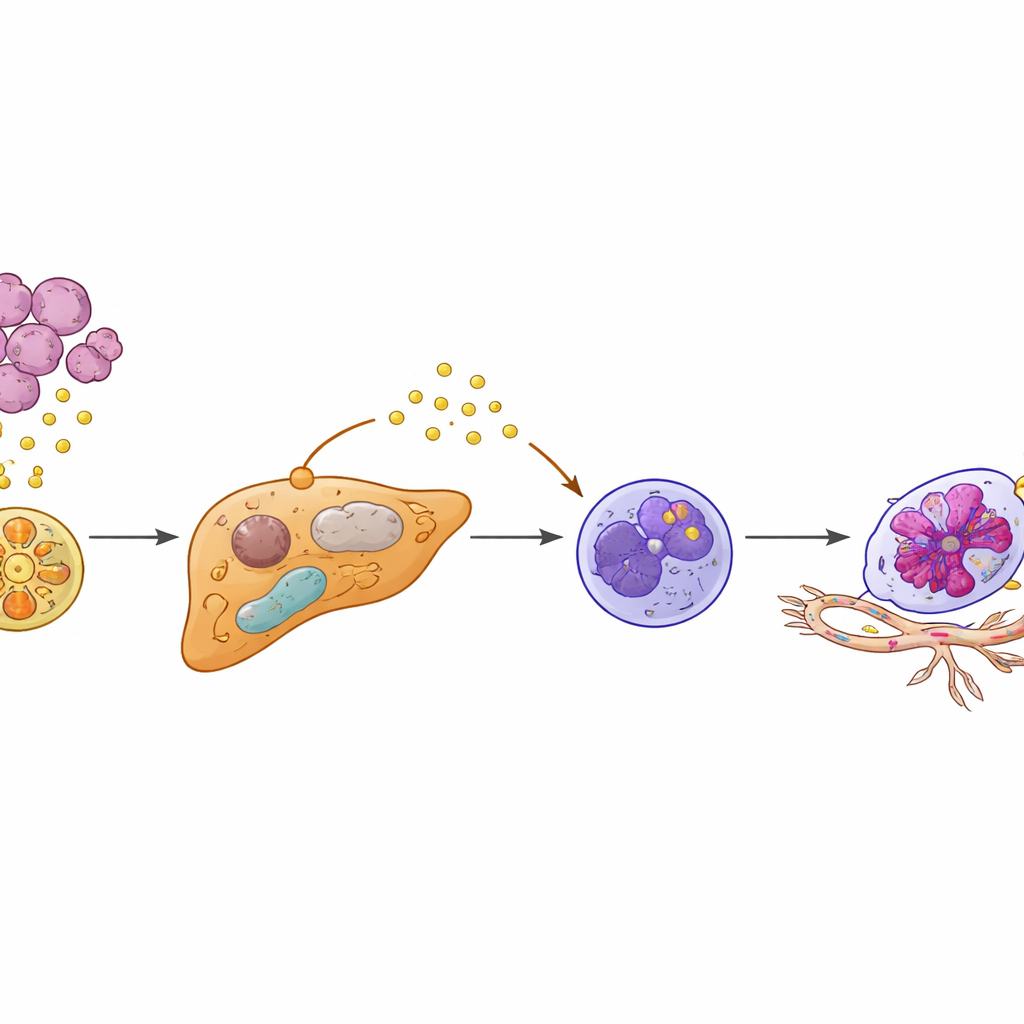
Van mechanisme naar voorspelling en preventie
Omdat KIAA1199 in tumoren en SAA2 in de lever hoog in deze cascade zitten, testten de auteurs of deze eiwitten patiënten met een hoog risico op levermetastase konden identificeren. In meerdere patiëntcohorten bleken mensen met hoge bloedspiegels van beide merkers veel waarschijnlijker en veel sneller levermetastasen te ontwikkelen. Een eenvoudige gecombineerde KIAA1199–SAA2-score presteerde beter dan één enkele marker in het voorspellen van risico en werd verpakt in een klinische ‘‘nomogram’’ dat de kans van een individuele patiënt op leveruitzaaiing over de volgende twee jaar schat. Samen schetsen de bevindingen een duidelijk beeld: KIAA1199-rijke colonkankers sturen via vesikelgevoerde signalen aanpassingen aan hepatocyten, die op hun beurt nabijgelegen neutrofielen omzetten in langlevende, vatvormende medespelers. Door deze KIAA1199–PPARγ/SAA2–Egr1-as te richten — met metabole geneesmiddelen, immuunregulerende middelen of beide — kan het mogelijk zijn niet alleen bestaande levermetastasen te behandelen, maar ze ook te voorkomen voordat ze zich vestigen.
Bronvermelding: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Trefwoorden: levermetastase van colorectale kanker, pre-metastatische niche, neutrofielen, reprogrammering van hepatocyten, tumormicro-omgeving