Clear Sky Science · nl
Vermindering van methylering van histon 3.3 lysine 4 in de mediale ganglionaire eminence en hypothalamus bootst fenotypes van neuro-ontwikkelingsstoornissen na
Hoe kleine chemische labels de hersenen en het lichaam vormen
Waarom veroorzaken sommige genetische veranderingen zowel leerproblemen als ongebruikelijke groei, zoals heel klein zijn in de kindertijd maar obesitas in de volwassenheid? Deze studie bekijkt kleine chemische labels op de eiwitten die DNA verpakken in de hersenen en laat zien hoe het verstoren ervan in slechts twee belangrijke regio’s kan doorwerken naar aanvallen, angstachtig gedrag, geheugenproblemen en sterke veranderingen in lichaamsgrootte bij muizen.
Schakelaars op de dimmers van het genoom
In elke hersencel is DNA rondom spoelachtige eiwitten gewikkeld die histonen worden genoemd. Chemische merktekens op deze histonen werken als dimmers: ze zetten groepen genen omhoog of omlaag. Eén zo’n merkteken, toegevoegd op een plek die H3K4 heet, is sterk gekoppeld aan het aanzetten van genen. Menselijke genetische studies hebben aangetoond dat mensen die geboren zijn met fouten in enzymen die dit merkteken toevoegen of verwijderen vaak neuro-ontwikkelingsstoornissen hebben die verstandelijke beperkingen, epilepsie en abnormale lichaamsgroei combineren. Het was echter onduidelijk welke hersencellen het meest gevoelig zijn voor deze verstoring en hoe hun disfunctioneren de relatie tussen hersenexcitabiliteit en het metabolisme van het hele lichaam kan verklaren.
Richten op twee kritieke hersenknooppunten
De onderzoekers ontwierpen muizen waarbij een gemuteerde versie van een histoneiwit (H3.3K4M) alleen werd aangezet in cellen die voortkomen uit twee embryonale hersenregio’s: de mediale ganglionaire eminence, die veel van de remmende ‘rem’-cellen van de hersenen produceert, en de zich ontwikkelende hypothalamus, die helpt bij het reguleren van eetlust, hormonen en energiebalans. Deze mutatie blokkeert specifiek H3K4-methylering zonder de histonen zelf te verwijderen. Tests bevestigden dat het gemuteerde eiwit wijd verspreid aanwezig was in de doelgebieden en dat de normale H3K4-merktekens daar sterk verminderd waren terwijl de totale histonniveaus stabiel bleven. Dit ontwerp bootst veel menselijke aandoeningen na waarbij slechts één kopie van een H3K4-gerelateerd gen defect is, in plaats van volledig afwezig.
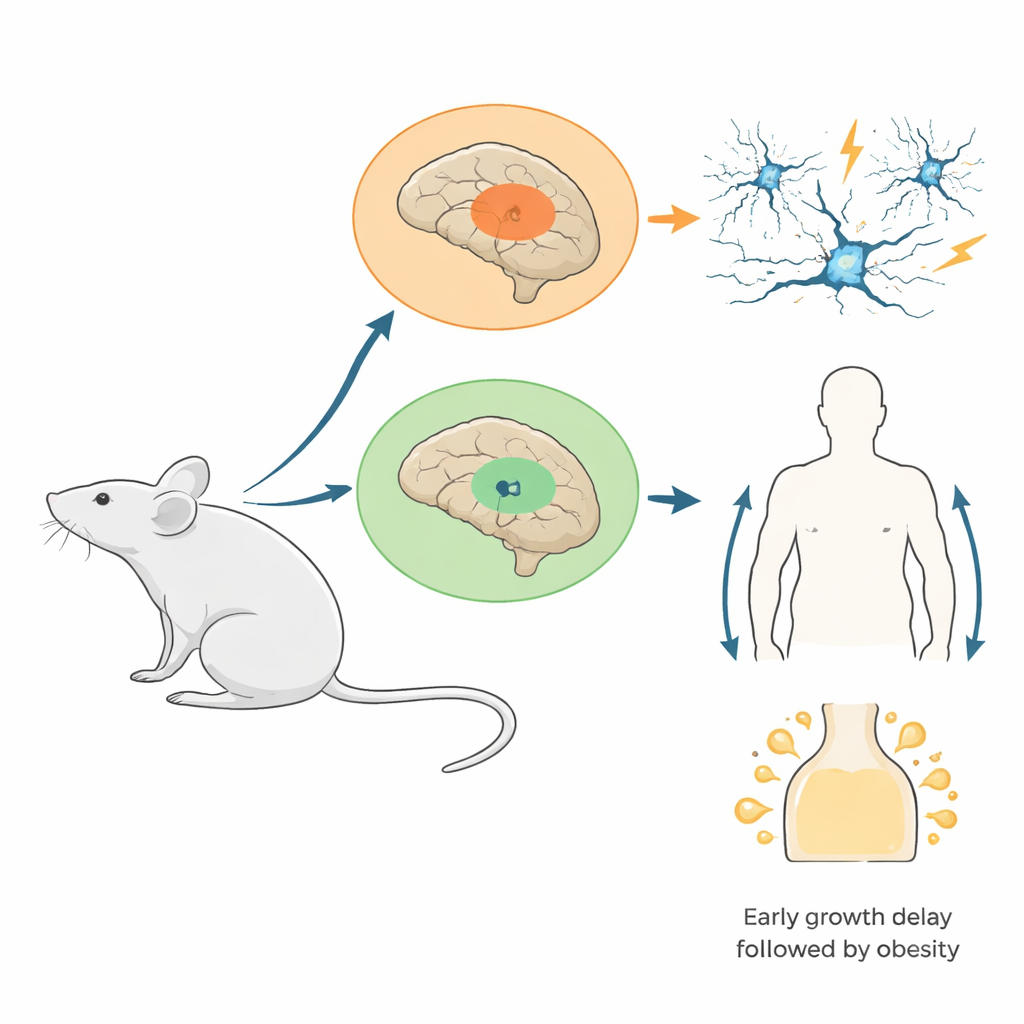
Van ontbrekende remcellen naar circuit-gevoeligheid voor aanvallen
Naarmate deze muizen opgroeiden, werden de gevolgen voor hersencircuits duidelijk. Jonge mutanten hadden minder remmende interneuronen in de cortex en hippocampus, vooral een snel vurende soort die normaal gesproken neurale ritmes strak timet. Gedetailleerde opnamen toonden dat de overgebleven interneuronen aanwezig waren maar meer variabel in hun elektrische eigenschappen, wat suggereert dat hun rijping verstoord was. Wanneer de hippocampus in breinsneden werd gestimuleerd, waren de gebruikelijke hoogfrequente ‘gamma’-oscillaties—elektrische ritmes die aan informatieverwerking zijn gekoppeld—zwakker en trager, en verschenen abnormale burst-achtige gebeurtenissen. In levende dieren ontwikkelden veel mutanten, vooral vrouwtjes, spontane aanvallen en waren ze veel gevoeliger voor geneesmiddel-geïnduceerde aanvallen. Vroeg in de ontwikkeling traceerde het team dit celverlies voornamelijk tot slechte migratie van interneuronen naar de cortex, niet tot verhoogde celdood of verminderde celdeling.
Herbedrading van genactiviteit in aan aanvallen gelinkte cellen
Om deze fysieke veranderingen aan genregulatie te koppelen, gebruikte het team single-nucleus sequencing die zowel genactiviteit als DNA-toegankelijkheid van individuele cellen leest. In de embryonale mediale ganglionaire eminence werden de meeste genen die in mutanten veranderden naar beneden bijgesteld, inclusief belangrijke regulatoren die cellen sturen naar specifieke remmende identiteiten. In volwassen interneuronen verschoof de balans tussen subtypes en waren groepen genen betrokken bij het vormen van verbindingen en het regelen van kaliumstromen—de stromen die helpen de vuursnelheid te bepalen—ontregeld. Netwerkanalyse benadrukte gecoördineerde verstoring van kaliumkanaalgenen die al bekend zijn om invloed te hebben op epilepsie en hersenritmes, wat een direct moleculair verband legt tussen het verlies van een histonmerkteken, veranderde interneuronenidentiteit en gevoeligheid voor aanvallen.
Hypothalamische disbalans en een tweefasige groeicurve
De hypothalamus vertelde een complementair verhaal gericht op lichaamsgroei. Als pups waren de mutantmuizen kleiner en een aanzienlijk deel stierf vroeg. Overlevers daarentegen aten later meer, stapelden vet op en ontwikkelden hoge niveaus van het hormoon leptine, wat wijst op obesitas en waarschijnlijke leptineresistentie. Single-cell-analyse van de embryonale hypothalamus toonde meer delende voorlopercellen maar minder cellen bestemd voor sleutelkernen die met eten te maken hebben, vooral regio’s die normaal voedingsstatus voelen en de groeihormoonregeling sturen. In de volwassen hypothalamus was de cellulaire samenstelling herschikt: astrocyten namen sterk toe, oligodendrocyten namen af, en gespecialiseerde barrièrecellen genaamd tanycyten en aangrenzende glia verloren hun ordelijke rangschikking op de grens tussen hersenen en circulerende hormonen en voedingsstoffen. Deze structurele en genexpressieveranderingen vervormen waarschijnlijk hoe de hersenen energiereserves waarnemen en eetlust reguleren.
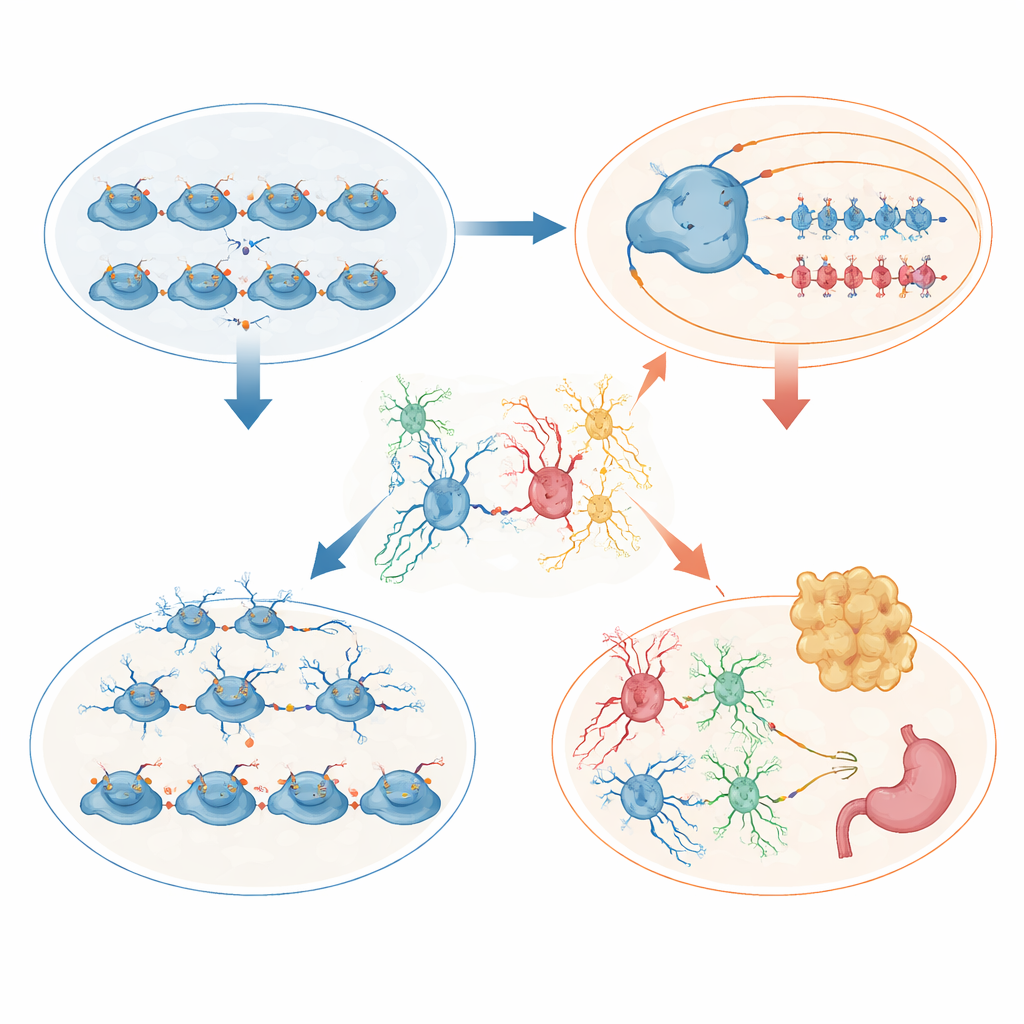
Gedragsweerklanken van menselijke neuro-ontwikkelingsstoornissen
Het gedrag van de muizen weerspiegelde symptomen die bij veel neuro-ontwikkelingscondities worden gezien. Ze vertoonden sterker angstachtig gedrag, veranderde gang, verminderde spontane beweging thuis en slechte prestaties bij taken die geheugen, objectherkenning en het filteren van schrikreacties onderzoeken. Sommige testen toonden verhoogd impulsief gedrag. Over meerdere metingen waren vrouwtjes doorgaans zwaarder getroffen dan mannetjes, wat suggereert dat sekse-specifieke hormoonsystemen en genregulatie kunnen samenkomen met histonmerktekens om kwetsbaarheid te vormen.
Wat dit betekent voor de menselijke gezondheid
Gezamenlijk tonen de bevindingen aan dat het verzwakken van één set histonmerktekens in slechts twee embryonale hersenknooppunten voldoende is om een brede constellatie van problemen na te bootsen: minder remmende ‘remmen’, instabiele hersennetwerken, aanvallen, verstoorde voedcircuits en abnormale lichaamsgroei. Voor niet-specialisten is de kernboodschap dat epigenetische merktekens zoals H3K4-methylering geen vage toevoegingen zijn maar precieze controleknoppen die ontwikkelende hersencellen helpen het juiste type te worden, op de juiste plaats en op het juiste moment. Wanneer die knoppen verkeerd staan, zoals bij veel zeldzame genetische syndromen, kan het resultaat een nauw verbonden combinatie van cognitieve, gedrags- en metabole symptomen zijn. Het begrijpen van deze gedeelde wortels kan uiteindelijk therapieën sturen die niet alleen één symptoom corrigeren, zoals aanvallen of obesitas, maar het onderling verbonden systeem dat eraan ten grondslag ligt.
Bronvermelding: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Trefwoorden: epigenetica, interneuronen, hypothalamus, aanvallen, obesitas