Clear Sky Science · nl
Ecologische partitionering maakt phage–antibiotica‑samenwerking mogelijk bij een humane Pseudomonas‑infectie
Waarom dit verhaal over bacteriën en virussen ertoe doet
Voor mensen met cystische fibrose kunnen longinfecties een levenslange strijd worden die standaardantibiotica uiteindelijk niet winnen. Deze studie volgt één oudere patiënt van wie de infectie door een hardnekkige Pseudomonas‑bacterie niet meer op veel middelen reageerde. Artsen voegden zorgvuldig bereide virussen toe die specifiek deze bacteriën aanvallen, zogenaamde fagen, aan zijn behandeling. Door niet alleen symptomen maar ook de microben en immunologische reacties in zijn longen in de tijd te volgen, laten de onderzoekers zien hoe antibiotica, fagen en de eigen afweer van de patiënt samenwerkten om een gevaarlijke infectie terug te dringen — maar niet volledig uit te roeien.
Een long in een langdurig patstelling
Bij gevorderde cystische fibrose zitten de luchtwegen vol met dik slijm en vestigen Pseudomonas‑bacteriën zich voor de lange termijn. In de loop van jaren splitsen ze zich in verschillende vormen: sommige omhuld met slijm, minder agressief maar makkelijker door antibiotica te bereiken, andere kaal, snelgroeiend en sterk geneesmiddelresistent. Bij deze patiënt bestonden twee zulke subpopulaties naast elkaar. Eerstelijnsantibiotica hielpen even, maar moesten worden gestaakt vanwege nierschade. Een tweede middel, ciprofloxacine, verbeterde de ademhaling enigszins maar liet de hardere, multiresistente bacteriën weer opkomen. In plaats van een simpele infectie was de long een mozaïek van bacteriële niches geworden die heel verschillend op hetzelfde geneesmiddel reageerden.
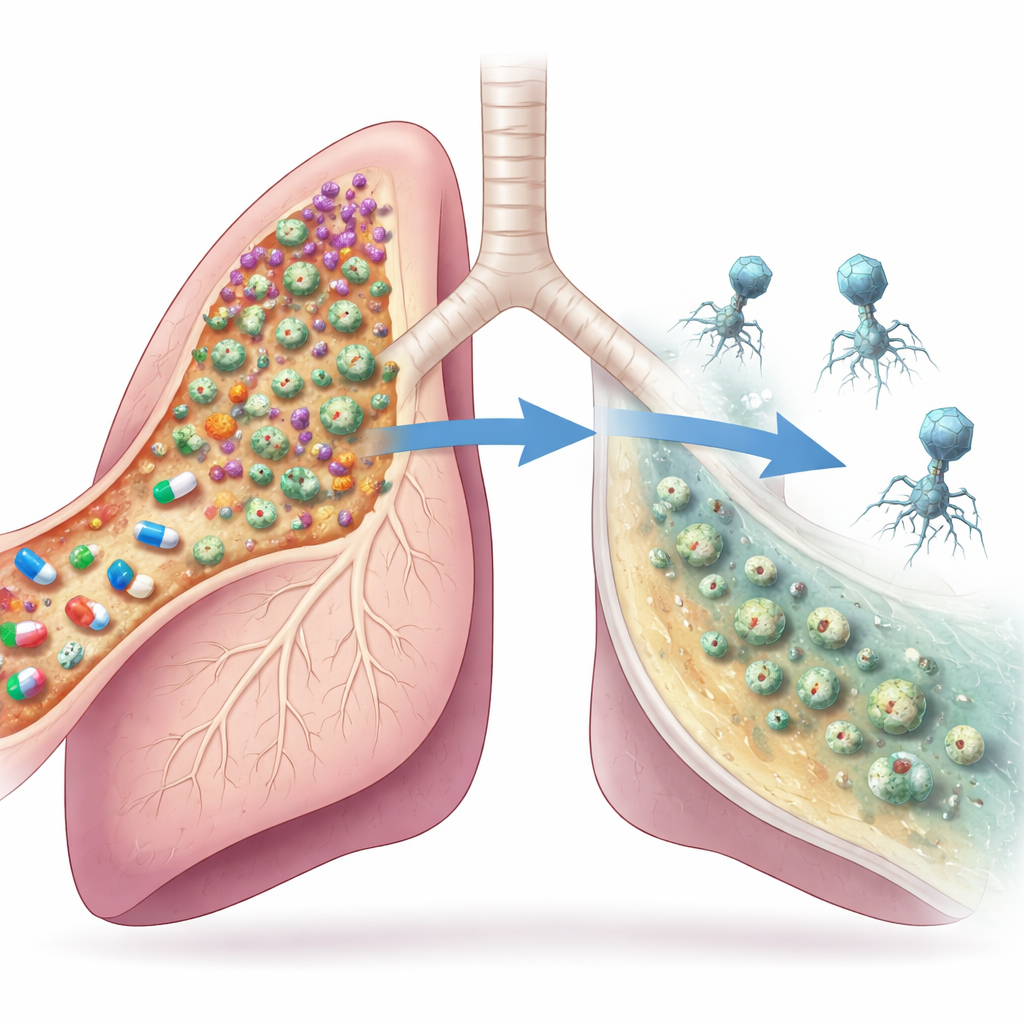
Virussen bundelen krachten met medicijnen
Om het evenwicht te kantelen, gaven clinici een intraveneus cocktail van twee fagen naast ciprofloxacine. Binnen enkele dagen verbeterde de longfunctie van de patiënt meer dan antibiotica alleen hadden bereikt, toonden thoraxbeelden schonere luchtwegen en nam de mate van luchtophoping in verschillende longregio’s af. Op microscopisch niveau steeg het totale aantal Pseudomonas‑cellen in het sputum eerst en daalde vervolgens meer dan tienvoud in de loop van een week. De samenstelling van de bacteriën verschuifde ook: de snelgroeiende, geneesmiddelresistente cellen stortten in, terwijl de slijmerige, minder virulente cellen opnieuw dominant werden op een lager totaalniveau. In plaats van elke bacterie uit te roeien, duwde de behandeling de infectie terug naar een stillere, chronische staat waar het lichaam van de patiënt mee kon leven.
Een verborgen touwtrekwedstrijd tussen fagen en immuniteit
De onderzoekers sequeerden ook viraal genetisch materiaal in het sputum om het lot van de twee therapeutische fagen te volgen. De ene faag floreerde vroeg, vermeerderde zich in de luchtwegen en volgde nauwgezet de instorting van de agressieve bacteriegroep. De andere kwam nauwelijks op gang. Bloedtests verklaarden waarom: de patiënt droeg al antistoffen die één faag herkenden en maakte snel meer, waardoor die faag vrijwel meteen geneutraliseerd werd. Antistoffen tegen de succesvollere faag verschenen later, nadat deze in de longen was geëxpandeerd, en stegen toen gestaag, waardoor ook diens activiteit uiteindelijk werd teruggedrongen. Gedurende deze periode bleven standaardmaatregelen van ontsteking acceptabel, wat laat zien dat de immuunreactie de faagactiviteit beperkte zonder schadelijke opflakkeringen te veroorzaken.
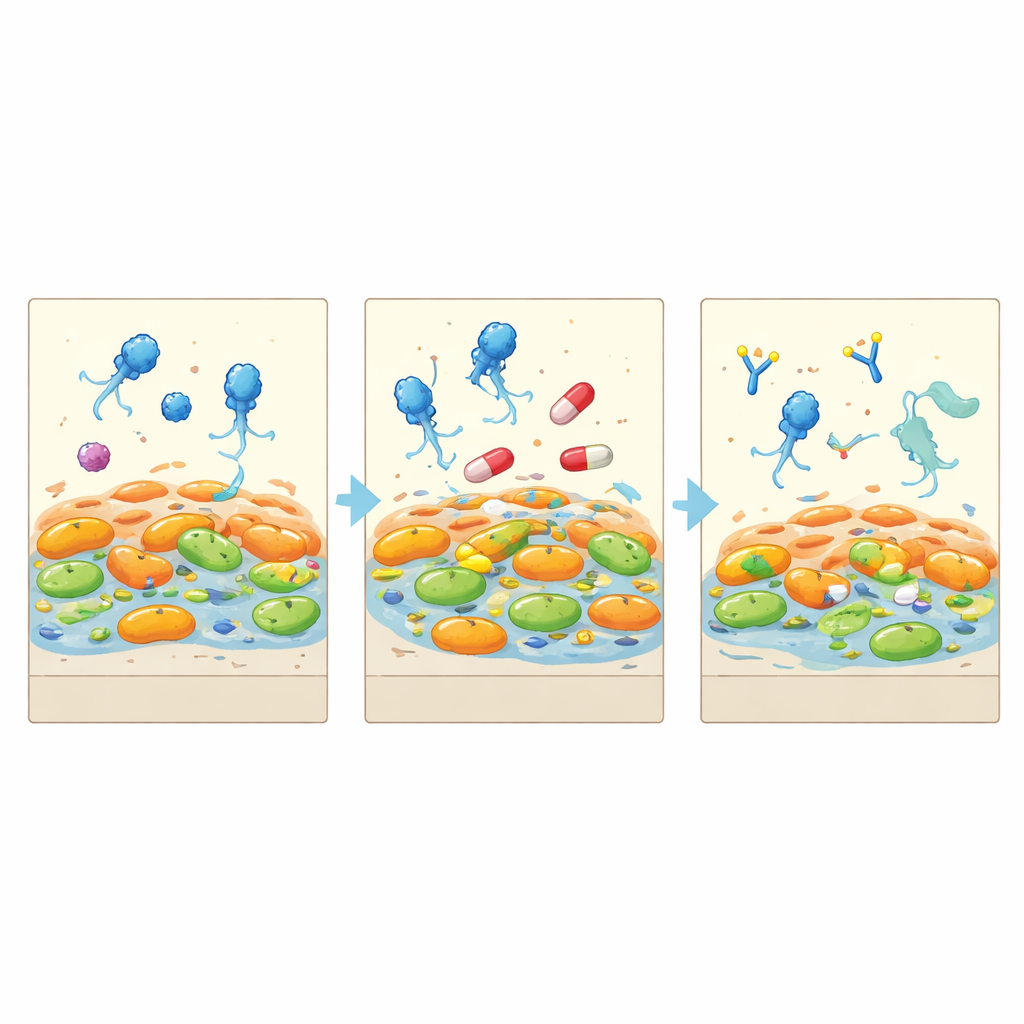
Hoe de bacteriën veranderden om te overleven
Door bacteriën voor, tijdens en na de therapie te isoleren en hun genomen te lezen, toonde het team aan dat de infectie voortkwam uit één langdurige Pseudomonas‑lijn die in meerdere takken was uiteengevallen. Onder faagaanval verdwenen sommige geneesmiddelresistente cellen volledig, terwijl anderen hun buitenste oppervlaktemoleculen herschikten om faaginvoer te blokkeren. Deze overlevers betaalden een prijs: ze groeiden 25–40 procent langzamer en vertoonden moleculaire tekenen van aanpassing aan stress in plaats van snelle expansie. Ondertussen volgden de slijmerige mucoïde bacteriën hun eigen evolutionaire koers, met aanscherping van pompmechanismen voor medicijnen en dikke coatings die ze van nature minder blootstelden aan fagen. Het eindresultaat was geen ‘superbug’‑overname maar een gemeenschap die naar tragere, minder schadelijke vormen was verschoven.
Een nieuw denkraam voor combinatiebehandeling
Over de klinische, microbiële en immuundata heen betogen de auteurs dat het herstel van de patiënt niet voortkwam uit simpele geneesmiddel–faag “super‑doding”. In plaats daarvan werkten antibiotica en fagen in verschillende hoeken van het infectielandschap. De chemische medicijnen snoeiden breed toegankelijke bacteriën terug en dempten ontsteking, terwijl fagen zich richtten op de verborgen, geneesmiddelresistente pockets die de uitbarsting aandreven. Toen antistoffen en bacteriële afweer toenamen, nam de faagactiviteit natuurlijk af, waardoor een geherstructureerde, lager‑risico gemeenschap overbleef die het immuunsysteem van de patiënt in toom kon houden. De auteurs noemen deze gecoördineerde maar niet strikt synergistische strategie “chemobiotherapie”: het samen gebruiken van chemische middelen en levende virussen om het infectie‑ecosysteem zodanig te hervormen dat blijvende controle, in plaats van totale uitroeiing, mogelijk wordt.
Wat dit betekent voor toekomstige zorg
Voor mensen met moeilijk behandelbare infecties, vooral bij cystische fibrose, suggereert dit geval dat fagen als echte biologische geneesmiddelen in het menselijke lichaam kunnen fungeren, zelfs wanneer ze via de bloedbaan worden toegediend en te maken hebben met immuunverdediging. Het benadrukt ook dat succes misschien minder afhangt van het wegvagen van elke microbe dan van het sturen van het hele systeem — bacteriën, virussen en gastheerimmuniteit — naar een stabielere, minder schadelijke configuratie. Als dit wordt bevestigd in grotere studies, kan dit op ecosysteem gebaseerde behandelingsperspectief sturen hoe we fagen timen en doseren naast antibiotica, en hoe we rekening houden met ieders bestaande virale bewoners en antistoflandschap bij het ontwerpen van gepersonaliseerde therapieën.
Bronvermelding: Luong, T., Kharrat, L., Champagne-Jorgensen, K. et al. Ecological partitioning enables phage–antibiotic cooperation in a human Pseudomonas infection. Nat Commun 17, 2615 (2026). https://doi.org/10.1038/s41467-026-69247-w
Trefwoorden: fagetherapie, cystische fibrose, Pseudomonas‑infectie, antibioticaresistentie, microbioom‑ecologie