Clear Sky Science · nl
Het ontkoppelen van fase-scheiding en fibrilisatie behoudt de activiteit van biomoleculaire condensaten
Waarom dit van belang is voor de gezondheid van de hersenen
Veel hersenaandoeningen, waaronder Alzheimer, betreffen eiwitten die in de loop van de tijd samenklonteren tot harde, vezelige verstrengelingen. Dezezelfde eiwitten kunnen ook zachtere, druppelachtige structuren vormen in cellen die helpen de chemie te organiseren, enigszins vergelijkbaar met kleine, vloeibare werkstations. Deze studie stelt een cruciale vraag: kunnen we het schadelijke verharden van deze druppels tot vezels stoppen zonder hun nuttige, dagelijkse functie te vernietigen? De auteurs laten zien dat een veelvoorkomend celmetaboliet, het aminozuur L-arginine, precies dat kan doen voor een sleutel-eiwit dat met Alzheimer wordt geassocieerd, genaamd Tau.
Van vrij zwevend eiwit naar kleine druppels
In cellen blijven bepaalde eiwitten niet altijd gelijkmatig gemengd in het vloeibare binnenmilieu. In plaats daarvan kunnen ze samenklonteren tot druppels, biomoleculaire condensaten genoemd, die zich gedragen als zeer zachte gels of stroperige vloeistoffen. Het team richtte zich op Tau, een eiwit dat normaal helpt bij de opbouw en stabilisatie van microtubuli—holle filamenten die fungeren als wegen binnen zenuwcellen. Tau is ook berucht omdat het amyloïde fibrillen vormt, de stugge vezels die voorkomen in de verstrengelingen die kenmerkend zijn voor veel neurodegeneratieve ziekten. Om te bestuderen hoe Tau-druppels in de tijd evolueren, ontwikkelden de onderzoekers een versie van het eiwit, SynTag-Tau genoemd, die actieve condensaten vormt die op een experimenteel handige tijdbaan verouderen tot amyloïde fibrillen, zonder agressieve toevoegingen.
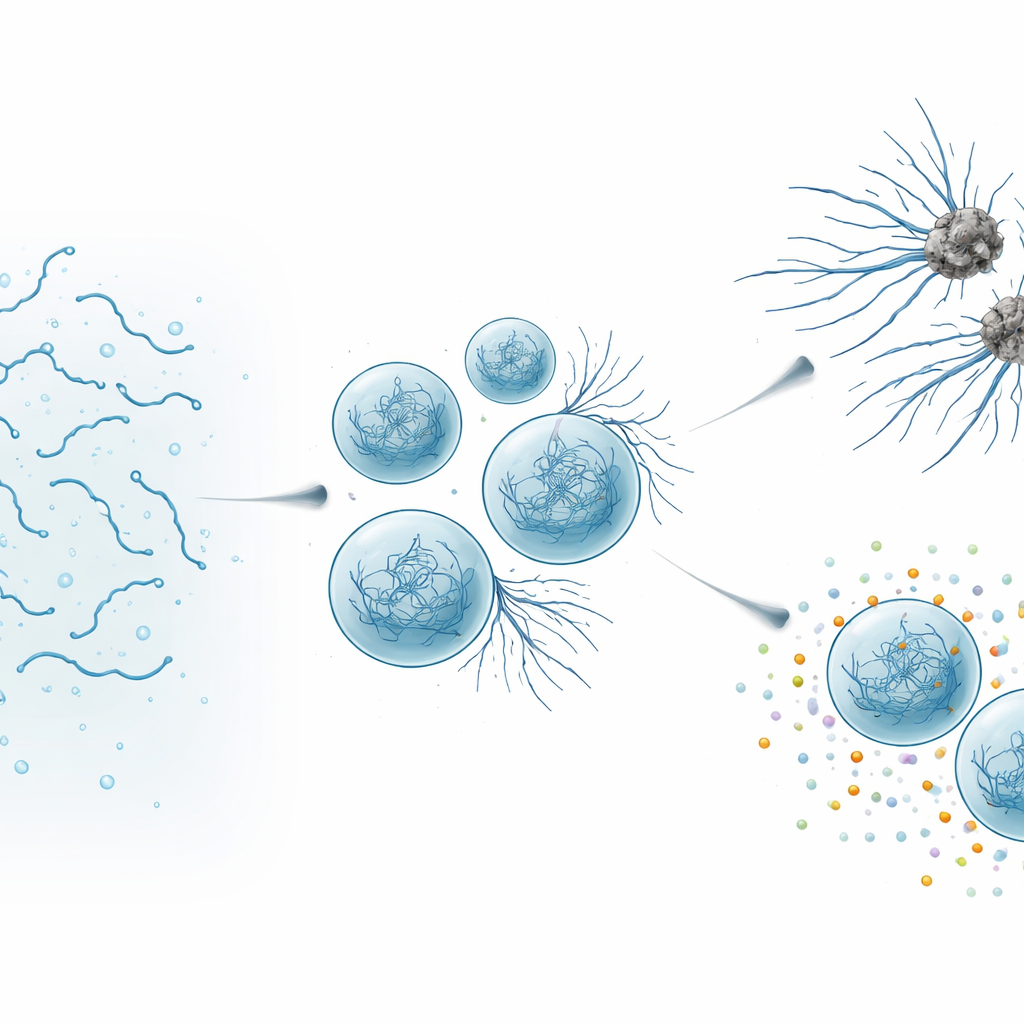
Wanneer nuttige druppels schadelijk worden
Met behulp van hoogresolutie-microscopie en biofysische metingen volgden de auteurs hoe SynTag-Tau-druppels veranderden over uren. Verse druppels gedroegen zich als vloeistoffen: ze fuseerden gemakkelijk, hun moleculen bewogen snel en er waren geen tekenen van geordende structuren. In de loop van de tijd vertraagden en verstijfden de druppels, en dunne vezels begonnen uit hun oppervlak te ontspruiten naar de omliggende oplossing. Gevoelige optische methoden toonden aan dat deze vezels de dicht opeengepakte “cross–beta” architectuur bevatten die typisch is voor amyloïde. Belangrijk was dat het grensvlak—de scheidslijn tussen de dichte druppel en het omringende vocht—als een brandpunt fungeerde waar fibrillen eerst verschenen. Terwijl druppels ouder werden en meer vezels uitsproten, leed Tau’s normale functie: de condensaten werden minder efficiënt in het aantrekken van tubuline, het bouwsteen van microtubuli, en verloren uiteindelijk hun vermogen om microtubuli-assemblage te ondersteunen.
Kleine moleculen die het evenwicht verschuiven
De onderzoekers vroegen vervolgens of eenvoudige metabolieten deze vloeistof-naar-vezel transitie konden vertragen of voorkomen terwijl de druppels zelf intact bleven. Bij het screenen van verschillende van nature voorkomende kleine moleculen vonden ze dat de positief geladen aminozuren L-arginine en L-lysine sterk de vorming van amyloïde fibrillen uit SynTag-Tau-druppels vertraagden of blokkeerden, maar de druppelvorming niet uitschakelden bij realistische, lage millimolaire concentraties. Ter vergelijking versnelden negatief geladen aminozuren zoals glutamaat en aspartaat de fibrilvorming, en algemene eiwitverstorende chemicaliën faalden of verstoorden de druppels zelf. Een fluorescent analoog van L-arginine toonde aan dat dit molecuul de voorkeur geeft om binnen Tau-condensaten te zitten in plaats van buiten, wat suggereert dat het werkt waar het het meest nodig is.
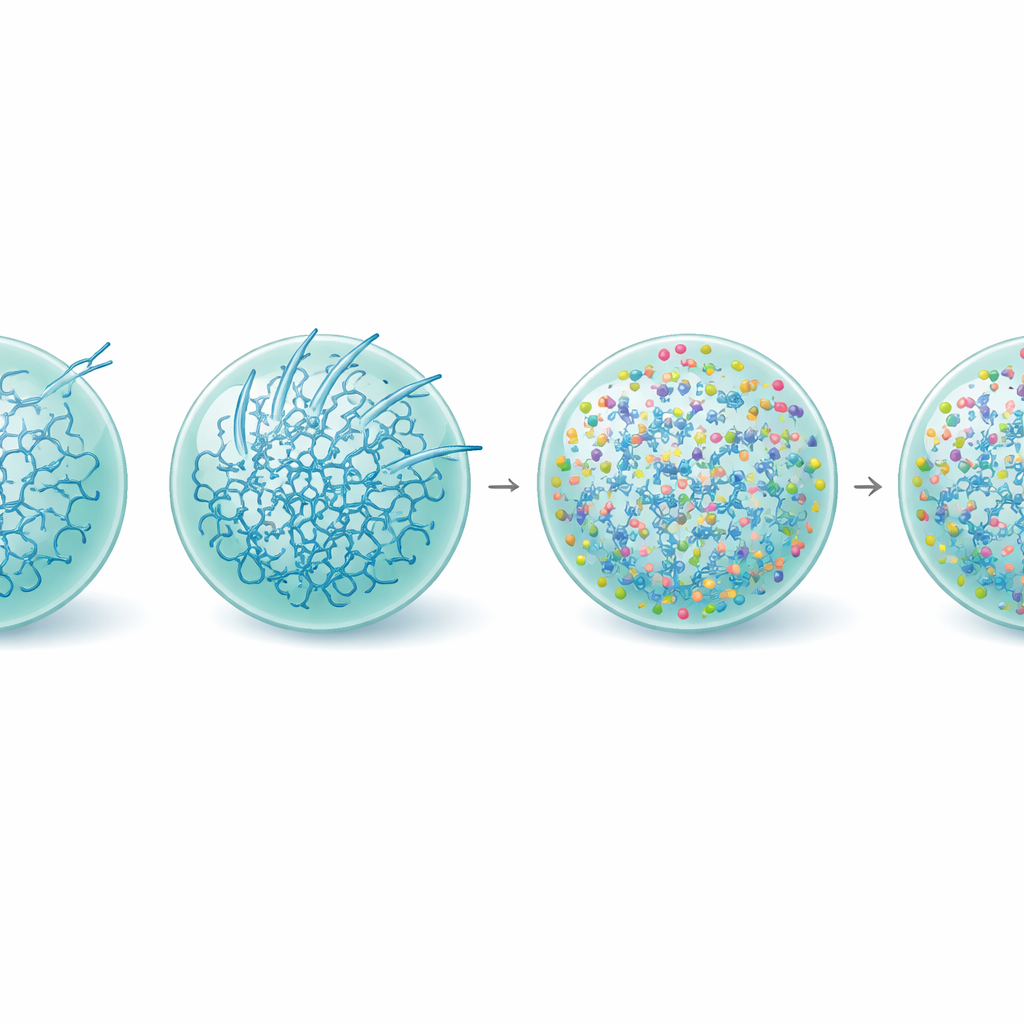
Verstijven van de druppel, functie behouden
Dieper gravend onderzochten de onderzoekers hoe L-arginine het innerlijke leven van Tau-druppels herschikt. Metingen van eiwitstructuur toonden aan dat, met L-arginine aanwezig, het aandeel Tau-moleculen dat de stijve, beta-rijke vormen aanneemt die met amyloïde geassocieerd zijn, verminderd was, zelfs in oudere druppels. Video-gebaseerde nanorheologie—het volgen van de beweging van piepkleine bolletjes binnen condensaten—liet zien dat L-arginine de Tau-druppels eigenlijk visco-elastischer maakte, wat betekent dat hun interne netwerk sterker en meer onderling verbonden werd terwijl het vloeibaar bleef. Deze versterking lijkt het systeem in een metastabiele, functionele toestand te houden en verhoogt de energetische barrière voor het vormen van fibrillen, met name aan het druppeloppervlak. In overeenstemming hiermee bleven L-arginine-behandelde condensaten tubuline gelijkmatig rekruteren en microtubuligroei ondersteunen lang nadat onbehandelde druppels inactief waren geworden.
Wat dit betekent voor toekomstige therapieën
Het werk toont aan dat de krachten die eiwitdruppelvorming aandrijven en die schadelijke vezelvorming bevorderen verwant maar scheidbaar zijn. Door de chemie binnen condensaten af te stemmen met een metaboliet zoals L-arginine, is het mogelijk de gunstige, vloeibare staat te behouden terwijl de overgang naar ziektegerelateerde amyloïde vezels wordt vertraagd of voorkomen. Hoewel deze studie een speciaal ontworpen Tau-systeem in vitro gebruikt, biedt het een bewijs van principe: kleine moleculen die selectief de stabiliteit van condensaten versterken, kunnen op een dag helpen cellen te beschermen tegen de geleidelijke ophoping van toxische eiwitaggregaten zonder de normale organiserende rollen van biomoleculaire condensaten te blokkeren.
Bronvermelding: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Trefwoorden: Tau-eiwit, biomoleculaire condensaten, amyloïde fibrillen, L-arginine, neurodegeneratie