Clear Sky Science · nl
Epilepsie-geassocieerde FOXJ3-varianten koppelen een transcriptieprogramma van de PTEN-mTOR-route aan neuronale specificatie en corticale laminatie
Wanneer de hersenbedrading licht uit de koers raakt
Epilepsie begint vaak in de kinderjaren, maar bij veel jonge patiënten zien artsen op hersenscans niets wat duidelijk mis is. Deze studie onderzoekt één verborgen oorzaak: kleine veranderingen in een gen genaamd FOXJ3 die op subtiele wijze bepalen hoe de buitenste laag van de hersenen, de cortex, wordt opgebouwd. Door de werking van dit gen te volgen in families met focale epilepsie en in zich ontwikkelende muizenhersenen, laten de onderzoekers zien hoe vroege misstappen in het ontstaan, de verplaatsing en de gelaagdheid van cellen uiteindelijk tot aanvallen kunnen leiden.
Een subtiele misvorming achter moeilijk behandelbare aanvallen
Veel kinderen met medicijnresistente focale epilepsie hebben een aandoening die focale corticale dysplasie (FCD) wordt genoemd, waarbij stukjes cortex misvormd zijn. Deze gebieden bevatten verplaatste en abnormaal grote zenuwcellen en zijn een veelvoorkomende reden waarom geneesmiddelen falen in het beheersen van aanvallen. Toch is de moleculaire oorzaak van FCD vaak onbekend en kan standaard-MRI kleine of oppervlakkige afwijkingen missen. De auteurs begonnen bij een familie waarin meerdere leden focale epilepsie en aanwijzingen voor FCD hadden. Zorgvuldige genoomanalyse wees op zeldzame veranderingen in FOXJ3, een gen dat eerder niet aan epilepsie werd gekoppeld. Extra gevallen uit grote genetische databanken lieten meer personen zien met ongewone FOXJ3-varianten en focale aanvallen, wat suggereert dat dit gen een herhaaldelijke rol kan spelen bij zulke aandoeningen.
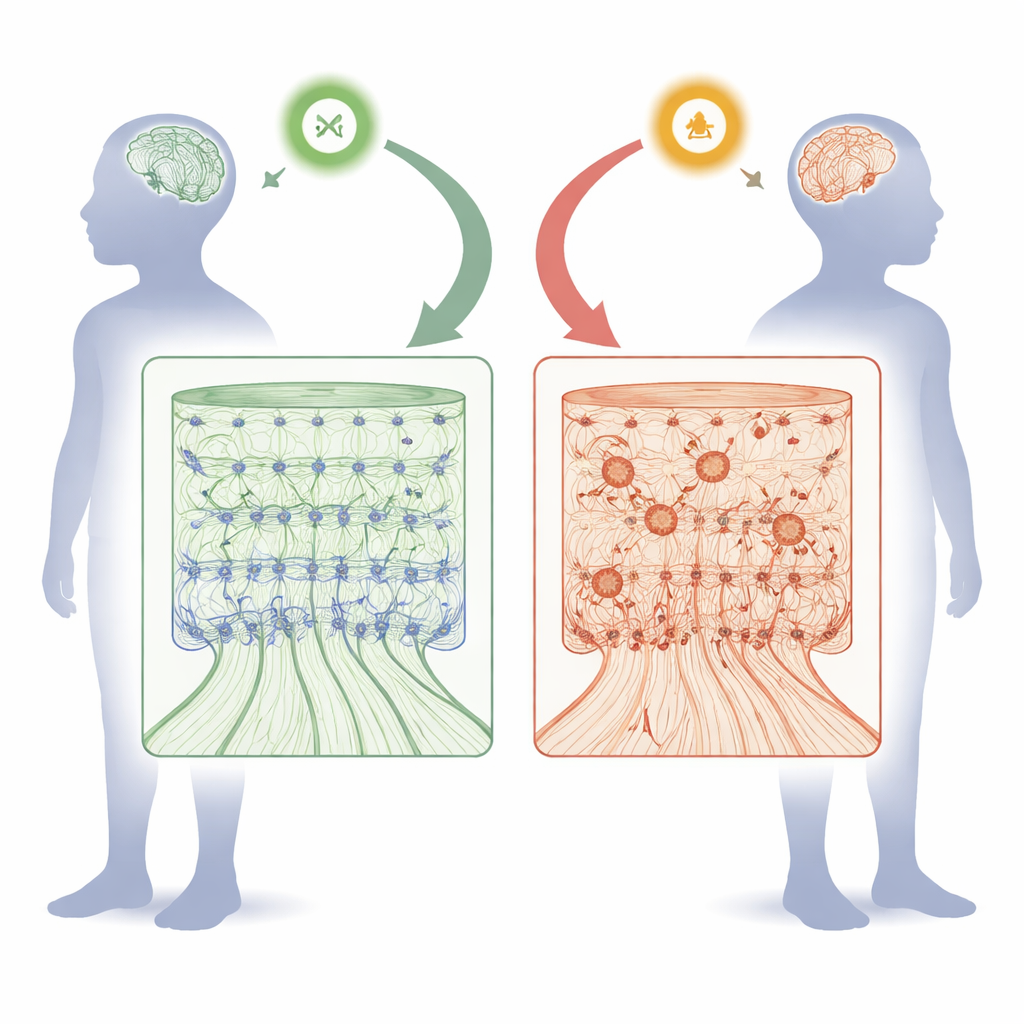
Hoe FOXJ3 helpt het denkoppervlak van de hersenen vorm te geven
Tijdens de foetale ontwikkeling wordt de cortex opgebouwd als een meerlagig gebouw. Stamachtige cellen die de binnenkant van de hersenen bekleden delen zich en sturen pasgeboren neuronen naar buiten langs radiale "steigers" om zes geordende lagen te vormen. Het team vond dat FOXJ3 actief is zowel in deze stamachtige voorlopercellen als in jonge neuronen, maar dat de activiteit in voorlopercellen van nature daalt na een specifiek tijdspunt in de midden-zwangerschap. Met genstillegingsinstrumenten in muizembrio’s verlaagden de onderzoekers Foxj3-niveaus op verschillende tijdstippen en observeerden wat er gebeurde. Vroeg verlies van Foxj3 veroorzaakte dat pasgeboren neuronen langzamer migreerden en in de verkeerde lagen terechtkwamen. Cellen die diepe-laagneuronen hadden moeten worden namen in plaats daarvan identiteiten aan die typerend zijn voor bovenste lagen, en callosale projectieneuronen, die de twee hersenhelften verbinden, werden in overmaat geproduceerd. Later in de ontwikkeling hadden het verminderen van Foxj3 veel mildere effecten, wat aantoont dat zijn rol sterk tijdsgebonden is.
Het in evenwicht houden van celdeling en groei
Om te begrijpen waarom FOXJ3 zoveel invloed heeft, combineerden de onderzoekers meerdere grootschalige benaderingen. Ze brachten in kaart waar FOXJ3 aan het DNA bindt en welke genen actief zijn in duizenden individuele corticale cellen. Dit wees sterk naar genen die de celcyclus en hersengroei beheersen, met name PTEN, een belangrijke rem op een groeipad dat bekendstaat als mTOR. In voorlopercellen bevorderde FOXJ3-binding de PTEN-activiteit, wat op zijn beurt hielp dat cellen de delingscyclus verlieten, zich tot neuronen transformeerden en ordelijk naar buiten migreerden. Wanneer Foxj3 werd gereduceerd, bleven meer voorlopercellen in een delende toestand, verlieten minder tijdig de cyclus en stokte de migratie in de intermediaire zones. Cruciaal was dat het herstellen van PTEN-niveaus in Foxj3-deficiënte hersenen grotendeels de migratie-, gelaagdheids- en celfate-problemen omkeerde, terwijl het versterken van een andere groeiregulator, TSC1, dat niet deed. Dit plaatst PTEN in het centrum van FOXJ3’s controle over de corticale bouw.
Van ontregelde routes naar vergrote neuronen
Het team vroeg zich vervolgens af hoe patiëntachtige FOXJ3-varianten zich gedragen. Een ziekte-geassocieerde versie van FOXJ3 faalde in het verhogen van PTEN-niveaus en liet de mTOR-route overactief worden, zoals zichtbaar aan verhoogde fosforylering van een sleuteleiwit gerelateerd aan groei. Bij adolescentie leken muizen die zo waren geconstrueerd dat ze deze gemuteerde vorm in de ontwikkelende cortex tot expressie brachten later opvallend gezwollen neuronen te hebben, met grotere cellichamen en omtrekken, wat de dysmorfe cellen bij menselijke FCD nabootst. Toch bereikte het gemuteerde eiwit nog steeds correct de kern, wat aangeeft dat het probleem ligt in defecte genregulatie en niet in mislokalisatie. Gezamenlijk koppelen deze bevindingen FOXJ3-mutaties aan een cascade van gebeurtenissen — minder PTEN, meer mTOR-signaal, vertraagde uitstroom uit de celcyclus, verstoorde migratie en hypertrofische neuronen — die het toneel kunnen vormen voor epileptische netwerken.
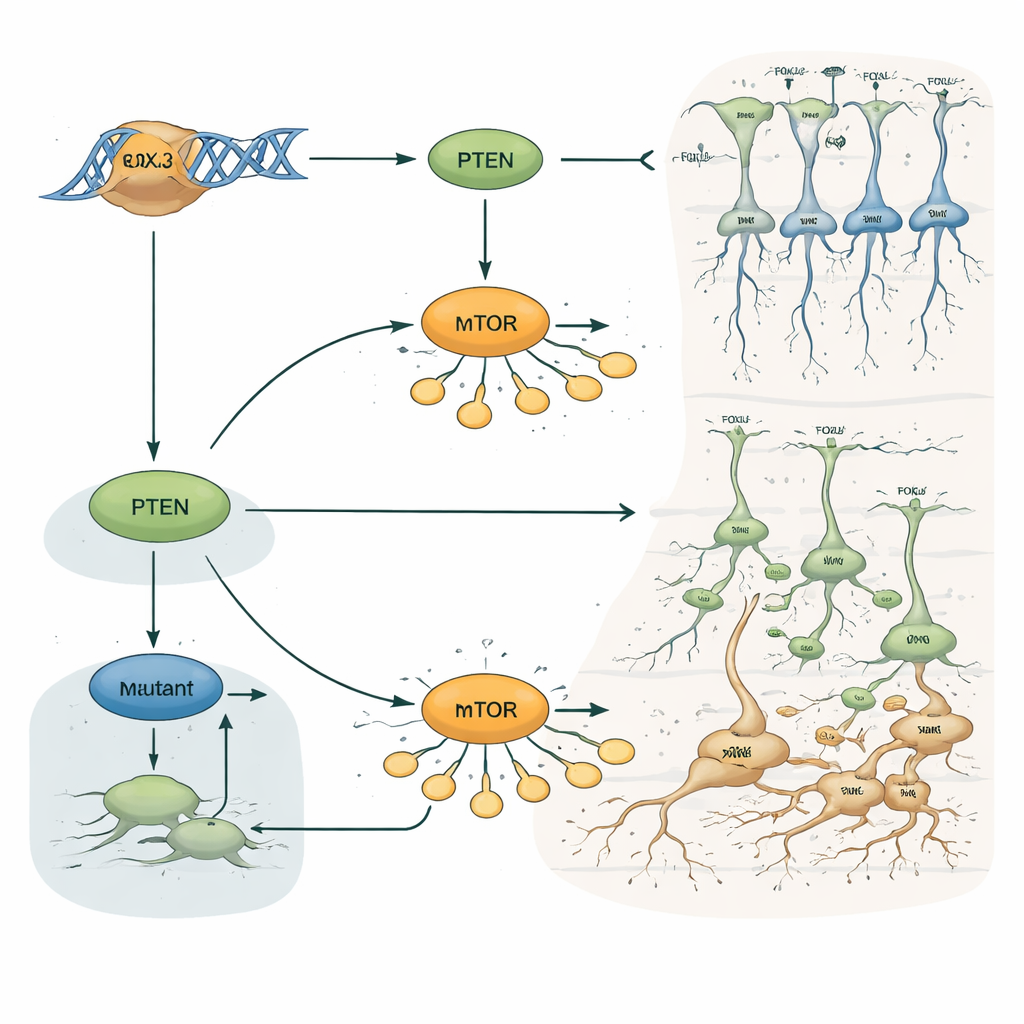
Waarom dit van belang is voor epilepsie en verborgen hersenlaesies
Voor niet-specialisten is de kernboodschap dat één transcriptiefactor, FOXJ3, helpt bepalen wanneer en waar corticale neuronen worden geboren, hoe ze zich verplaatsen en in welke laag ze uiteindelijk terechtkomen. Door te werken via de PTEN–mTOR-groeiroute houdt FOXJ3 de bouw van de hersenen op schema. Zeldzame veranderingen in dit gen kunnen dat evenwicht doen kantelen, waardoor kleine stukjes cortex abnormaal worden aangesloten en gelaagd, zelfs wanneer MRI-scans normaal lijken. Dit werk stelt FOXJ3 niet alleen voor als een nieuwe genetische oorzaak van focale corticale dysplasie en epilepsie, maar illustreert ook hoe subtiele verschuivingen in vroege hersenontwikkeling tientallen jaren later kunnen terugkeren als moeilijk behandelbare aanvallen.
Bronvermelding: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Trefwoorden: focale corticale dysplasie, FOHJ3-gen, PTEN mTOR-route, corticale ontwikkeling, focale epilepsie