Clear Sky Science · nl
Moleculaire basis van galactosylatie van collageen door GLT25D1
Hoe kleine suikertags helpen sterke weefsels op te bouwen
Collageen is het meest voorkomende eiwit in het lichaam en vormt het geraamte van huid, botten, bloedvaten en vele andere weefsels. Maar collageen werkt niet alleen: het moet op specifieke plaatsen worden voorzien van kleine suikermoleculen om de juiste sterkte en flexibiliteit te krijgen. Deze studie onthult, op atomaire schaal, hoe één sleutelenzym, GLT25D1, een specifiek suiker aan collageen bevestigt en hoe fouten in dit proces kunnen leiden tot kwetsbare bloedvaten, spierproblemen en mogelijk zelfs kanker.
Een nadere blik op collageen’s verborgen make-over
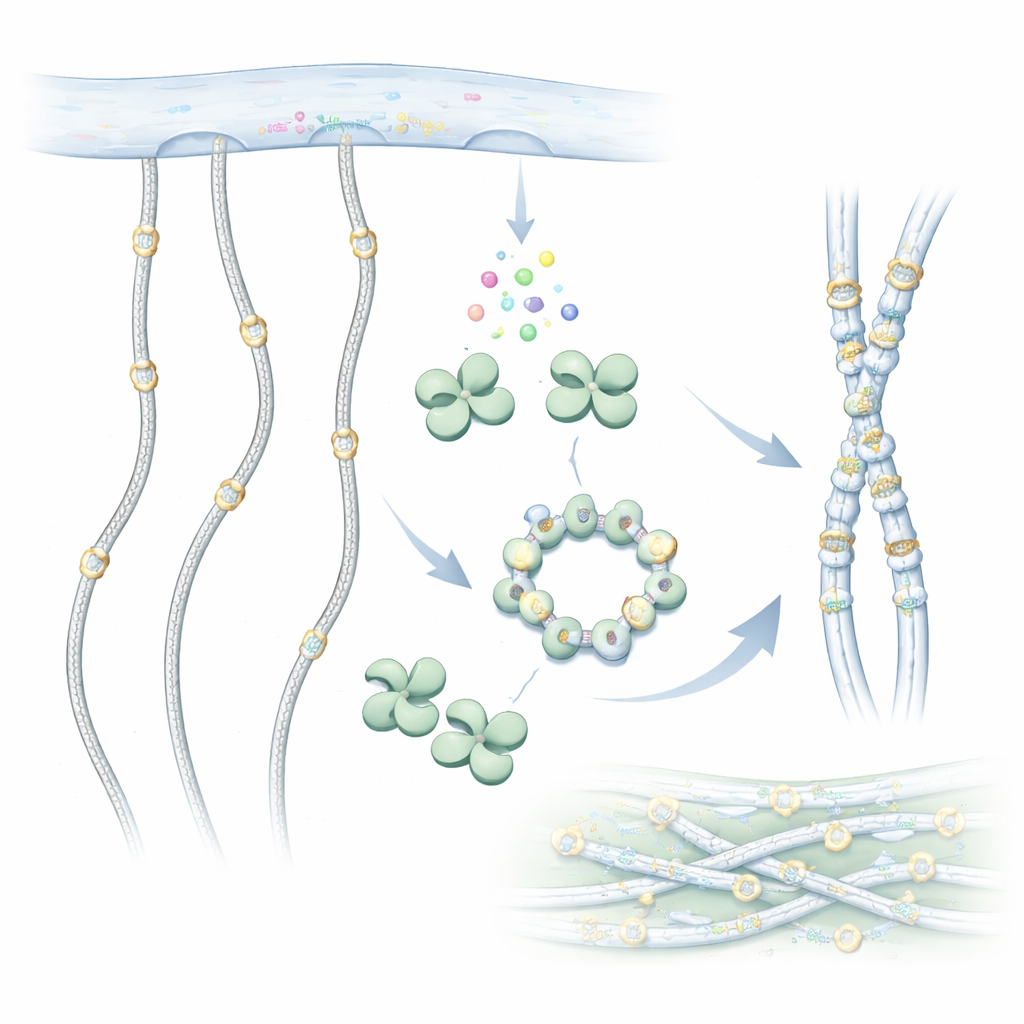
Collageenmoleculen zijn lange, touwachtige ketens die buiten de cel samen stevige vezels vormen. Voordat ze de cel echter verlaten, worden ze chemisch bewerkt. Eén belangrijke bewerking is de toevoeging van suikergroepen aan speciale bouwstenen, hydroxylysines, langs de collageenketen. GLT25D1 voert de eerste stap in deze suikertagging uit door een galactosesuiker van een donormolecuul over te dragen op hydroxylysine. Deze suikerdecoratie is geconserveerd van eenvoudige dieren tot mensen en helpt collageen correct te vouwen, te interageren met cellen en slijtage te weerstaan.
De vorm van een collageendecorator onthuld
Om te begrijpen hoe GLT25D1 werkt, gebruikten de onderzoekers cryo-elektronenmicroscopie om het menselijke enzym op bijna atomische resolutie in beeld te brengen. Ze ontdekten dat elk GLT25D1-molecuul twee vergelijkbare lobben heeft, beide verwant aan een veelvoorkomend enzymvouw die wordt gezien bij suikeroverdrachtseiwitten. Deze lobben koppelen samen tot langwerpige dimeren, en drie dimeren kunnen verder assembleren tot een hexameer in de vorm van een ring. In deze assemblages liggen de echte krachtcentra—de catalytische plekken—ver uit elkaar, een indeling die mogelijk toelaat dat meerdere suikertoevoegingsplaatsen tegelijk werken langs een uitgerekte collageenketen.
De werkende delen: waar suikeroverdracht echt plaatsvindt
Het team loste structuren op van GLT25D1 gebonden aan zowel zijn suikerdonor als een kort collageenachtig peptide dat hydroxylysine bevat. Dit tertiaire complex toonde aan dat alleen de tweede lob, genoemd het C‑terminale domein, daadwerkelijk de chemie uitvoert. Daar nestelt het donormolecuul in een pocket die gestabiliseerd wordt door een metaalion, terwijl het peptide in een smalle groef ligt die een specifiek lokaal patroon afdwingt: een hydroxylysine onmiddellijk gevolgd door een kleine glycine. Een enkele aspartaatresidu fungeert als chemische base en activeert de hydroxylgroep van hydroxylysine zodat deze het suiker kan aanvallen en de overdracht kan voltooien. Veranderingen in een van deze sleutelaminozuren verminderen of doen de activiteit drastisch teniet, wat hun essentiële rol bevestigt.
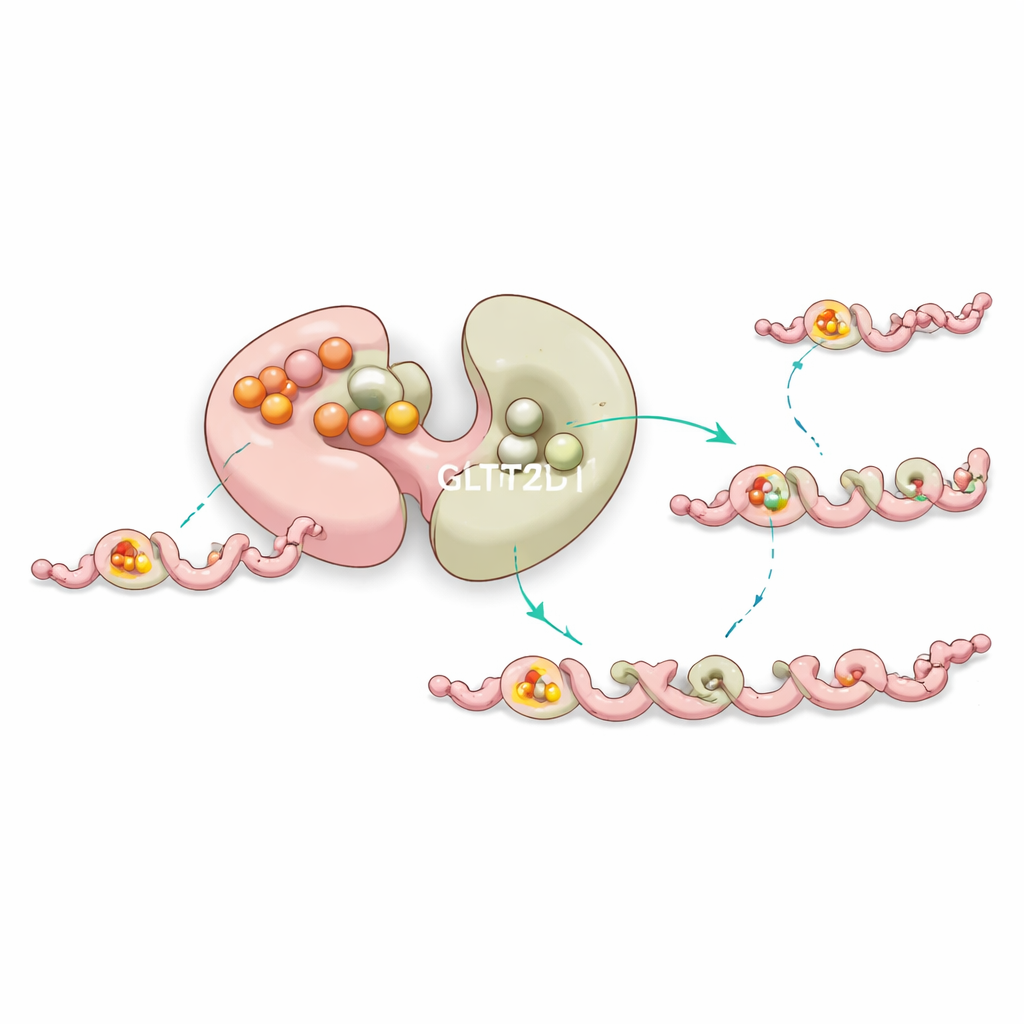
Een ingebouwde stabilisator en langafstandsturing
Vreemd genoeg bindt de eerste lob van GLT25D1 een suikerdonor zeer sterk maar voert niet de overdracht uit. In plaats daarvan suggereren experimenten en computersimulaties dat deze "stille" plek helpt het enzym te stabiliseren en het gedrag van de actieve lob subtiel af te stemmen via langafstandscommunicatie binnen het eiwit. Mutaties nabij deze niet-catalytische pocket destabiliseren het enzym vaak of verschuiven de efficiëntie, wat erop wijst dat de natuur deze extra bindingsplaats gebruikt als een vorm van interne kwaliteitscontrole om de collageenmodificatie soepel te laten verlopen.
Als de decorator faalt: verbanden met ziekte
Door mutaties afkomstig van patiënten op hun structureel model in kaart te brengen, konden de auteurs verklaren hoe fouten in GLT25D1 leiden tot menselijke ziekten. Sommige mutaties kappen de catalytische lob volledig af, andere destabiliseren de eiwitkern, en weer andere treffen precies de suiker- of collageenbindingsplaatsen. Deze fouten verminderen of elimineren de suikeradditie aan collageen en zijn in verband gebracht met kleine-vaatziekte van de hersenen, cognitieve problemen en spier- en skeletaandoeningen. Mutaties geassocieerd met kanker clusteren ook in cruciale regio’s, wat suggereert dat veranderde collageendecoratie de tumorgroei en -uitzaaiing kan beïnvloeden.
Waarom dit belangrijk is voor gezondheid en toekomstige behandelingen
Door een gedetailleerde driedimensionale blauwdruk van GLT25D1 in actie te schetsen, verklaart dit werk hoe precieze suikertags aan collageen worden toegevoegd en waarom deze stap zo belangrijk is voor de weefselintegriteit. Voor niet‑specialisten is de kernboodschap dat kleine chemische veranderingen op collageen grote effecten kunnen hebben op bloedvaten, botten en mogelijk het kankerrisico. De structurele kaart van GLT25D1 biedt nu een leidraad voor het diagnosticeren van schadelijke varianten en voor het ontwerpen van therapieën—of het nu kleine moleculen zijn die foutieve enzymen stabiliseren of gengebaseerde strategieën—die op termijn de defecte collageensuikertagging bij de bron zouden kunnen corrigeren.
Bronvermelding: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Trefwoorden: collageen-glycosylering, GLT25D1, extracellulaire matrix, vasculaire aandoening, cryo-EM-structuur