Clear Sky Science · nl
Lokale PI(4,5)P2-synthese door septine-geassocieerde PIPKIγ-isoformen regelt de associatie van centralspindlin met het midbody tijdens cytokinese
Hoe cellen het splitsen voltooien
Cytokinese — de laatste vernauwing die één cel in tweeën deelt — lijkt vanzelfsprekend, maar als dit proces misgaat kan het bijdragen aan kanker en andere ziekten. Deze studie onthult hoe een specifieke set moleculen fungeert als bouwplaatsvoorlieden bij de smalle brug die twee pasgeboren cellen verbindt, en ervoor zorgt dat de splitsing netjes wordt afgerond in plaats van terug te veren of vast te lopen.
De laatste brug tussen dochtercellen
Nadat een cel zijn genetisch materiaal heeft verdubbeld en de chromosomen heeft gescheiden, moet hij zich fysiek opsplitsen. Een contractiele ring van eiwitfilamenten trekt samen rond het midden van de cel en vormt een diepe groeve, het cleavegefurrow. Terwijl deze furrow naar binnen trekt, blijven de twee dochtercellen verbonden door een dunne intercellulaire brug met een dicht kerngebied, het midbody. Het midbody is een klein maar complex bouwwerk van gebundelde microtubuli, scaffold-eiwitten en signalerende lipiden; het fungeert zowel als verbindingspunt als controlecentrum dat de laatste stappen van deling en de uiteindelijke doorsnijding coördineert. 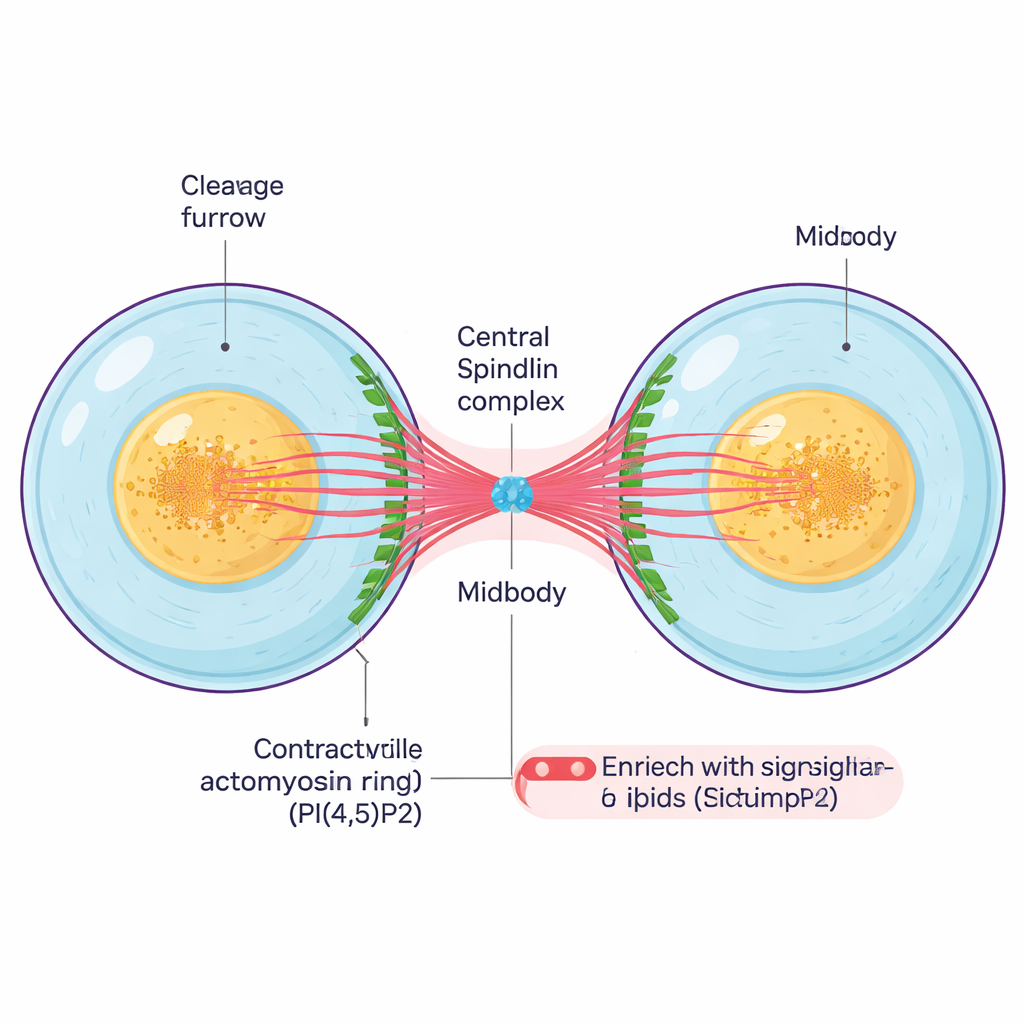
Een lipidesignaal dat op de juiste plaats moet zijn
Een belangrijke speler in dit proces is een signalerend vetmolecuul in het celmembraan, PI(4,5)P2. Dit lipide helpt vele eiwitten verankeren die de contractiele ring opbouwen en laten samentrekken en die de brug stabiliseren. De vraag is hoe cellen bepalen waar en wanneer PI(4,5)P2 verschijnt, aangezien het in het membraan kan diffusëren. De auteurs richtten zich op enzymen die type I PIP-kinasen heten en PI(4,5)P2 aanmaken, en in het bijzonder op één gen, PIPKIγ, dat in meerdere subtiel verschillende splicevarianten bestaat. Door elk van deze kinasen selectief te verminderen in menselijke cellen en de effecten met geavanceerde microscopie te observeren, ontdekten ze dat PIPKIγ een speciale rol speelt laat in de cytokinese, wanneer de brug en het midbody zich vormen, hoewel het niet sterk het totale PI(4,5)P2-niveau aan het celoppervlak verandert.
Septine-scaffolds rekruteren een gespecialiseerd enzym
Het team vond dat twee splice-versies van PIPKIγ, genoemd i3 en i5, als precisiegereedschap fungeren dat naar de juiste plek wordt gebracht door structurele eiwitten die septines heten. Septines vormen filamenten en ringen die helpen de brug vorm te geven en andere componenten te organiseren. Biochemische pull-downs en celbeeldvorming toonden aan dat PIPKIγ-i3 en PIPKIγ-i5 fysiek binden aan septinecomplexen en septinefilamenten bekleden, terwijl andere PIPKIγ-varianten dat niet doen. Wanneer de onderzoekers twee specifieke aminozuren in deze splice-inserts muteerden, konden de enzymen niet langer aan septines binden. In delende cellen verschuiven normale PIPKIγ-i3/i5 van een diffuse membraanlokalisatie naar concentraties in het cleavegefurrow en markeren vervolgens de intercellulaire brug en het midbody synchroon met septines en een ander scaffold-eiwit, anillin. Het verwijderen van alleen de i3- en i5-varianten verspreidde anillin en septines langs de brug weg van het midbody, en veel cellen faalden in cytokinese en eindigden met meerdere kernen.
Lokale lipideproductie verankert de delingsmachine
Om te testen of deze effecten afhankelijk waren van lokale PI(4,5)P2-productie, maten de auteurs PI(4,5)P2 rond het midbody en manipuleerden enzymen die dit lipide toevoegen of verwijderen. Het depletiveren van PIPKIγ-i3/i5 verminderde PI(4,5)P2 in het midbody, terwijl het blokkeren van een PI(4,5)P2-afbrekend enzym het tegenovergestelde effect had. Belangrijk was dat het herstellen van een normale, septine-bindende en katalytisch actieve PIPKIγ-splicevariant de juiste clustering van anillin en septines aan de brug herstelde, maar kinase-dode of septine-bindingsdeficiënte mutants deden dat niet. Met live-imaging en een expansion-microscopietechniek, die het preparaat fysiek opblaast om fijne details zichtbaar te maken, toonde het team aan dat zonder PIPKIγ-i3/i5 septines niet langer op brug-microtubuli migreren, de brug korter en minder gebundeld wordt, en een cruciaal complex genaamd centralspindlin er niet in slaagt nauw met het midbody geassocieerd te blijven. 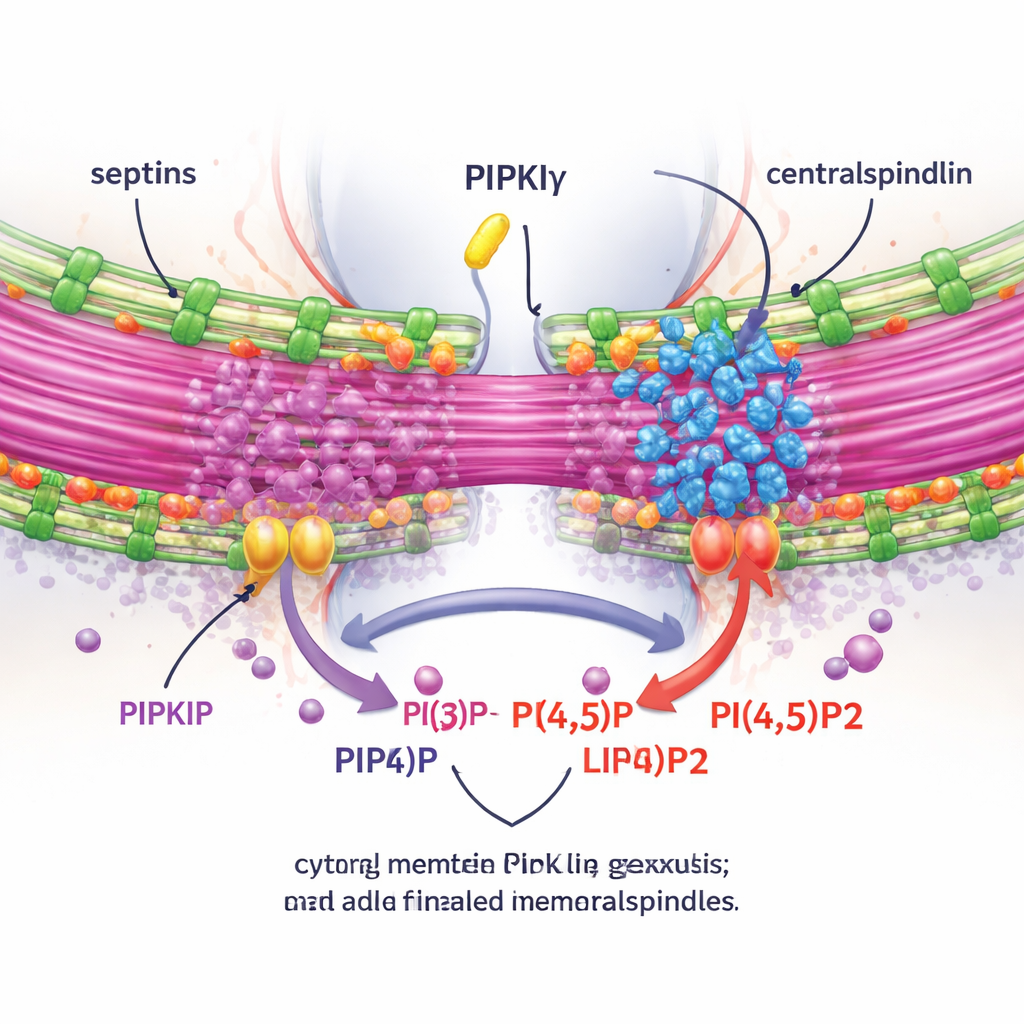
Een checkpoint bouwen voor een schone doorsnijding
Centralspindlin helpt de microtubuli van het midbody te koppelen aan het omringende membraan en reguleert kleine moleculaire schakelaars die de celsvorm aansturen. De studie vindt dat centralspindlin zowel met septines als met PIPKIγ associeert, en dat het verlies van beide partners de aanwezigheid ervan in het midbody op vergelijkbare wijze verzwakt. De auteurs stellen voor dat septines PIPKIγ-i3/i5 rekruteren naar het ingezakte furrow, waar deze enzymen een geconcentreerde patch van PI(4,5)P2 creëren. Deze lokale lipidepool stabiliseert op haar beurt anillin, centralspindlin en septines nabij het midbody, bevordert het bundelen en stabiliseren van brug-microtubuli, en laat de intercellulaire brug rijpen totdat de uiteindelijke abscissie kan plaatsvinden. Als dit systeem verstoord raakt, verschijnt PI(4,5)P2 op de verkeerde plekken, verspreiden scaffold-eiwitten zich, zijn microtubuli slecht gebundeld en faalt cytokinese vaak.
Waarom dit verder gaat dan fundamentele celbiologie
Door te laten zien hoe specifieke PIPKIγ-splicevarianten en septines samenwerken om een lokaal lipidesignaal in het midbody te genereren, legt dit werk uit hoe cellen ruimtelijke precisie verschaffen aan een sterk mobiel signaalmolecuul. Die precisie is cruciaal voor de veilige voltooiing van celdeling en helpt chromosoommis-segregatie en abnormale cel-aantallen te voorkomen die tumorontwikkeling kunnen bevorderen. Dezelfde midbody-structuren beïnvloeden ook de celfate en proliferatie na deling, dus inzicht in hun assemblage opent nieuwe wegen om te onderzoeken hoe fouten in deze nanoschaal-scaffolds kunnen bijdragen aan kanker en mogelijk de manipulatie van stamcellen.
Bronvermelding: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Trefwoorden: celdeling, cytokinese, signalerende lipiden, septines, kankerbiologie