Clear Sky Science · nl
Pan-RAF-remmer exarafenib richt zich op BRAF klasse II/III NSCLC en onthult ARAF-KSR1-resistentie en combinatiestrategieën
Waarom dit onderzoek van belang is voor longkankerpatiënten
De meeste mensen hebben wel gehoord van gerichte kankertherapieën die zich richten op specifieke genetische afwijkingen. Voor veel longkankerpatiënten, en in het bijzonder degenen met minder gebruikelijke mutaties in het gen BRAF, werken de huidige gerichte middelen echter vaak niet. Deze studie introduceert een nieuw experimenteel middel, exarafenib, ontworpen om een bredere reeks BRAF-gedreven tumoren aan te pakken, en legt uit hoe kankercellen proberen eraan te ontsnappen—waardoor combinatietherapieën naar voren komen die deze tumoren langer onder controle zouden kunnen houden.
Een verborgen meerderheid van over het hoofd geziene mutaties
De onderzoekers begonnen met een eenvoudige vraag: hoe vaak komen de verschillende typen BRAF-mutaties voor bij gevorderde kankers, en speciaal bij niet-kleincellige longkanker (NSCLC)? Met behulp van een zeer grote vloeibare-biopsiedatabase van meer dan 160.000 patiënten analyseerden ze tumor-DNA-fragmenten die in de bloedbaan circuleren. Ze vonden dat BRAF-mutaties bij longkanker in ongeveer 4–5% van de patiënten voorkomen, wat wereldwijd nog altijd neerkomt op vele duizenden mensen. Cruciaal is dat ongeveer twee derde van deze longtumoren zogenoemde klasse II- en klasse III-BRAF-mutaties droeg—typen die door de momenteel goedgekeurde BRAF-medicijnen niet effectief worden aangepakt. Patiënten met een van deze klassen, vooral klasse II, hadden doorgaans een kortere overleving dan degenen met de bekendere klasse I-mutatie, waarschijnlijk omdat klasse I-patiënten toegang hebben tot gevestigde gerichte therapieën terwijl klasse II/III-patiënten meestal chemotherapie of immunotherapie krijgen.
Een geneesmiddel van de volgende generatie dat de hele route target
BRAF maakt deel uit van een keten van eiwitten (de MAPK-route) die groeisignalen van het celoppervlak naar de kern doorgeeft. Veel bestaande BRAF-middelen zijn ontworpen om slechts één gemuteerde vorm te blokkeren en kunnen zelfs per ongeluk gerelateerde eiwitten in normale cellen stimuleren. Exarafenib is anders ontwikkeld: het is een “pan‑RAF”-remmer die meerdere RAF-familielidmuutanten (ARAF, BRAF en CRAF) in zowel enkelvoudige als gekoppelde vormen moet uitschakelen, terwijl het de meeste andere cellulaire enzymen spaart. In biochemische tests over honderden menselijke kinasen blokkeerde exarafenib sterk alle drie de RAF-eiwitten en had het weinig off-target effecten, wat wijst op een schoner veiligheidsprofiel dan eerdere pan‑RAF-verbindingen.
Krachtige effecten in modellen van moeilijk te behandelen tumoren
Het team testte exarafenib in een reeks kweeklijnen en muismodellen met verschillende BRAF- en RAS-mutaties, inclusief patiënt-afgeleide tumoren. In celkweken remde exarafenib de groei en schakelde het MAPK-signaaltransductie uit, niet alleen in klassieke BRAF V600E-kankercellen maar ook in cellen met klasse II- en klasse III-mutaties en in veel RAS-gemuteerde cellen waarvoor momenteel weinig gerichte opties bestaan. In muizen met longtumoren met deze afwijkingen krimpten of vertraagden de tumoren dosisafhankelijk bij behandeling met exarafenib, en er waren duidelijke verbanden tussen medicijnniveaus, remming van de route en tumorrepons. Vroege klinische gegevens van twee patiënten met gevorderde BRAF-gemuteerde longkanker—één met een zeldzame BRAF-fusie en een andere met een klasse II-puntmutatie—toonden gedeeltelijke responsen en betekenisvolle symptoomverlichting, wat de relevantie van het preklinische werk ondersteunt.
Hoe kanker leert het middel te omzeilen
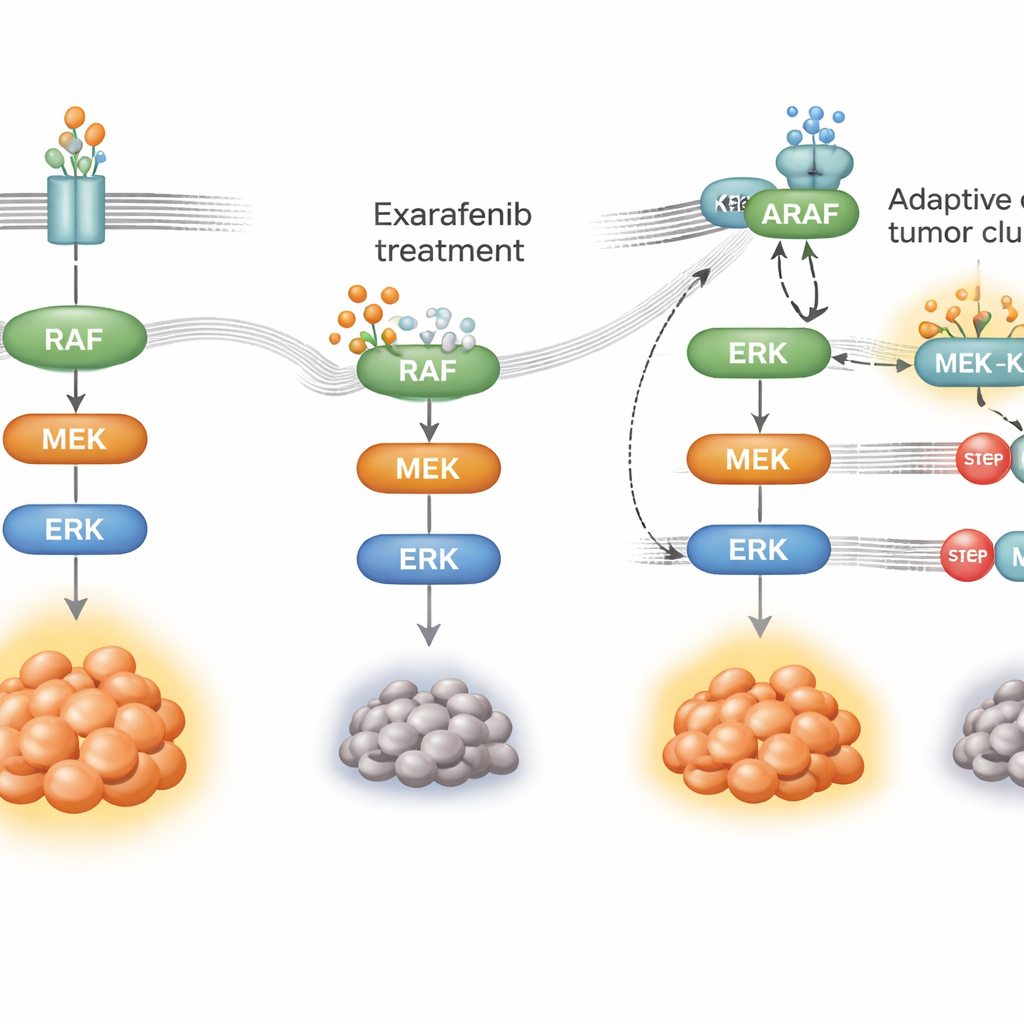
Geen enkele gerichte therapie werkt voor altijd; kankercellen passen zich aan. Om te onderzoeken hoe tumoren resistent zouden kunnen worden tegen exarafenib, zetten de onderzoekers BRAF-gemuteerde longkankercellen gedurende maanden bloot aan het middel totdat resistente populaties ontstonden. Deze cellen bleven afhankelijk van dezelfde groeiroute maar hadden de manier waarop ze die gebruikten herschikt. In plaats van vooral te vertrouwen op gemuteerde BRAF, verhoogden ze de activiteit van een upstream schakelaar genaamd RAS en schakelden ze over op het gebruik van een ander familielid, ARAF, samen met een scaffold-eiwit genaamd KSR1. Onder druk van het middel vormden ARAF en KSR1 sterke complexen die hielpen de MAPK-keten draaiende te houden, zelfs terwijl exarafenib gebonden was. Toen de wetenschappers ARAF of KSR1 selectief stillegden, of de RAS-activiteit verminderden, werden de resistente cellen opnieuw gevoelig voor exarafenib en stortten de overlevingssignalen in.
Combinatiestrategieën om resistentie voor te blijven
Met deze mechanistische kaart zocht het team naar partnermiddelen die de route op knelpunten konden blokkeren die zowel door de oorspronkelijke als de omzeilroutes worden gedeeld. Ze ontdekten dat het combineren van exarafenib met middelen die MEK of ERK remmen—belangrijke downstreamstappen in de MAPK-keten—sterke synergie gaf in veel cel- en muismodellen, inclusief tumoren die intrinsiek minder gevoelig waren of resistentie hadden verworven. Deze combinaties hielden de route langer gesloten, veroorzaakten meer celdood en werkten bij dieren vaak even goed of beter dan hogere doses exarafenib alleen, zonder duidelijke extra toxiciteit. Middelen die RAS direct targeten versterkten ook de effecten van exarafenib in modellen waarbij RAS duidelijk de resistentie dreef, wat een andere klinisch veelbelovende tactiek suggereert.
Wat dit betekent voor patiënten
Voor mensen met NSCLC die klasse II- of klasse III-BRAF-mutaties hebben—of complexe BRAF-fusies en RAS-co-mutaties—zijn er momenteel geen goedgekeurde gerichte therapieën en blijven de uitkomsten achter bij die van patiënten met meer voorkomende afwijkingen. Deze studie levert sterke wetenschappelijke argumenten dat exarafenib kan helpen die leemte te vullen door breed RAF-gedreven signalering uit te schakelen. Ook legt het uit hoe tumoren zich kunnen aanpassen via een ARAF‑KSR1-omweg en toont het aan dat het raken van de route op meerdere niveaus, vooral door RAF- en MEK-remmers te combineren of RAS-remmers toe te voegen, diepere en duurzamere tumorcontrole kan opleveren. Samen banen deze inzichten de weg naar klinische studies die gericht zijn op het brengen van op maat gemaakte combinatiegerichte therapieën naar een grote en eerder onderbediende groep longkankerpatiënten.
Bronvermelding: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Trefwoorden: BRAF-gemuteerde longkanker, pan-RAF-remmer, MAPK-signaaltransductie, medicijnresistentie, combinaties voor gerichte therapie