Clear Sky Science · nl
Erfelijke veranderingen in chromatinecontacten geassocieerd met transgenerationele vatbaarheid voor door dieet veroorzaakte insulinedisregulatie en obesitas
Wanneer het dieet van voorouders samenkomt met moderne tailleomvang
Waarom vallen sommige mensen gemakkelijker in gewicht toe en ontwikkelen ze sneller problemen met hun bloedsuiker dan anderen, zelfs wanneer hun eigen levensstijl gezond lijkt? Deze studie onderzoekt een verontrustende mogelijkheid: dat blootstelling aan bepaalde industriële chemicaliën tijdens de zwangerschap nazaten, generaties later, stilletjes kan "voorprogrammeren" om slecht te reageren op vette diëten. Werkend met muizen ontdekken de onderzoekers een manier waarop dit risico kan worden doorgegeven zonder de DNA-letters te veranderen, door te hervormen hoe het genoom zich vouwt binnen cellen.
Een chemische stof die een lange schaduw werpt
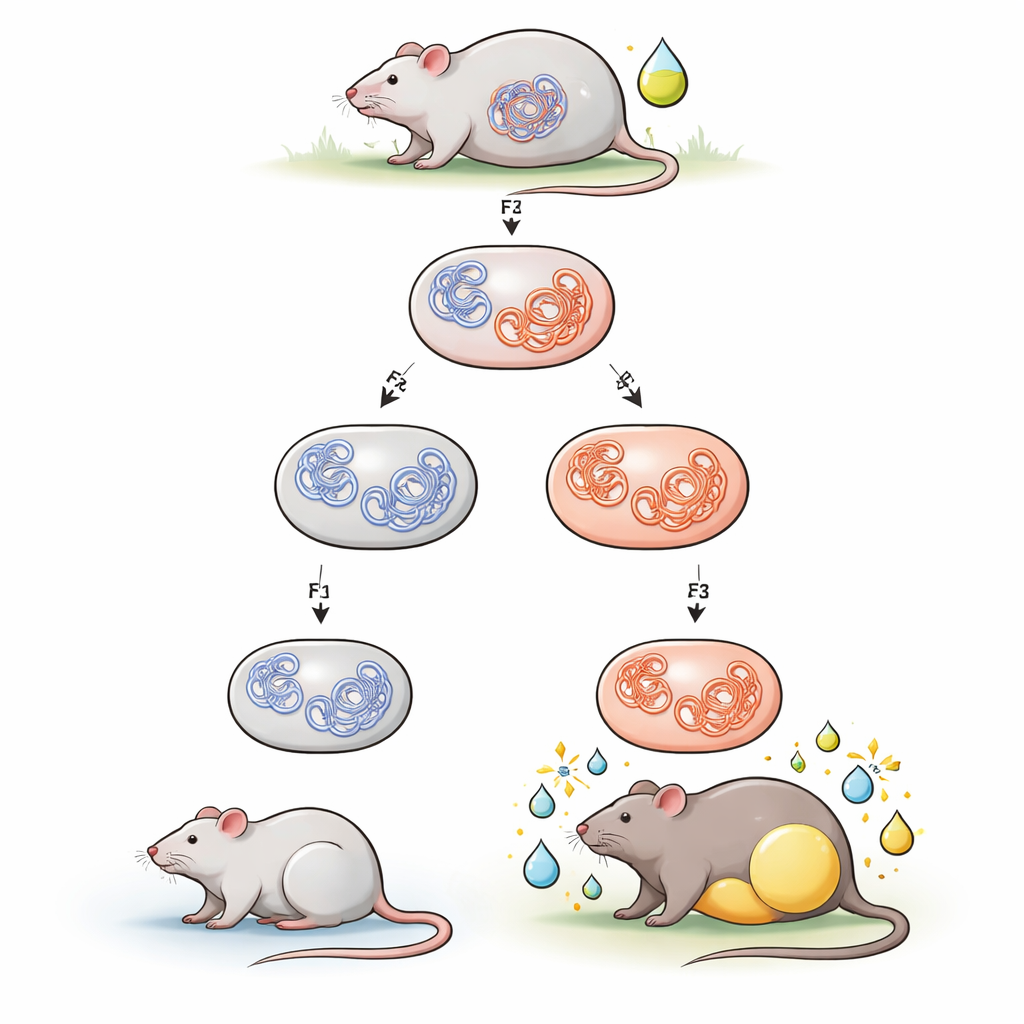
Het team richtte zich op tributyltin, een ooit veelgebruikt antifouling- en industrieel middel dat bekend staat als een obesogeen omdat het vetopslag bevordert. Draagmoedermuizen kregen lage doses tributyltin in hun drinkwater tijdens de zwangerschap. Hun nakomelingen (de eerste generatie) werden in de baarmoeder blootgesteld, hun kleinkinderen (tweede generatie) werden blootgesteld als zich ontwikkelende kiemcellen binnen die nakomelingen, en hun achterkleinkinderen (derde generatie) werden nooit direct blootgesteld. Toen jonge volwassen nakomelingen werden overgezet van standaardvoer naar een vetrijker dieet, kregen mannelijke nakomelingen van voorouders die tributyltin hadden ontmoet meer lichaamsvet en gewicht dan niet-blootgestelde controles. Vrouwtjes daarentegen vertoonden weinig of geen verandering. Deze mannelijke-specifieke neiging tot door dieet veroorzaakte obesitas weerspiegelde eerder werk van dezelfde groep.
Vouwen van het genoom als verborgen geheugen
Om te begrijpen hoe dit kenmerk kon worden geërfd zonder DNA-mutaties, onderzochten de onderzoekers primaire kiemcellen uit embryo's in de eerste drie generaties. Dit zijn de onrijpe cellen die uiteindelijk sperma en eicellen vormen. Met een techniek die in kaart brengt welke stukjes DNA elkaar in driedimensionale ruimte raken, zochten ze naar duurzame veranderingen in hoe chromosomen vouwen. Ze vonden dat het patroon van contacten in het algemeen vrij stabiel was. Echter, in mannelijke kiemcellen stak één klein gebied op chromosoom 19 bovenuit: een cluster van nieuwe, versterkte contacten verscheen en bleef bestaan van de direct blootgestelde embryo's tot twee niet-blootgestelde generaties. Dit gebied bevat het Ide-gen, dat het insuline-afbrekende enzym codeert, een sleutelproteïne die normaal helpt insuline uit de bloedbaan te verwijderen.
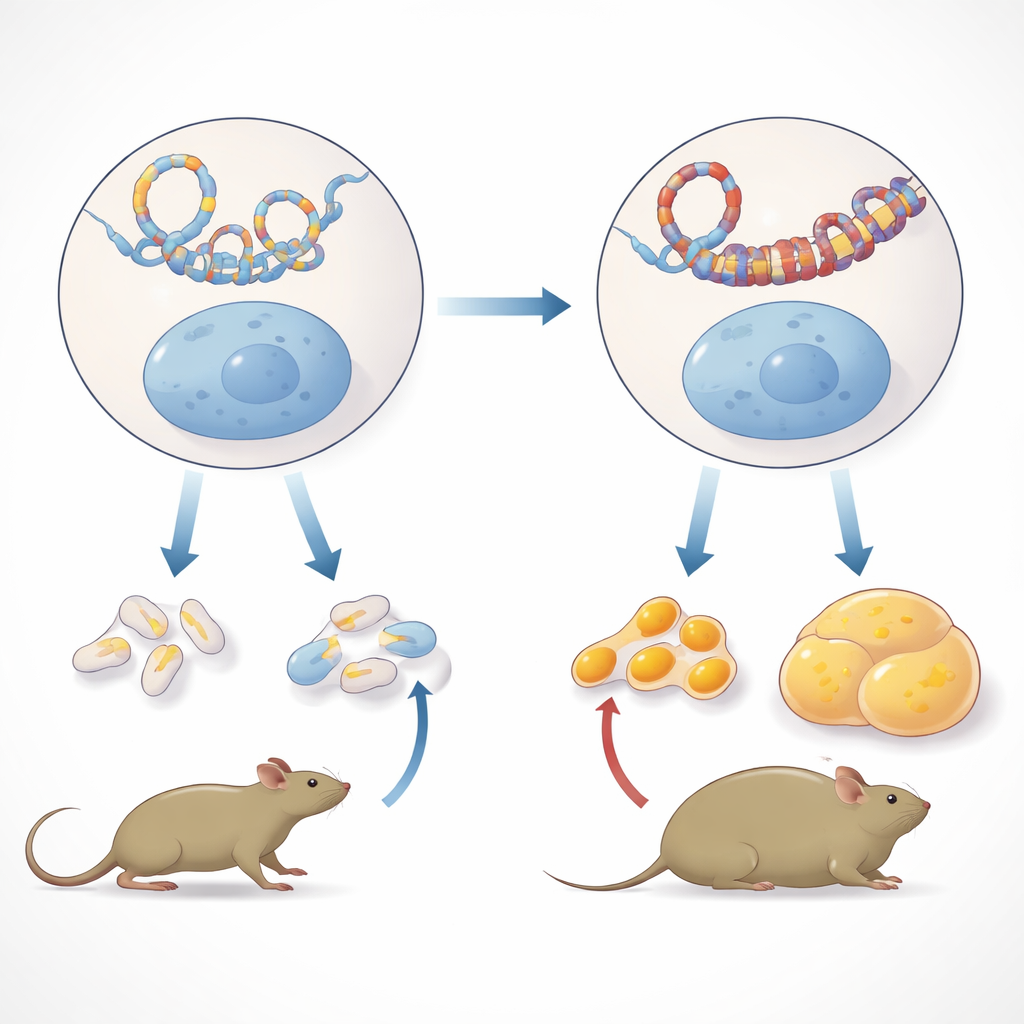
Een enkel gen in het hart van de metabolische verschuiving
Het team vroeg zich vervolgens af of deze gewijzigde DNA-contacten consequenties hadden in gewone lichaamstissues. In de lever van volwassen achterkleinzonen van de blootgestelde muizen zagen ze sterker binden van een genoom-organiserend eiwit genaamd CTCF op meerdere sites binnen het Ide-gebied, wat consistent is met de vorming van een nieuwe chromatinerlus. Tegelijkertijd daalde Ide-activiteit in mannelijke lever, terwijl nabijgelegen genen Hhex en Kif11 actiever werden. Het patroon verscheen niet in vrouwelijke lever of in andere mannelijke weefsels zoals spier, vetkussentjes, hersenen of milt, wat het weefsel- en seksspecifieke karakter benadrukt. Belangrijk is dat de auteurs een eenvoudige structurele duplicatie van dit deel van het chromosoom als verklaring uitsloten, door aan te tonen dat het kopieaantal van het Ide-gebied niet verschildde tussen blootgestelde en controlelijnen.
Van veranderde insulineclearance naar obesitas
Aangezien het insuline-afbrekende enzym helpt insuline uit de circulatie te verwijderen, zou verminderde Ide-activiteit meer insuline in het bloed achterlaten. Dat is precies wat de onderzoekers zagen. Zelfs vóór het vette dieet hadden mannelijke nakomelingen van tributyltin-blootgestelde moeders verhoogde insulinespiegels en hogere scores op een standaardindex van insulineresistentie, ondanks normale nuchtere bloedsuiker. Na weken op een rijker dieet ontwikkelden ze zowel hoge bloedsuiker als hoge insuline, samen met grotere vetreserves en verhoogd leptine, een hormoon dat gekoppeld is aan lichaamsvet. De niveaus van C-peptide, dat bijhoudt hoeveel insuline wordt geproduceerd, stegen vergelijkbaar bij blootgestelde en controledieren. Het cruciale verschil was de verhouding C-peptide tot insuline, die wees op verminderde afbraak van insuline in plaats van extra secretie — consistent met de waargenomen daling van hepatische Ide.
Wat dit betekent voor overerving en gezondheid
Gezamenlijk schetsen de bevindingen een keten van gebeurtenissen: ancestrale blootstelling aan een obesogene chemische stof hervormt subtiel hoe een specifiek deel van het genoom vouwt in mannelijke kiemcellen; deze nieuwe 3D-structuur wordt gereconstrueerd in de lever van mannelijke nakomelingen, waardoor één insuline-ruimende gen wordt teruggeschroefd; daardoor hebben deze dieren chronisch hogere insulinespiegels en zijn ze voorgeprogrammeerd om vet aan te zetten en bloedsuikerproblemen te ontwikkelen wanneer ze worden uitgedaagd met een vetrijk dieet. Voor een lekenlezer is de kernboodschap dat wat voorouders in hun omgeving tegenkomen, een fysieke "herinnering" kan achterlaten in hoe DNA is verpakt — niet door de genetische code te veranderen, maar door de vorm ervan te veranderen. Die herinnering kan stilletjes beïnvloeden hoe latere generaties reageren op moderne diëten, en onderstreept het belang van het beperken van schadelijke blootstellingen lang voordat gezondheidsproblemen zichtbaar worden.
Bronvermelding: Chang, R.C., Egusquiza, R.J., Amato, A.A. et al. Heritable changes in chromatin contacts associated with transgenerational susceptibility to diet-induced insulin dysregulation and obesity. Nat Commun 17, 2662 (2026). https://doi.org/10.1038/s41467-026-69214-5
Trefwoorden: transgenerationele epigenetica, obesogenen, insulineresistentie, chromatine-structuur, milieu-expositie