Clear Sky Science · nl
Een cytochroom P450-enzym herontwerpen als peroxygenase voor selectieve hydroxylatie van steroïden
Medicijnen maken van moeilijk te verfijnen moleculen
Steroïde geneesmiddelen — van ontstekingsremmende pillen tot hormoontherapieën — behoren tot de meest gebruikte medicijnen ter wereld. Toch is het fijnstemmen van deze moleculen, door precies één zuurstofatoom op de juiste plek toe te voegen, berucht lastig met klassieke chemie. Deze studie laat zien hoe onderzoekers een natuurlijk enzym zo herontworpen hebben dat het steroïden precies kan "polijsten" met eenvoudig waterstofperoxide, wat mogelijk groenere en goedkopere routes naar belangrijke geneesmiddelen oplevert.
Waarom steroïden zo moeilijk aan te passen zijn
Steroïden bestaan uit een compacte stapeling van koolstofringen, met veel vrijwel identieke koolstof–waterstofbindingen. Conventionele chemische methoden hebben moeite om precies één van deze bindingen aan te pakken zonder de andere te raken; ze vereisen vaak agressieve reagentia, hoge temperaturen en meerdere beschermingsstappen die afval genereren. Toch kunnen kleine veranderingen — zoals het toevoegen van een enkele hydroxylgroep (een –OH) op één specifieke positie — dramatisch beïnvloeden hoe een steroïde in het lichaam werkt. Enzymen uit de cytochroom P450-familie zijn de natuurkundigen voor dit soort precieze C–H-activatie, maar in hun natuurlijke vorm hebben ze meestal dure hulpstoffen en zuurstofverwerkende machinerie nodig, wat hun directe inzet in de industrie beperkt.
Een veelbelovend startenzym vinden
Met genome mining identificeerden de onderzoekers een zelfvoorzienend P450-enzym, P450stri, uit een bodem-bacterie. In tegenstelling tot de klassieke werkpaard-enzym P450BM3, dat voorkeur heeft voor kleine vetzuren, accepteert P450stri van nature volumineuze steroïden zoals testosteron. Onder zijn native omstandigheden, aangedreven door de cellulaire cofactor NADH, introduceert P450stri hydroxylgroepen op drie posities van testosteron en levert zo een mengsel van producten. Dit ingebouwde vermogen om steroïden te herkennen maakte P450stri tot een aantrekkelijke "startscaffold" voor het ontwerpen van een selectiever, industrievriendelijk katalysator.
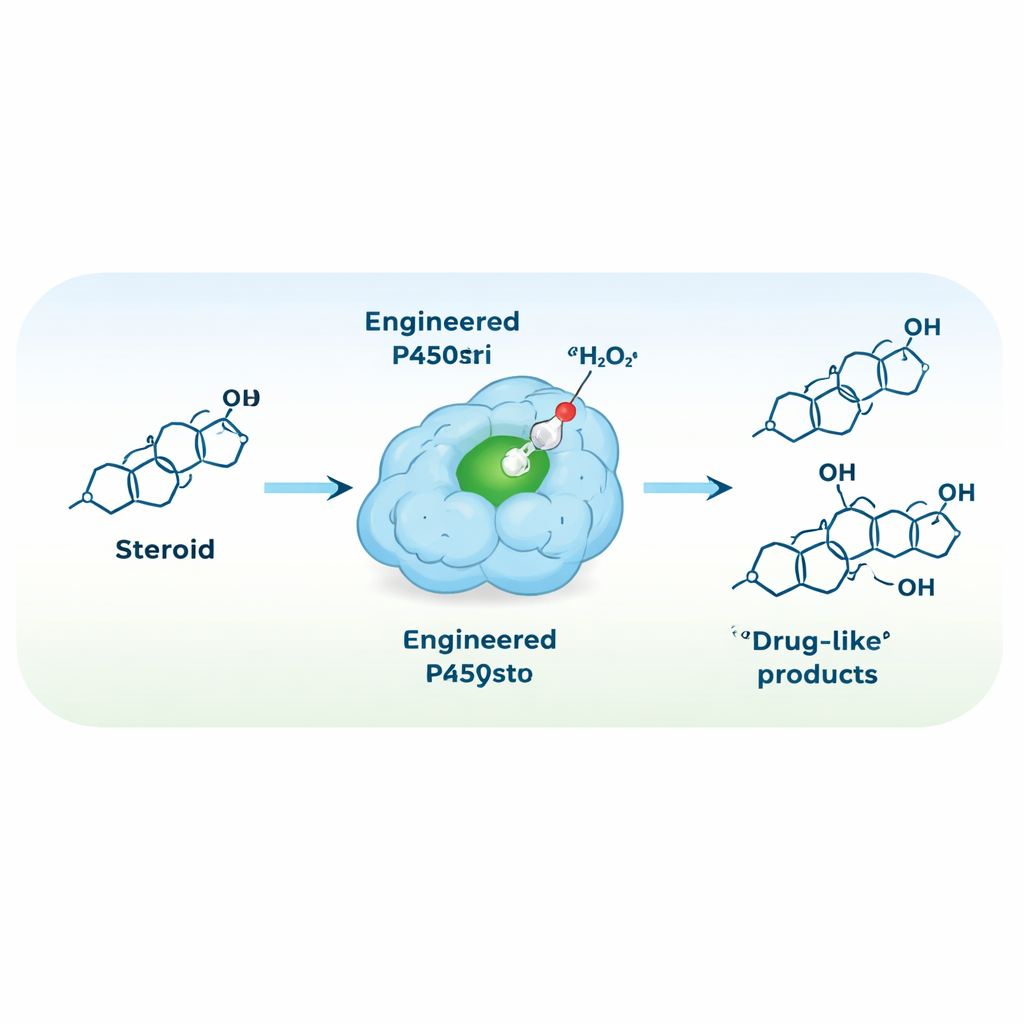
Het enzym herbedraden om op waterstofperoxide te draaien
Om de reactiestel te vereenvoudigen, streefde het team ernaar P450stri om te zetten in een peroxygenase — een enzym dat direct waterstofperoxide als oxidant gebruikt en daarmee de noodzaak voor kostbare cofactoren en hulpproteïnen wegneemt. Een enkele strategische mutatie, waarbij een volumineuze fenylalanine net boven het heemcentrum werd vervangen door een kleinere alanine, creëerde een variant genaamd M1. Deze wijziging opende ruimte rond het reactieve ijzercentrum en maakte het enzym verrassend zowel verdraagzamer voor hoge concentraties waterstofperoxide als veel selectiever. In de nieuwe, peroxide-gedreven modus zette M1 testosteron voornamelijk om in één product, gehydroxyleerd op de 15β-positie, met ongeveer 94% selectiviteit — vergeleken met 35% in het oorspronkelijke enzym.
Een "Ronde Kolk"-model voor slimmer enzymontwerp
Om de prestaties verder te verbeteren, introduceerden de auteurs een ontwerpopvatting die zij het "Ronde Kolk"-model noemen. Ze behandelen de actieve site waar de chemie plaatsvindt als de afgeronde bodem en de smalle toegangstunnels als de hals en dop. De bodem bepaalt welke positie op het steroïde wordt gemodificeerd, terwijl de hals regelt hoe gemakkelijk het steroïde en het waterstofperoxide het reactieve centrum bereiken. Geleid door computersimulaties en tunnel-mapping software, stelden ze systematisch een kleine set aminozuren die de tunnels bekleden bij, en pasten hun grootte en hydrofoobiteit aan. Deze tweedimensionale strategie leverde een opvallende variant op, M4, die hoge 15β-selectiviteit behield terwijl hij de reactiesnelheid sterk verhoogde en tolerant bleef voor waterstofperoxideconcentraties tot enkele honderden millimolair.
Van laboratoriumbank naar schaalbare steroïde-upgrades
Het ontworpen M4-enzym werd vervolgens getest in grotere schaalreacties met testosteron en een verwant steroïde dat in prestatiebevorderende contexten wordt gebruikt. In eenvoudige waterige mengsels bij kamertemperatuur, uitsluitend aangedreven door waterstofperoxide, zette M4 meer dan 90% van het beginmateriaal om en leverde geïsoleerde 15β-gehydroxyleerde producten in opbrengsten rond 75–80%. Deze omstandigheden zijn veel milder en schoner dan typische chemische routes. Tot slot toonden de onderzoekers aan dat door de sleutelmutaties over te brengen op meerdere verwante P450-enzymen in dezelfde evolutionaire "tak", ze deze betrouwbaar in vergelijkbaar selectieve en efficiënte peroxygenases konden veranderen, wat de generaliteit van hun ontwerpregels benadrukt.
Wat dit betekent voor toekomstige geneesmiddelen
Voor de niet-specialist komt het erop neer dat de onderzoekers een natuurlijk enzym hebben geleerd te werken als een uiterst precies, peroxide-aangedreven "microfabriekje" voor het modificeren van steroïde geneesmiddelen. Door een eenvoudig conceptueel model te combineren met gerichte mutaties, creëerden ze een enzym dat onder zachte en schaalbare omstandigheden een OH-groep precies op de juiste plaats kan toevoegen, en ze pasten deze strategie toe op verwante eiwitten. Deze aanpak kan de productie van bestaande steroïden stroomlijnen, routes openen naar nieuwe geneesmiddelkandidaten en dienen als blauwdruk voor het ontwerpen van andere enzymen die hardnekkige C–H-bindingen in complexe moleculen schoon activeren.
Bronvermelding: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Trefwoorden: steroïde biokatalyse, cytochroom P450-engineering, peroxygenase, waterstofperoxide-katalyse, selectieve hydroxylatie