Clear Sky Science · nl
Sequentiële ketenkoppeling over hiërarchische click‑sites maakt zeer selectieve ureum‑elektrosynthese mogelijk
Afval omzetten in plantenvoeding
Ureum als meststof voedt gewassen wereldwijd, maar de traditionele productie verbrandt enorme hoeveelheden fossiele brandstoffen en stoot grote hoeveelheden kooldioxide uit. Deze studie verkent een ander pad: met elektriciteit — bij voorkeur uit hernieuwbare bronnen — koolstof en stikstof uit afvalgassen en vervuild water samenvoegen tot nieuwe ureummoleculen. Geïnspireerd door principes uit “click chemistry” ontwerpen de auteurs een slimme katalysator die deze bouwstenen schoon en efficiënt aan elkaar koppelt, wat wijst op groener kunstmest en betere benutting van industriële afvalstromen.

Waarom het maken van ureum heroverwegen?
De huidige ureumproductie steunt op eeuwenoude, hoogtemperatuurs‑ en hogedrukprocessen die tot 2% van de wereldwijde energie verbruiken en meer dan een ton CO2 uitstoten per ton geproduceerd ureum. Tegelijkertijd stoten energiecentrales, fabrieken en afvalwaterstromen kooldioxide en nitraat uit die vaak ongebruikt blijven of milieuschade veroorzaken. Elektrochemische ureumsynthese biedt een manier om twee dingen tegelijk te doen: CO2 en nitraat opruimen en tegelijkertijd bij kamertemperatuur een waardevolle meststof maken. Het probleem is dat op de kleine schaal van moleculen op een metaaloppervlak koolstof‑ en stikstofhoudende fragmenten geneigd zijn hun eigen weg te gaan en veel bijproducten te vormen in plaats van netjes tot ureum te verenigen.
Een door click chemistry geïnspireerde moleculaire assemblagelijn
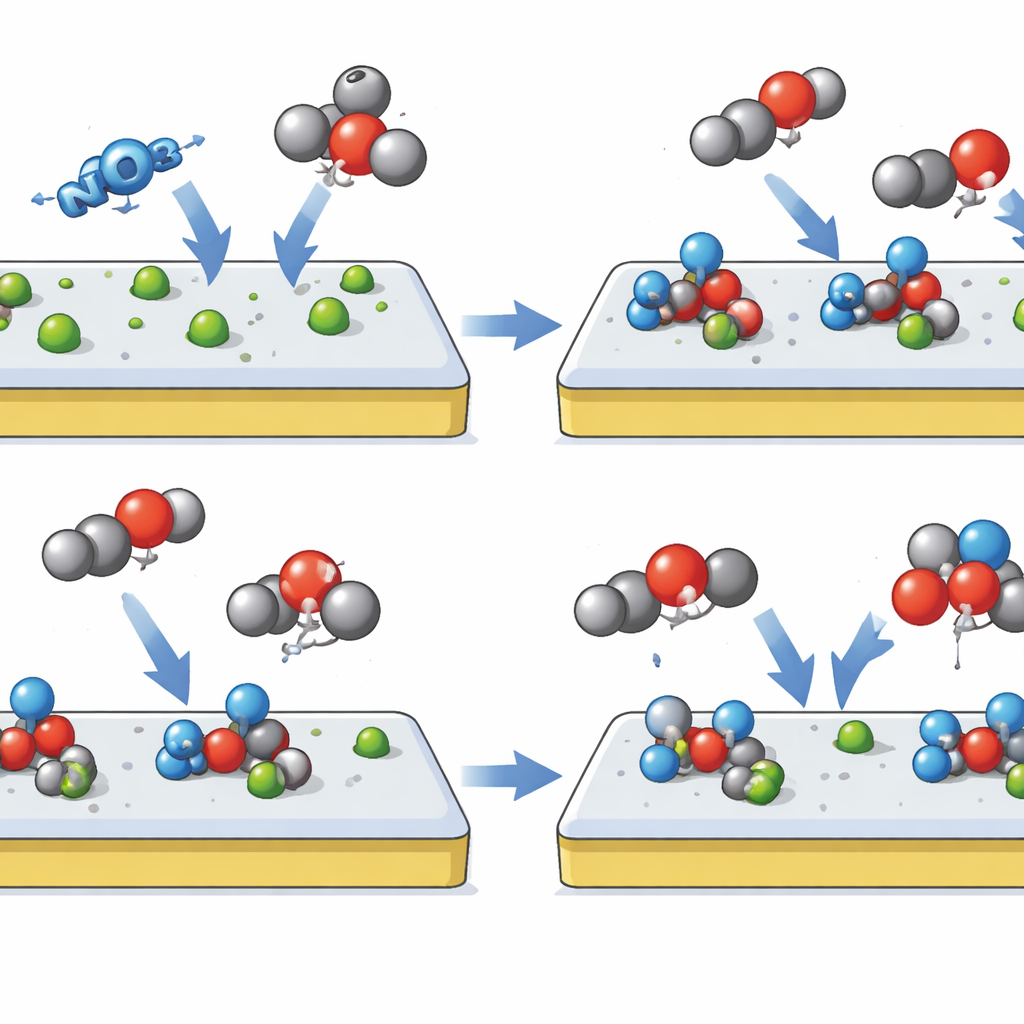
De onderzoekers laten zich inspireren door click chemistry, een gereedschapskist van reacties die gewaardeerd worden omdat ze moleculaire stukjes snel, selectief en met weinig afval verbinden. Ze vertalen dit idee naar een elektrodeoppervlak door een "hiërarchische click‑site" katalysator te bouwen op basis van indiumoxide licht gemodificeerd met het element selenium, genaamd Se–InOx. Het ontwerp creëert twee opeenvolgende fasen op hetzelfde oppervlak. In de eerste fase geeft de katalysator de voorkeur aan het opnemen van nitraat uit de oplossing en zet dat om in een stabiel, nitrietachtig fragment, terwijl hij opzettelijk weigert binnenkomende CO2 te binden. In de tweede fase wordt dat vastgehechte stikstoffragment zelf een aanmeerpunt dat CO2 aantrekt en laat verbinden, waardoor een cruciaal koolstof‑stikstofgebonden intermediair ontstaat dat direct naar ureum leidt.
Hoe het slimme oppervlak zijn werk doet
Om dit gedrag mogelijk te maken, vormt het team subtiel het elektronische landschap van indiumoxide door een klein deel van de zuurstofatomen te vervangen door selenium. Deze aanpassing vergroot de lokale elektrondichtheid en vervormt het kristalrooster net genoeg zodat CO2 het oppervlak onaantrekkelijk vindt, terwijl nitraat en zijn nitrietachtige afsplitsingen sterker binden. Computersimulaties tonen aan dat op dit afgestemde oppervlak het vormen van de cruciale koolstof‑stikstofbinding minder energie kost en concurrerende nevenreacties, die anders nitraat in ammoniak of CO2 in mierenzuur zouden omzetten, naar de achtergrond drukt. Geavanceerde in‑situ metingen — het oppervlak onderzoeken met infraroodlicht en magnetische resonantie terwijl de reactie plaatsvindt — detecteren rechtstreeks de verwachte intermediairen, waaronder de verbonden koolstof‑stikstofsoort, waarmee de stapsgewijze assemblagelijn die de ontwerpers voor ogen hadden wordt bevestigd.
Schonere opbrengst en sterke prestaties
Getest in een stromende elektrochemische cel levert de Se–InOx‑katalysator ureum met zowel hoge snelheid als hoge zuiverheid. Onder geoptimaliseerde omstandigheden bereikt hij een ureumproductiesnelheid van ongeveer 255 millimol per uur per gram katalysator en zet bijna 79% van de elektrische lading om in ureum, waarbij meer dan 85% van de stikstof en praktisch 100% van de koolstof in de producten in ureum terechtkomen in plaats van in nevenproducten. Concurrerende paden die ammoniak, mierenzuur of waterstof genereren, worden sterk onderdrukt. De katalysator behoudt zijn structuur en activiteit over herhaalde cycli en in een opgeschaalde 5 × 5 cm cel die continu 20 uur draait, waarbij meer dan een gram vast ureum wordt geproduceerd dat zuiverheidscontrole met kernspinresonantie doorstaat.
Kosten, klimaatimpact en toekomstige beloften
Naast laboratoriumprestaties beoordelen de auteurs of deze benadering economisch en ecologisch zinvol kan zijn op grotere schaal. Hun analyse suggereert dat, als het wordt aangedreven door goedkope hernieuwbare elektriciteit en verder wordt verbeterd naar een iets hogere efficiëntie, elektrochemisch ureum de huidige marktprijzen zou kunnen benaderen of zelfs onderbieden, vooral wanneer nevenproducten ook gewaardeerd worden. Een levenscyclusanalyse laat zien dat het gebruik van lage‑koolstof elektriciteit de broeikasgasemissies per kilogram ureum onder die van de conventionele route kan brengen. Simpel gezegd toont dit werk aan dat zorgvuldig ontworpen "click‑achtige" oppervlakken kunnen choreograferen hoe afvalkoolstof en ‑stikstof elkaar ontmoeten, waardoor een vervuilingsprobleem verandert in een mestoplossing en een blauwdruk wordt geboden voor schonere productie van andere complexe chemicaliën.
Bronvermelding: Sun, Y., Tian, M., Wu, Q. et al. Sequential-chain coupling over hierarchical click-sites enables highly selective urea electrosynthesis. Nat Commun 17, 2388 (2026). https://doi.org/10.1038/s41467-026-69207-4
Trefwoorden: elektrochemische ureumsynthese, kooldioxide‑benutting, nitraatreductie, heterogene katalyse, duurzame meststof