Clear Sky Science · nl
Structuuranalyse op celniveau met intracellulaire elektronenkristallografie
De vorm van het leven zien, cel voor cel
Eiwitten zijn de kleine machientjes die elke cel in leven houden, maar om echt te begrijpen hoe ze werken moeten wetenschappers hun driedimensionale vormen in detail kunnen zien. Traditioneel betekende dat het zuiveren van enorme hoeveelheden eiwit en het kweken van grote, fragiele kristallen buiten de cel—vaak een langzaam proces dat vaak misgaat. Deze studie presenteert een nieuwe manier om eiwitstructuur direct uit een enkel kristal binnen een enkele cel af te lezen, waarbij elektronen in plaats van röntgenstralen worden gebruikt. Het wijst op een toekomst waarin hoogresolutie structurele biologie kan worden uitgevoerd in gewone laboratoria, en zelfs op het niveau van individuele cellen.
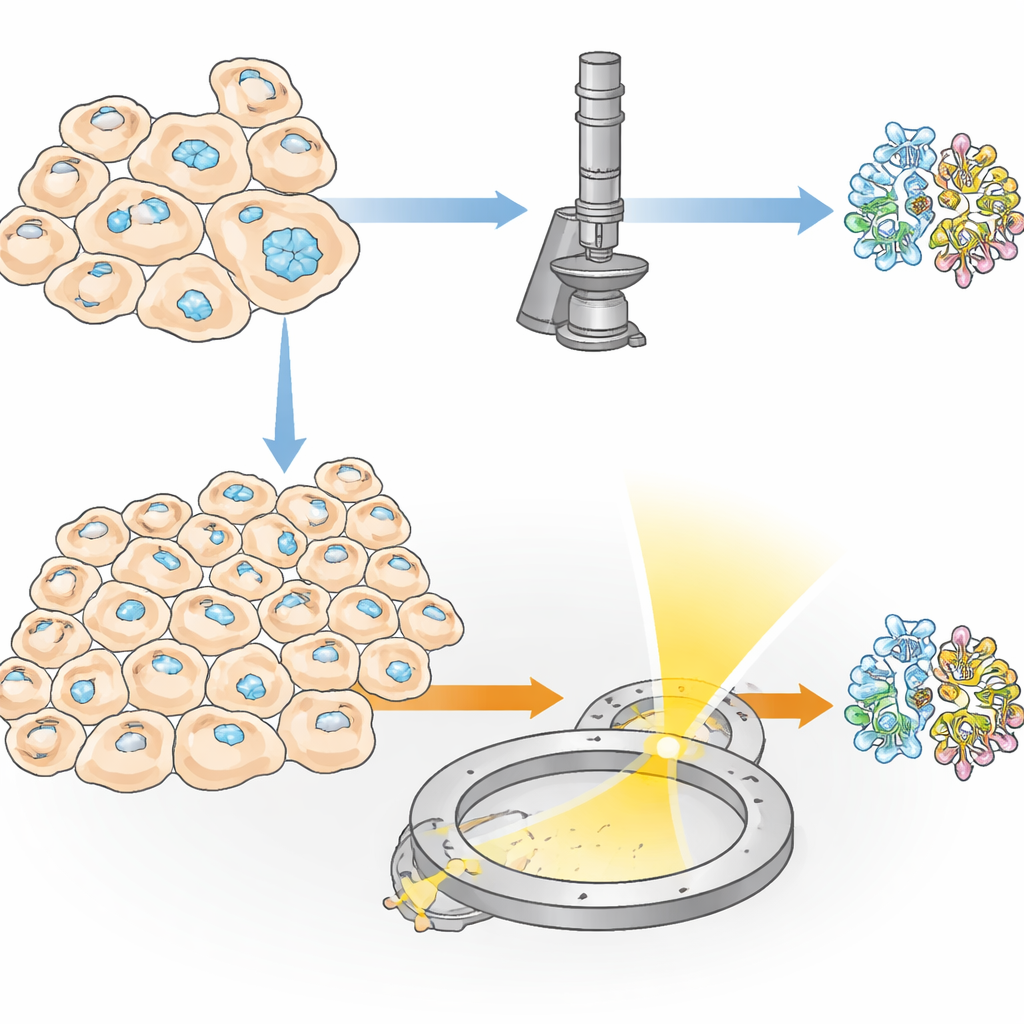
Kristallen verborgen in levende cellen
Sommige eiwitten verzamelen zich van nature in kleine kristallen binnen levende cellen en vervullen functies zoals opslag, bescherming of het helpen van cellen bij stressreacties. Onderzoekers kunnen cellen ook aanzetten tot het produceren van zulke kristallen door ze zo te manipuleren dat ze grote hoeveelheden van een gekozen eiwit maken. Deze “in‑cell” kristallisatie heeft twee grote voordelen: het eiwit verlaat nooit zijn natuurlijke-achtige omgeving, en delicate kenmerken—zoals suikerdecoraties of kleine gebonden moleculen—kunnen behouden blijven op manieren die bij standaard testbuis‑kristallisatie vaak verloren gaan. Toch bleef één groot obstakel bestaan: in veel experimenten vormt slechts een klein deel van de cellen daadwerkelijk kristallen, waardoor traditionele röntgenmethoden tienduizenden kristallen en dus enorme aantallen cellen nodig hebben.
Een nieuwe route: elektronen in plaats van röntgen
De auteurs introduceren een methode die ze IncelluloED noemen, die in‑cell kristallisatie combineert met driedimensionale elektronen‑diffractie. Elektronen wisselen veel sterker met materie dan röntgenstralen, wat betekent dat bruikbare data kunnen worden verzameld uit kristallen die zowel kleiner als talrijker weinig zijn. Het team koos een schimmeleiwit genaamd HEX‑1, dat normaal hexagonale kristallen vormt die helpen kleine poriën tussen schimmelcellen af te dichten onder stress. Door dit eiwit in insectencellen te produceren creëerden ze regelmatige microscopische kristallen die als testcase voor de nieuwe workflow dienden.
Van één kristal naar een gedetailleerde kaart
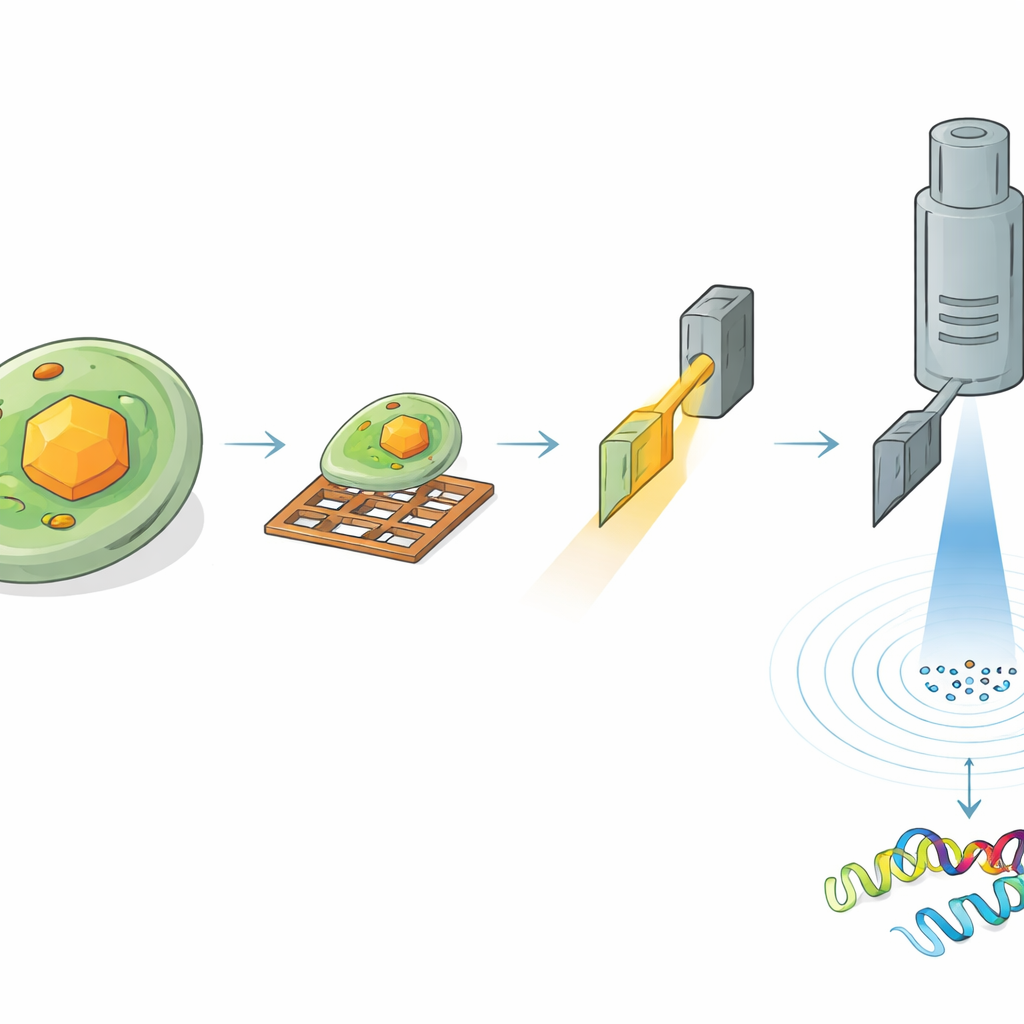
Om de structuur van HEX‑1 binnen een cel te bepalen, moesten de onderzoekers de juiste regio van het monster vinden en zorgvuldig dunner maken. Eerst bevroren ze de kristalhoudende cellen op kleine metalen gaasjes en bedekten het oppervlak met een dunne platinalaag. Met cryogene lichtmicroscopie doorzochten ze grote gebieden van het gaas om cellen met kristallen te lokaliseren en maten de driedimensionale posities van de kristallen onder het oppervlak. Vervolgens brachten ze hetzelfde monster over naar een gespecialiseerd instrument dat een rasterelektronenmicroscoop combineert met een gefocusseerde ionenbundel. Geleid door de eerdere lichtbeelden maalde men het omringende materiaal weg om een ultradunne plak, of lamella, uit te frezen die door een gekozen kristal liep, slechts een paar honderden nanometers dik—ideaal om elektronen doorheen te laten gaan.
Elektronen tonen atomair detail uit microscopische volumes
De voorbereide lamellae werden daarna overgebracht naar een hoogwaardige elektronenmicroscoop die bij cryogene temperaturen opereert. Terwijl de kristalplaat langzaam in de microscoop draaide, passeerde een fijn gecontroleerde elektronenbundel erdoor en creëerde een reeks diffractiepatronen—fijne vlekkenpatronen die de posities van atomen coderen. Uit een kristalvolume van ongeveer 1,6 kubieke micrometer reconstrueerde het team de volledige 3D‑structuur van HEX‑1 met 1,9 ångström resolutie, scherp genoeg om het grootste deel van de zijketens van het eiwit te modelleren. Zelfs kleinere volumes van ongeveer 0,8 kubieke micrometer gaven een vrijwel identieke structuur tegen slechts iets lagere resolutie. Belangrijk is dat de resulterende modellen goed overeenkwamen met die verkregen met een conventionele seriële röntgenaanpak die meer dan 60.000 kristallen en een totaal kristalvolume vereiste dat ongeveer zeven miljoen keer groter was.
Wat dit verandert voor de structurele biologie
Vergelijkingen naast elkaar lieten zien dat de structuur bepaald uit een enkel in‑cell elektronen‑diffractie‑kristal in wezen dezelfde is als die gemiddeld uit tienduizenden kristallen met röntgen. Eventuele verschillen waren klein en grotendeels beperkt tot flexibele lussen, waar natuurlijke beweging te verwachten is. De onderzoekers toonden ook aan dat de gebruikte elektronen‑doses laag genoeg waren om ernstige stralingsschade te voorkomen, en dat elk kristal dat ze verwerkten data van hoge kwaliteit opleverde. Hoewel het prepareren van de dunne lamellae nog steeds vaardigheid en tijd vereist, zijn de benodigde instrumenten—cryo‑lichtmicroscopen, systemen met gefocusseerde ionenbundels en cryo‑elektronenmicroscopen—nu wijdverbreid in veel onderzoekscentra.
Van vele cellen naar een single‑cell structureel lab
Dit werk toont aan dat het nu mogelijk is om een eiwitstructuur op atomair niveau te bepalen uit slechts één kristal binnen één cel, zonder het eiwit ooit te zuiveren. IncelluloED kan bijzonder krachtig zijn wanneer slechts enkele cellen kristallen vormen, of wanneer eiwitten moeilijk te isoleren zijn zonder belangrijke partners of chemische groepen te verliezen. Naarmate de workflow meer geautomatiseerd wordt en op andere eiwitten wordt toegepast, kan het onderzoekers in staat stellen te onderzoeken hoe structuren per cel variëren, ziektes gerelateerde veranderingen in hun native omgeving te bestuderen en zelfs de geneesmiddelontwikkeling direct in levende cellen te ondersteunen. In feite brengt de studie de visie van een “single‑cell structureel laboratorium” veel dichterbij realiteit.
Bronvermelding: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Trefwoorden: elektronendiffractie, in cellulo kristallografie, single-cell structurele biologie, eiwitstructuur, cryo-EM