Clear Sky Science · nl
Vroege diagnose van pancreatische ductale adenocarcinoom met signaal‑versterkte lateral flow immunoassay: SELFI
Waarom het belangrijk is deze kanker vroeg te ontdekken
Alvleesklierkanker is een van de dodelijkste vormen van kanker, grotendeels omdat het meestal te laat wordt ontdekt voor effectieve behandeling. Vroege tumoren geven vaak geen duidelijke symptomen, en de alvleesklier ligt diep in het lichaam waardoor standaard scans ze moeilijk kunnen vinden. Deze studie introduceert een nieuw soort snelle bloedtest, ontworpen om pancreatisch ductaal adenocarcinoom (PDAC) in een vroeger en behandelbaarder stadium op te sporen, met een eenvoudige striptest vergelijkbaar in gebruiksgemak met een zwangerschapstest voor thuis.
Een stille ziekte die moeilijk te zien is
PDAC heeft een vijfjaarsoverleving van minder dan 10%, grotendeels omdat de huidige middelen moeite hebben om het vroeg te detecteren. Beeldvormingstechnieken zoals CT en MRI zijn kostbaar, kunnen belastend zijn en zijn niet bijzonder gevoelig voor kleine, vroege tumoren. Bloedtests zoeken naar moleculen die door tumoren in de bloedbaan worden afgegeven. Voor PDAC is de enige veelgebruikte marker een suikergelagde eiwitmolecule genaamd CA19‑9. Tegenwoordig wordt CA19‑9 meestal gemeten met een enzyme‑linked immunosorbent assay (ELISA), een meerstaps laboratoriumprocedure die gespecialiseerde apparatuur en meer dan vier uur vergt, wat het onpraktisch maakt als eenvoudige screeningsmethode.
Een striptest veranderen in een precisie-instrument
Lateral flow immunoassays—dezelfde basisvorm als veel snelle thuistests—bieden snelheid en eenvoud, maar hun kleurbanden kunnen te zwak zijn wanneer het doelmolecuul in zeer lage concentraties aanwezig is. De auteurs wilden de gebruiksvriendelijkheid van een striptest behouden en tegelijk de gevoeligheid van ELISA evenaren of overtreffen. Ze ontwikkelden SELFI (signal‑enhanced lateral flow immunoassay), die nog steeds CA19‑9 op een testlijn opvangt maar speciaal ontworpen nanodeeltjes gebruikt om die lijn veel donkerder te maken voor dezelfde hoeveelheid marker in bloed. Het doel is een 15‑minuten test die betrouwbaar PDAC‑gerelateerde CA19‑9‑niveaus kan detecteren die oudere striptests zouden missen.
Microscopisch kleine, ontworpen deeltjes die feller schijnen
De kern van SELFI bestaat uit composietnanodeeltjes opgebouwd uit een silica‑bol omhuld met vele kleine gouddeeltjes die door nanometerschalen kloven van elkaar worden gescheiden. Wanneer licht op deze structuur valt, concentreert het elektrische veld sterk in de kloven—"hotspots" die de absorptie en verstrooiing van licht door het deeltje versterken. Met computersimulaties liet het team zien dat het verkleinen van de kloven belangrijker is dan het simpelweg groter maken van de gouddeeltjes: naarmate de kloven kleiner worden, intensiveren de hotspots, wat de totale optische signaalsterkte dramatisch verhoogt. Ze vervaardigden vervolgens een reeks van deze deeltjes met verschillende kloofgroottes en bevestigden experimenteel dat die met de kleinste kloven de diepste kleur op testmembranen produceerden, ver boven de conventionele enkelvoudige gouddeeltjes uitkomend.
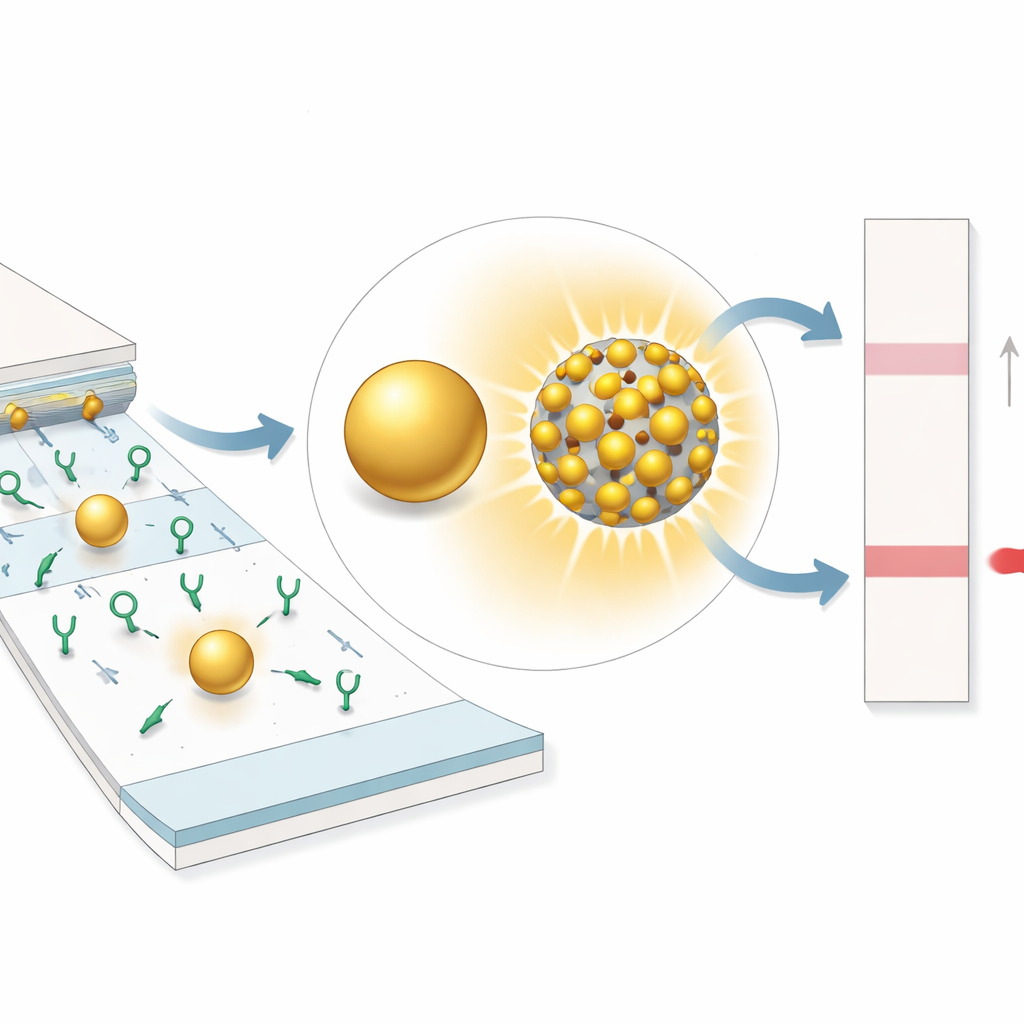
Een snellere en veel gevoeliger bloedtest
Met deze felle nanoprobes meet SELFI CA19‑9 in serum binnen 15 minuten, vergeleken met ongeveer 285 minuten voor ELISA. In gecontroleerde monsters kon SELFI CA19‑9 detecteren bij concentraties die meer dan tienduizend keer lager lagen dan bij een standaard gouddeeltje‑stripsneltest en ongeveer 25 keer lager dan bij een commercieel ELISA‑kit. Hetzelfde nanopartikelontwerp verbeterde ook de detectie van andere aan kanker gerelateerde eiwitten, wat suggereert dat het platform toepasbaar is buiten alleen alvleesklierkanker. Toegepast op bloedmonsters van 150 personen—gezonde vrijwilligers en patiënten met vroeg- en laatstadium PDAC—was SELFI’s vermogen om patiënten in een vroeg stadium van gezonde controles te onderscheiden iets maar significant beter dan ELISA en veel beter dan gewone striptests, gemeten met standaard methoden voor diagnostische nauwkeurigheid.
Wat dit voor patiënten kan betekenen
Dit onderzoek toont aan dat door zorgvuldig te ontwerpen hoe licht interageert met nanodeeltjes op een eenvoudige strip, het mogelijk is een snelle, goedkope bloedtest te creëren die de laboratoriumkwaliteit benadert. SELFI introduceert geen nieuwe biomarker; in plaats daarvan benut het veel beter het al lang bekende CA19‑9‑signaal en kan het in principe worden uitgebreid tot panelen van markers voor verschillende ziekten. Als vervolgonderzoek de prestaties in grotere en diversere populaties bevestigt, zou deze technologie routinematige screening en vroegere diagnose van alvleesklierkanker kunnen mogelijk maken, waardoor patiënten een betere kans krijgen op tijdige chirurgie en effectieve behandeling.
Bronvermelding: Jang, S., Shin, M., Han, J. et al. Early diagnosis of pancreatic ductal adenocarcinoma by signal-enhanced lateral flow immunoassay: SELFI. Nat Commun 17, 2768 (2026). https://doi.org/10.1038/s41467-026-69204-7
Trefwoorden: alvleesklierkanker, vroegtijdige opsporing, lateral flow test, nanodeeltjes, biomerkers