Clear Sky Science · nl
14-3-3ζ interageert met de DNA-bindende domein van FOXO3a en dissocieert competitief DNA via dubbele-motief bevestiging
Hoe kankercellen hun eigen zelfvernietigingsschakelaar uitschakelen
Onze cellen hebben ingebouwde fail-safe systemen die hun eigen dood kunnen activeren wanneer ze te beschadigd of gevaarlijk worden. Een van die systemen wordt geregeld door een eiwit genaamd FOXO3a, dat genen activeert die afwijkende cellen aanzetten tot zelfmoord. Veel kankers vinden echter manieren om FOXO3a te stil te leggen en blijven daardoor doorgroeien. Deze studie onderzoekt op moleculair niveau hoe een ander eiwit, 14-3-3ζ, kankercellen helpt FOXO3a van het DNA los te wrikken en zo deze zelfvernietigingsschakel uit te schakelen.
Het waakzame eiwit dat terugdringt tegen kanker
FOXO3a fungeert als een soort veiligheidsinspecteur voor de cel. Het bindt aan specifieke plekken op het DNA en activeert genen die de groei vertragen of geprogrammeerde celdood (apoptose) op gang brengen wanneer er iets misgaat. In gezonde cellen helpt dit voorkomen dat tumoren ontstaan. In veel kankers echter wordt een groeibevorderend pad, aangedreven door gemuteerde Ras-eiwitten, permanent geactiveerd. Dit pad zet een kinase genaamd AKT aan, die FOXO3a op meerdere plekken chemisch markeert met fosfaatgroepen. Die markeringen vormen aanhechtingsplekken voor 14-3-3ζ, een dimerisch “adapter”-eiwit dat gefosforyleerde motieven op veel doelwitten herkent. Wanneer 14-3-3ζ zich vastklampt aan FOXO3a, beginnen de interne remmen van de cel te falen.
Waarom eenvoudige bindingssterkte het effect niet kon verklaren
Eerder werk aan een verwant eiwit, FOXO4, suggereerde dat 14-3-3-eiwitten FOXO-factoren van DNA wegtrekken simpelweg omdat ze sterker binden. Maar FOXO3a heeft een sterkere voorkeur voor zijn natuurlijke DNA-doelen dan het oudere model veronderstelde. In deze studie maakten de onderzoekers een versie van FOXO3a die het DNA-bindende domein en twee belangrijke fosforyleringsplaatsen bevat. Ze maten hoe sterk dit eiwit aan DNA of aan 14-3-3ζ bindt en vonden dat de verschillen in bindingssterkte bescheiden waren: 14-3-3ζ was slechts ongeveer twee keer een sterkere partner dan DNA. Toch kon 14-3-3ζ in mengexperimenten die volgen hoe moleculen door een chromatografiekolom reizen bijna volledige vrijgave van DNA uit FOXO3a veroorzaken, alsof het ongeveer 100 keer competitiever was dan verwacht. Deze discrepantie wees erop dat er een extra mechanisme werkzaam was.
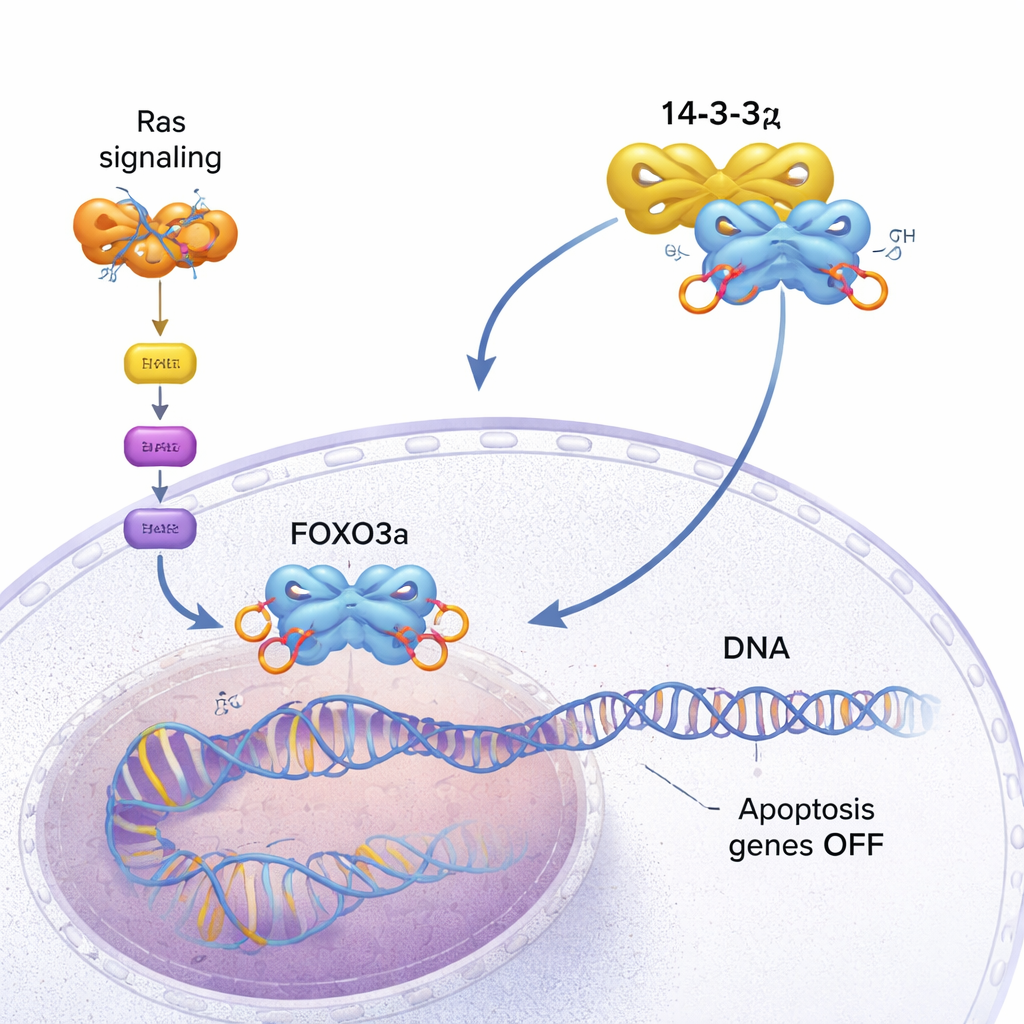
Een driepuntsgreep die DNA verdringt
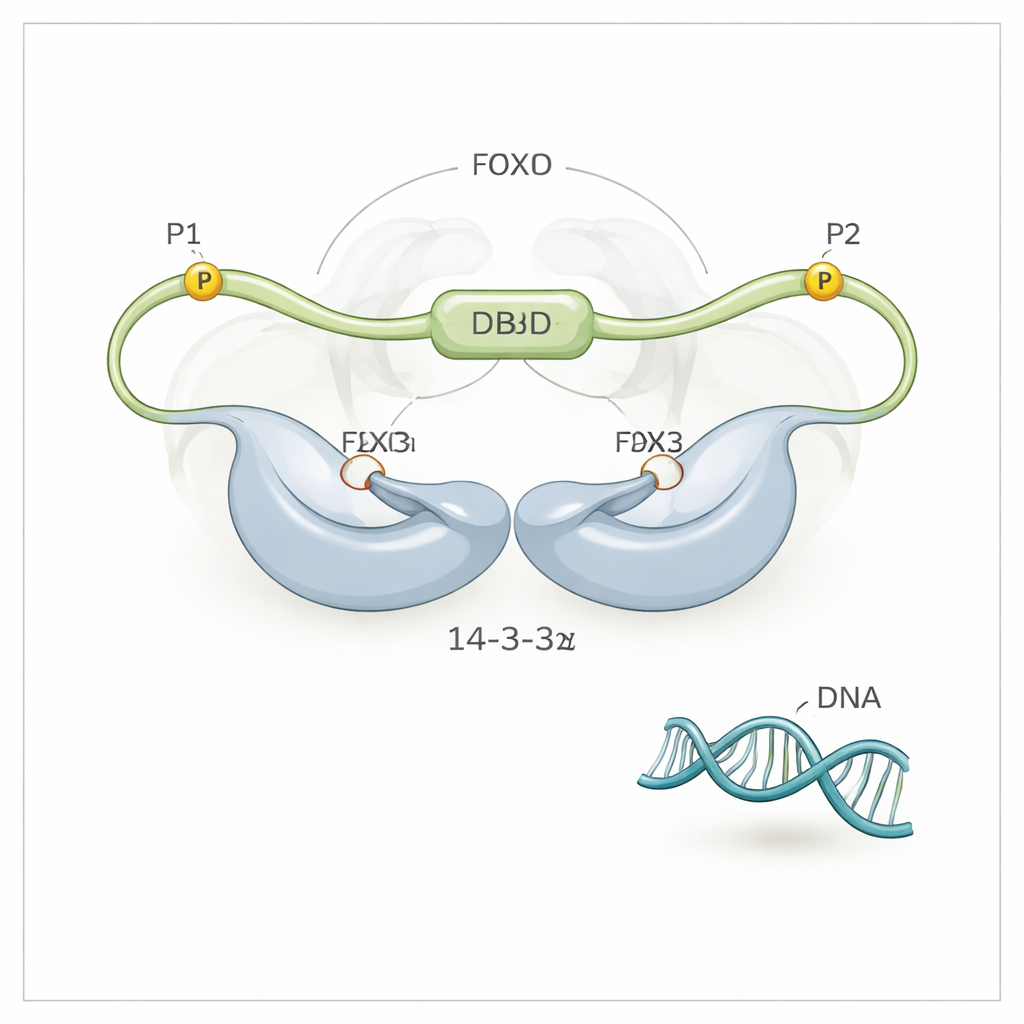
Met behulp van hoogresolutie NMR-spectroscopie ontdekte het team dat 14-3-3ζ meer doet dan alleen FOXO3a bij zijn twee gefosforyleerde motieven (P1 en P2) grijpen. Het maakt ook directe, hoewel zwakkere, contacten met het DNA-bindende domein (DBD) van FOXO3a zelf — het oppervlak dat normaal gesproken het DNA omarmt. Het 14-3-3ζ-eiwit vormt een symmetrische dimer met twee groeven. Elke groeve klemt zich vast aan een van de gefosforyleerde motieven op FOXO3a, waardoor FOXO3a op twee punten aan 14-3-3ζ wordt bevestigd. Omdat een van deze motieven (P2) zeer dicht langs de keten bij het DNA-bindende domein ligt, houdt deze “dubbele-motief bevestiging” 14-3-3ζ effectief vlak naast het DBD, waardoor de kans sterk toeneemt dat het DBD tegen en op het oppervlak van 14-3-3ζ bindt in plaats van aan DNA. De onderzoekers zagen zelfs dat het DBD heen en weer schommelt tussen de twee zijden van de 14-3-3ζ-dimer, waarbij het grootste deel van de tijd afgeschermd is van het DNA.
Welke fosfaatlabels het meest belangrijk zijn
Om de rollen van de twee gefosforyleerde sites uit elkaar te houden, ontwierp het team FOXO3a-varianten waarin telkens slechts één site tegelijk gefosforyleerd kon worden. Wanneer alleen de P2-site nabij het DBD actief was, kon 14-3-3ζ het DNA gedeeltelijk losmaken maar niet volledig. Wanneer alleen de meer verre P1-site actief was, kon 14-3-3ζ wel aan FOXO3a binden maar had het nauwelijks effect op de greep op DNA. Volledige vrijgave van DNA vereiste dat beide sites samenwerkten: P1 biedt een hoogaffiniteit initiële aanhechtingsplaats voor 14-3-3ζ, en P2 positioneert de dimer dicht genoeg bij het DBD om de lokale concentratie van 14-3-3ζ op die plek effectief enorm te maken. Deze meerstaps-tethering versterkt een bescheiden voorkeur in bindingssterkte tot een krachtige capaciteit om DNA te verdrijven.
Van moleculaire touwtrek naar nieuwe medicijnideeën
Voor niet-specialisten is de kernboodschap dat kankercellen een slimme ruimtelijke truc gebruiken, niet alleen brute bindingssterkte, om een belangrijk tumorsuppressoreiwit stil te leggen. 14-3-3ζ gebruikt twee kleine fosfaatafhankelijke ankerpunten op FOXO3a als bevestigingspunten, reikt vervolgens over om het DNA-grippende oppervlak van het kern-domein van FOXO3a te dekken en voorkomt zo dat het genen voor celdood activeert. Omdat dezelfde FOXO- en 14-3-3-families veelvuldig in verschillende weefsels voorkomen, is deze dubbele-tetheringstrategie waarschijnlijk ook gebruikelijk in andere vormen van kanker. Het verstoren van óf de fosfaatafhankelijke ankers óf het zwakkere contact met het DNA-bindende oppervlak van FOXO3a zou zijn vermogen om zelfvernietigingsprogramma's in tumorcellen te activeren kunnen herstellen, en biedt veelbelovende nieuwe invalshoeken voor het ontwerpen van anti-kanker medicijnen.
Bronvermelding: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Trefwoorden: FOXO3a, 14-3-3-eiwitten, apoptose, Ras–AKT-signaaloverdracht, kankertherapieën