Clear Sky Science · nl
Overleving van weefsel‑residentiële macrofagen hangt af van mitochondriale functie gereguleerd door SerpinB2 bij chronische ontsteking
Waarom de immuuncellen in vet ertoe doen
De meeste mensen denken bij lichaamsvet aan passieve opslag, maar het is in feite een bedrijvig weefsel vol immuuncellen die helpen ontsteking en bloedsuiker te regelen. Deze studie laat zien hoe een specifieke groep langlevende immuuncellen in diep buikvet functioneert als beschermers tegen type 2‑diabetes — en hoe chronische ontsteking bij obesitas ze geruisloos omlegt door hun kleine energiecentrales, de mitochondriën, te beschadigen.
Twee soorten vet‑beschermers
Visceraal vet — vet rondom de inwendige organen — bevat twee hoofdtypen immuuncellen die macrofagen worden genoemd. Het ene type is kortlevend en wordt constant aangevuld uit het bloed; deze "inflammatoire" macrofagen bevorderen doorgaans ontsteking en insulineresistentie. Het andere type zijn langetermijn, weefsel‑residentiële macrofagen die vroeg in het leven ontstaan en normaal gesproken het weefsel tot rust brengen, gezonde vetopslag ondersteunen en de insulinegevoeligheid van het hele lichaam bevorderen. Door deze cellen bij muizen te volgen en de genactiviteit te vergelijken, toonden de onderzoekers aan dat residentiële macrofagen verrijkt zijn in anti‑inflammatoire en insuline‑sensitiserende genen, terwijl inkomende monocyten‑afgeleide macrofagen genen tot expressie brengen die de bloedsuikercontrole verslechteren.
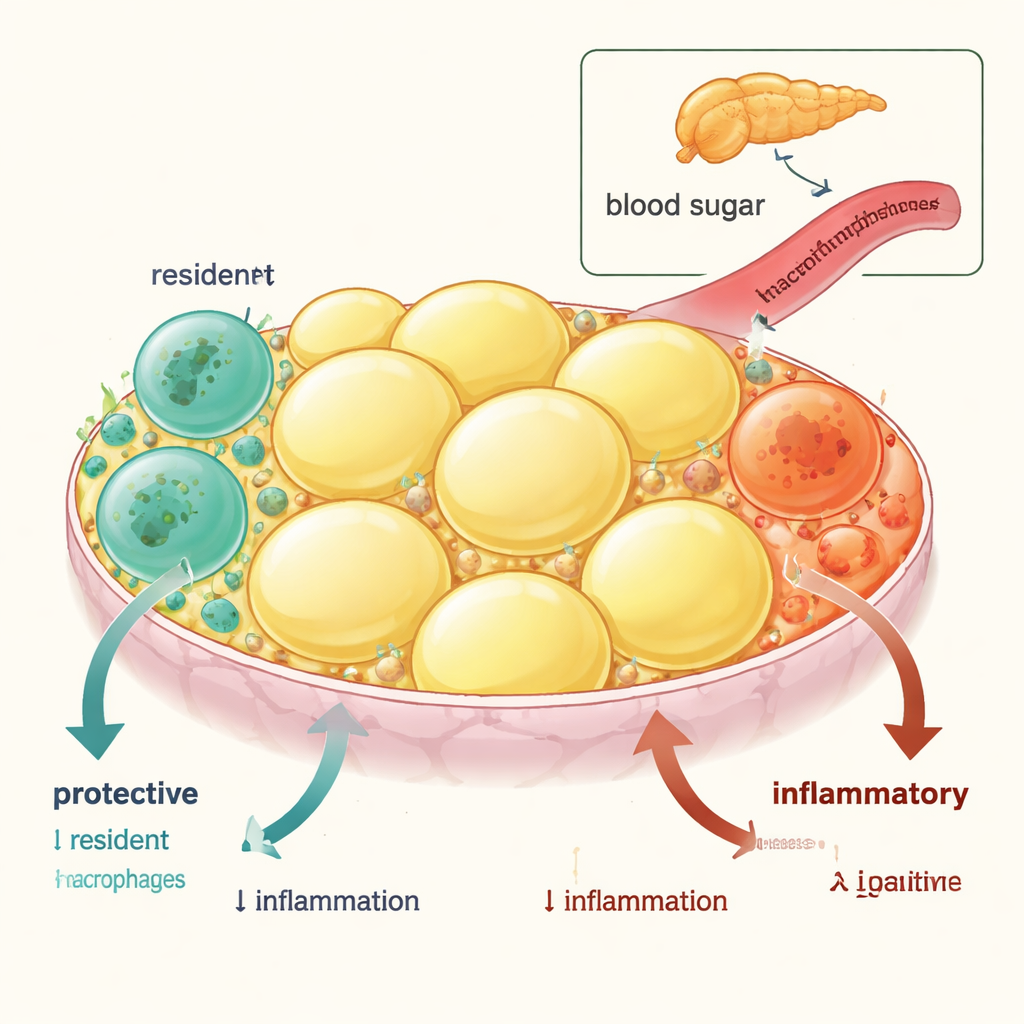
Wanneer ontsteking de goeden doodt
Bij obesitas verschuift dit beschermende evenwicht. Het team vond dat bij zowel obese muizen als obese of diabetische mensen het aantal residentiële macrofagen in visceraal vet afneemt, terwijl het aantal inflammatoire macrofagen toeneemt. Zorgvuldig beeldvormend onderzoek en merkers voor celdood toonden waarom: residentiële macrofagen ondergaan meer geprogrammeerde celdood (apoptose), terwijl de inflammatoire cellen dat niet doen. Opmerkelijk is dat toen obese muizen van een vetrijk dieet werden gehaald, de residentiële populatie langzaam herstelde via lokale proliferatie en de metabole gezondheid verbeterde — wat laat zien dat dit verlies wordt aangedreven door de ontstekingsstatus en kan worden omgekeerd.
Één eiwit verbindt mitochondriën met overleving
Een belangrijke aanwijzing was een eiwit genaamd SerpinB2, beter bekend van functies bij de bloedstolling. De onderzoekers ontdekten dat SerpinB2 zeer sterk wordt geproduceerd in residentiële macrofagen, maar veel minder in inflammatoire. Bij obese mensen en muizen verminderde de expressie van SerpinB2 in residentiële macrofagen scherp, en een hogere body‑massindex ging samen met minder SerpinB2‑positieve cellen. Experimenten in cellen zonder SerpinB2 toonden verhoogde lekkage van cytochroom c — een cruciaal eiwit — uit mitochondriën naar het cytoplasma, een klassieke trigger van apoptose. Deze SerpinB2‑deficiënte macrofagen hadden minder antioxiderende verdediging, meer mitochondriale reactieve zuurstofsoorten (ROS) en een hoger zuurstofverbruik, allemaal tekenen van gestreste, overbelaste mitochondriën die cellen richting inflammatoir gedrag en celdood duwen.
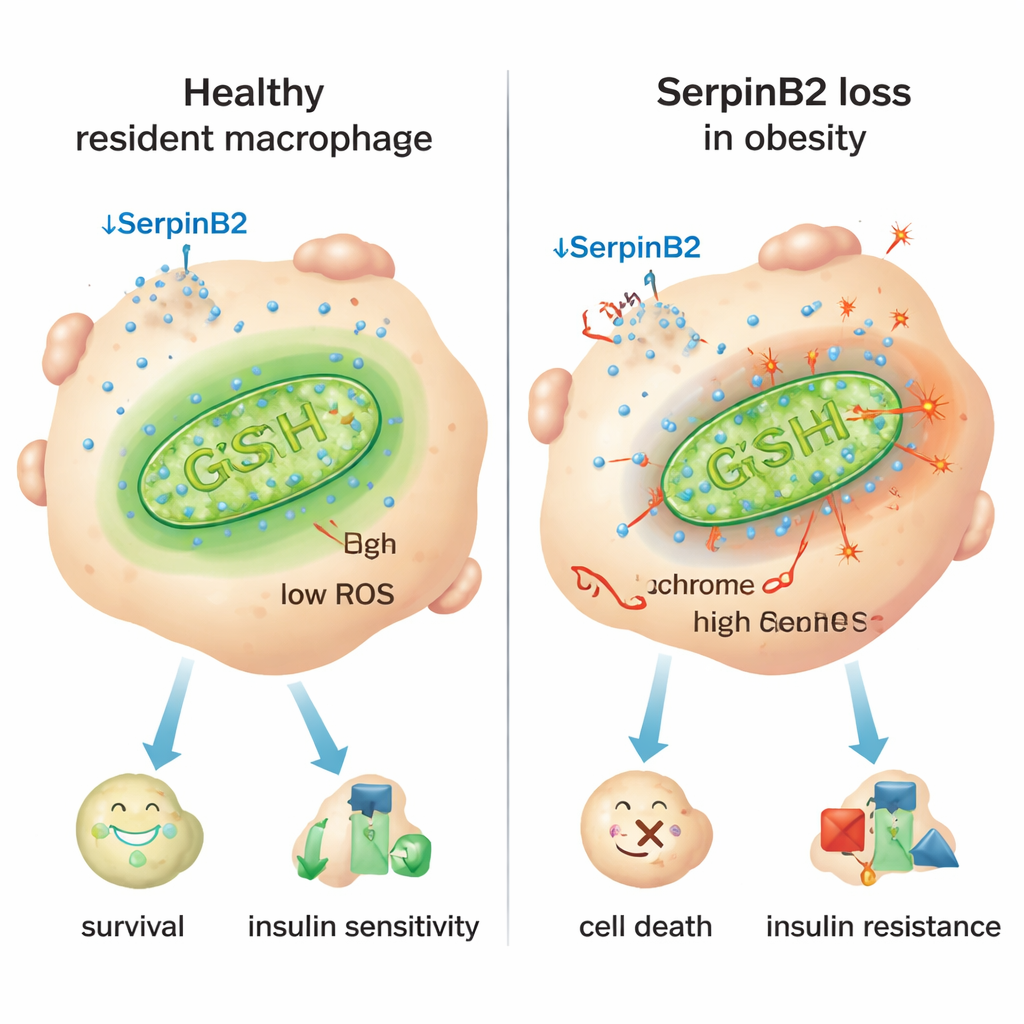
De ontstekingsschakelaar en een mogelijke oplossing
De studie herleidde deze mitochondriale stress tot chronische ontstekingssignalen bij obesitas, met name de immuunboodschapper interferon‑γ (IFN‑γ), die in vetweefsel in overmaat wordt geproduceerd. IFN‑γ activeert een transcriptierepressor genaamd Ikaros die bindt aan de regelregio van het SerpinB2‑gen en de expressie onderdrukt. In muizen die zo zijn gemodificeerd dat hun myeloïde cellen niet op IFN‑γ kunnen reageren, behielden residentiële macrofagen SerpinB2, overleefden ze beter en toonden de dieren lagere bloedsuiker, betere insulinegevoeligheid en kleinere vetcellen. Omgekeerd verergerde het verwijderen van SerpinB2 specifiek in macrofagen de glucosetolerantie en insulineresistentie, deels omdat het vetweefsel meer ontstoken raakte en vergrootte. Het verhogen van glutathion‑antioxidanten met het supplement N‑acetylcysteïne (NAC) herstelde de mitochondriale bescherming, redde de overleving van residentiële macrofagen, verkleinde adipocyten en verbeterde metabole maten zelfs wanneer SerpinB2 ontbrak.
Wat dit betekent voor metabole gezondheid
Voor de niet‑specialist is de kernboodschap dat niet alle vet of vet‑residentiële immuuncellen schadelijk zijn. Een gespecialiseerde, langlevende groep macrofagen in visceraal vet beschermt ons juist tegen toenemende ontsteking en hoge bloedsuiker door hun mitochondriën gezond te houden via SerpinB2‑gedreven antioxidantverdediging. Bij obesitas schakelen chronische ontstekingssignalen SerpinB2 uit, raken mitochondriën gestrest, sterven deze beschermende cellen en nemen meer schadelijke macrofagen het over, wat bijdraagt aan insulineresistentie. Het werk suggereert dat therapieën die gericht zijn op het behouden van residentiële macrofagen — door de IFN‑γ/Ikaros‑rem op SerpinB2 te blokkeren of door glutathion‑gebaseerde antioxidantverdediging te ondersteunen — kunnen helpen metabole ziekten gerelateerd aan obesitas te voorkomen of behandelen.
Bronvermelding: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Trefwoorden: visceraal vet, macrofagen, mitochondriën, insulineresistentie, SerpinB2