Clear Sky Science · nl
Metabole engineering van doxorubicine-biosynthese via optimalisatie van P450-redoxpartners en structurele analyse van DoxA
Waarom het ontstaansverhaal van een kankergeneesmiddel ertoe doet
Doxorubicine is een van de pijlers van de moderne chemotherapie en wordt gebruikt bij kanker van leukemie tot borstumoren. Toch is de manier waarop we dit geneesmiddel maken verrassend omweggerelateerd: de industrie bouwt het meestal op uit een verwant molecuul in plaats van het zijn oorspronkelijke microbe het proces te laten afronden. Deze studie onthult waarom de producerende bacterie moeite heeft met het voltooien van de laatste chemische stappen en toont aan hoe het herontwerpen van haar interne machinerie het aandeel volledig gevormde doxorubicine sterk kan verhogen, wat de weg vrijmaakt voor betrouwbaardere en mogelijk goedkopere voorraden.
Van bodembacteriën tot levensreddend geneesmiddel
Doxorubicine behoort tot de anthracyclines, een familie van natuurlijke moleculen geproduceerd door bodembacteriën van het geslacht Streptomyces. Deze verbindingen delen een stijf, vlak koolstofskelet dat tussen DNA-basen schuift, plus een suikereenheid die in de groeven van DNA past. Samen blokkeren deze eigenschappen de DNA-verwerkende machinerie van de cel en leiden ze uiteindelijk tot celdood — nuttig tegen snel delende kankercellen. De klassieke producent, Streptomyces peucetius, maakt van nature voornamelijk een voorloper genaamd daunorubicine en slechts een bescheiden hoeveelheid van het effectievere doxorubicine, dat verschilt door slechts één extra zuurstofdragende groep. Die kleine structurele wijziging verbetert de activiteit dramatisch, maar blijkt verrassend moeilijk efficiënt door de microbe te worden aangebracht.
Het juiste elektrische bedrading in de cel vinden
Het cruciale enzym dat de laatste drie oxidatiestappen op het geneesmiddelskerm uitvoert, heet DoxA, een lid van de cytochroom P450-familie. Als een miniatuurfabriek heeft DoxA een constante aanvoer van elektronen nodig om zuurstof te activeren en nieuwe zuurstofatomen op het geneesmiddel aan te brengen. Binnen de bacterie worden die elektronen geleverd via een relais van hulpproteïnen, bekend als redoxpartners. Het genoom van S. peucetius bevat meerdere kandidaten, waardoor onduidelijk was welke daadwerkelijk met DoxA samenwerken. Door genexpressie en metabolisme te vergelijken in een normale stam, een daunorubicine-rijke mutant en een doxorubicine-rijke mutant, identificeerden de onderzoekers één ferredoxine (Fdx4) en één ferredoxine-reductase (FdR3) als de natuurlijke partners. Het herbouwen van dit trio in reageerbuisreacties bevestigde dat DoxA het best werkt wanneer het is aangesloten op deze specifieke elektronenoverdrachtsketen, vergelijkbaar met het kiezen van de juiste stroomadapter voor een apparaat.
Het wegnemen van de door het enzym zelf veroorzaakte vertraging
Zelfs met de juiste elektrische bedrading heeft DoxA de neiging vast te lopen bij de laatste stap die daunorubicine omzet in doxorubicine. Eerder werk suggereerde dat het product zelf het enzym kan blokkeren. Het team richtte zich op een aangrenzend gen, dnrV, waarvan de functie onduidelijk was. Biochemische tests toonden aan dat het DnrV-eiwit een reeks anthracyclinemoleculen, waaronder doxorubicine, sterk bindt zonder ze chemisch te veranderen. Het toevoegen van DnrV aan DoxA-reacties verbeterde de chemische doorstroom aanzienlijk, waardoor voorlopers volledig naar het eindproduct werden omgezet en destructieve bijreacties werden vermeden. In praktische termen fungeert DnrV als een interne spons die vers gevormde doxorubicine opneemt en voorkomt dat het enzym verstopt raakt of het DNA in de producerende cel beschadigt.
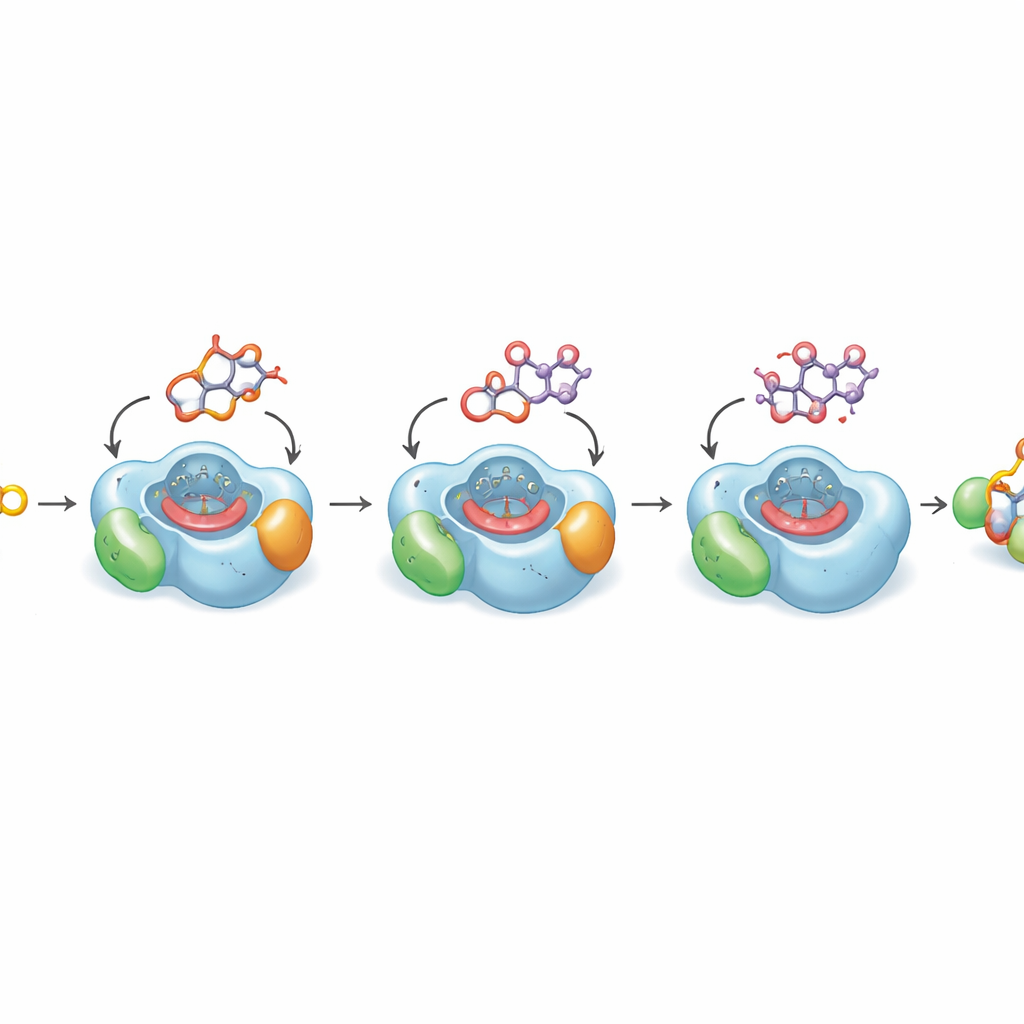
Zien waarom de laatste stap zo traag is
Om te begrijpen waarom de cruciale laatste oxidatie van nature traag verloopt, bepaalden de auteurs hogeresolutie-kristalstructuren van DoxA gebonden aan drie opeenvolgende tussenproducten. Deze structuren tonen hoe de platte drugkern en de eraan bevestigde suiker in een nauwsluitend pocket boven het heemgroepen van het enzym nestelen, het reactieve metaalcentrum dat de oxidatie uitvoert. Voor de eerdere stappen ligt het koolstofatoom dat gemodificeerd moet worden dicht bij het heem in een ideale positie voor de reactie. Maar in het laatste substraat, daunorubicine, buigt het deel van het molecuul dat gehydroxyleerd moet worden weg van het heem in een kleine olieachtige holte, een rangschikking die kwantumberekeningen laten zien energetisch gunstiger is. Computersimulaties over microseconde-tijdschaal bevestigen dat het molecuul slechts af en toe een productieve houding aanneemt voor die laatste zuurstofinvoering. Deze structurele voorkeur verklaart waarom de omzetting naar doxorubicine van nature inefficiënt is.
Een betere doxorubicine-producerende stam bouwen
Gewapend met deze inzichten ontwierpen de onderzoekers de bacterie rationeel in plaats van te vertrouwen op willekeurige mutagenese. Ze introduceerden een gen voor DNA-reparatie om de productie te stabiliseren, installeerden vervolgens extra kopieën van doxA, de optimale redoxpartners fdx4 en fdr3, en de behulpzame binder dnrV onder zorgvuldig gekozen promoterreeksen om hun hoeveelheden in balans te brengen. Ze verfijnden ook de kweekcondities en gebruikten speciale harsen om toxische en kleverige tussenproducten op te nemen. In flessen in het laboratorium en in een 20-liter bioreactor produceerde de beste gemodificeerde stam 336 milligram doxorubicine per liter cultuur met een verhouding van 81:19 doxorubicine tot daunorubicine — een stijging van ongeveer 180% ten opzichte van de beginnende stam en een veel schoner productmengsel.
Wat dit betekent voor de toekomstige aanvoer van kankergeneesmiddelen
Door zowel het elektrische ondersteuningssysteem als de driedimensionale structuur van een sleutelenzym te ontleden, verklaart dit werk waarom een medisch vitale microbe ondermaats presteert bij het maken van onze meest gewaardeerde anthracycline. Het koppelen van DoxA aan zijn natuurlijke redoxpartners, het toevoegen van een drugbindend helper-eiwit en het opnieuw in balans brengen van genexpressie veranderde een terughoudende producent in een robuuste. Hoewel verdere tuning van het enzym de laatste chemische stap nog verder zou kunnen versnellen, brengt de studie biologische productie van doxorubicine al veel dichter bij industriële toepasbaarheid. Voor patiënten en zorgsystemen kunnen dergelijke verbeteringen leiden tot een veiligere, schaalbaardere en kosteneffectievere toegang tot een essentieel chemotherapiemiddel.
Bronvermelding: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Trefwoorden: doxorubicineproductie, anthracycline-biosynthese, enzymengineering, microbiële geneesmiddelenfabricage, cytochroom P450