Clear Sky Science · nl
Atypische proteïnekinase C-activatie zorgt voor intestinale glucose-excretie bij diabetes mellitus
De darm als suikerkraan
Mensen met diabetes hebben te veel suiker in hun bloed. Bariatrische ingrepen zoals gastric bypass kunnen de bloedglucose verrassend snel normaliseren, zelfs voordat er veel gewicht verloren is, maar hoe dat gebeurt was lange tijd onduidelijk. Deze studie onthult een darmspecifieke "suikerkraan"—een manier waarop de darm suiker uit het bloed kan halen en een deel daarvan terug in de darm kan lozen—en suggereert een nieuw medicijndoel dat de voordelen van de operatie zou kunnen nabootsen zonder snede.
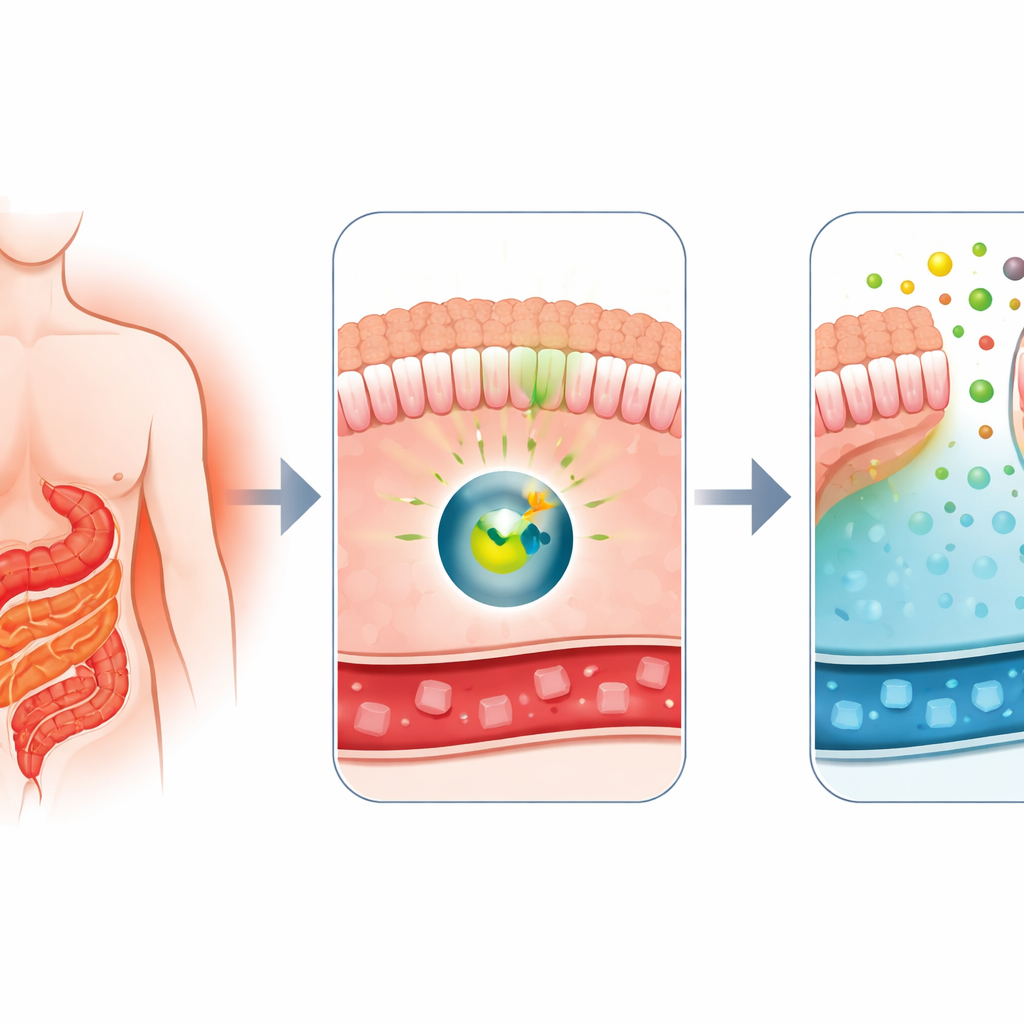
Waarom chirurgie de bloedglucose zo snel verandert
Artsen weten al lang dat Roux-en-Y gastric bypass, een veelvoorkomende gewichtsverliesoperatie, ook een van de krachtigste behandelingen tegen type 2 diabetes is. Kort na de ingreep verbetert de bloedglucose van patiënten vaak dramatisch, nog voordat ze veel gewicht verliezen. Eerder werk van deze groep toonde aan dat delen van de dunne darm na bypass als een spons beginnen te werken: ze nemen glucose uit de bloedbaan op en geven een deel ervan af aan het lumen van de darm. Dat vreemde gedrag, intestinale glucose-excretie genoemd, leek afhankelijk te zijn van een transportereiwit genaamd GLUT1. De grote vraag was: welke moleculaire schakelaar zet de darm aan om in deze suikerruimingmodus te gaan?
Met big data op zoek naar een moleculaire schakelaar
Om die schakelaar te vinden gebruikten de onderzoekers een grootschalig computationeel geneesmiddelen-ontdekkingssysteem gebaseerd op de Connectivity Map, een databank van hoe duizenden chemicaliën de genactiviteit in cellen veranderen. Ze vergeleken genexpressiepatronen uit vijf situaties waarin intestinale glucose-excretie hoog is—including weefsel van bypass-geopereerde ratten en cellen behandeld met een darmsgroeisignaal—with patronen veroorzaakt door bekende geneesmiddelen. Één klasse verbindingen sprong consequent in het oog: activatoren van proteïnekinase C (PKC), een familie enzymen die signalen binnen cellen doorgeven. Bij nadere bestudering concentreerde het team zich op de “atypische” subgroep van PKC-enzymen, met name een isoform genaamd PKCζ, wiens activiteit in darmcellen het meest overeenkwam met de bypass-achtige, glucose-uitdrijvende toestand.
De suikerpomp van darmcellen in actie
Met single-cell RNA-sequencing keken de auteurs fijnmazig naar individuele darmcellen en vonden dat bypasschirurgie zowel PKCζ als GLUT1 verhoogt in specifieke nutriëntopnemende cellen die de distale dunne darm bekleden. In celkweken en humane intestinale organoïden leidde het kunstmatig verhogen van PKCζ, of behandeling met prostratine—een plantaardige verbinding die deze atypische PKC-enzymen veilig activeert—ertoe dat GLUT1 naar het celoppervlak werd gebracht. Daar fungeerde GLUT1 als een tweerichtingspomp: het trok meer glucose uit de bloedzijdige kant van de cellen en maakte het mogelijk dat overtollige glucose naar het darmlumen werd afgevoerd. Belangrijk is dat deze omleiding van suiker de glycolyse in de cellen zelf niet significant versnelde, wat erop wijst dat het belangrijkste effect het afvoeren van glucose was, niet extra energieproductie.
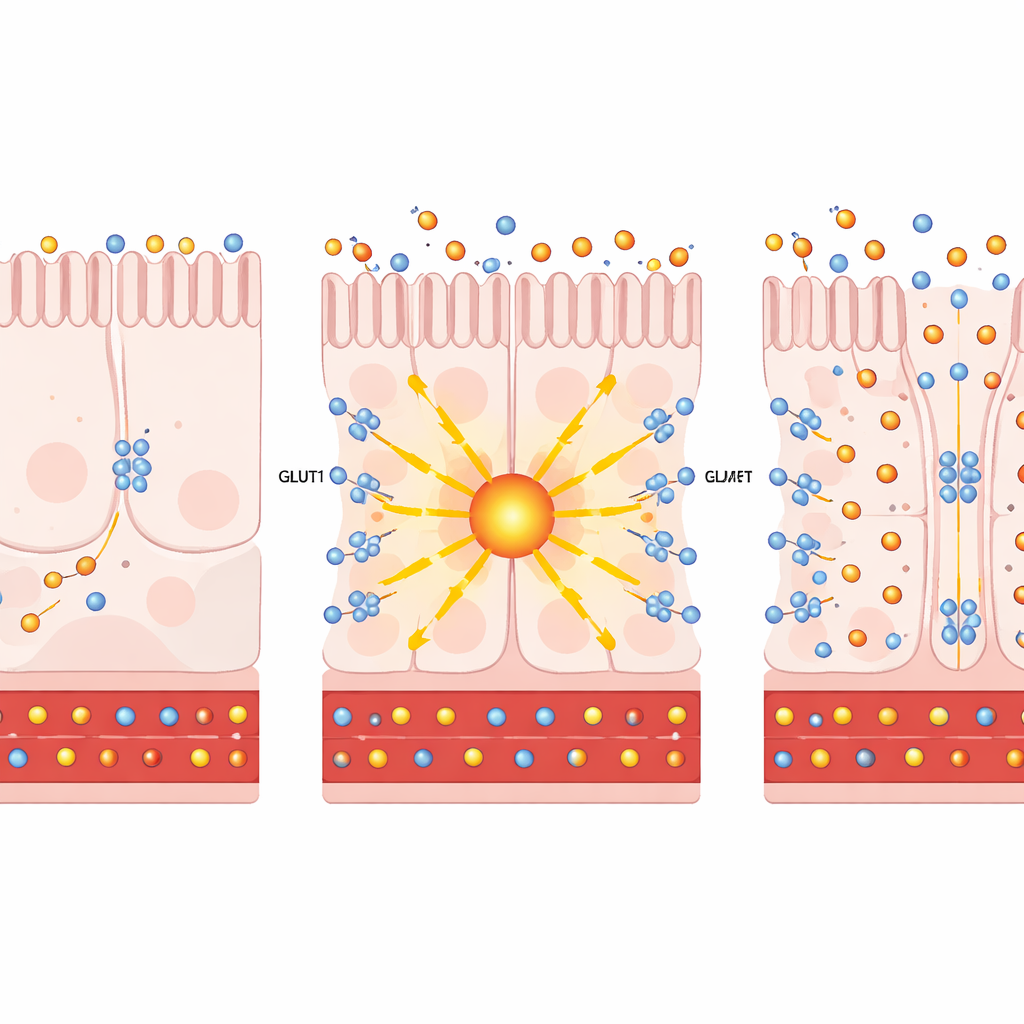
Van cellen naar muizen: chirurgie nabootsen zonder scalpel
Het team testte vervolgens of het activeren van deze route in levende dieren diabetes zou kunnen verbeteren. Bij obese, insulineresistente muizen leidde het specifiek extra in de darm toedienen van PKCζ tot langzamer gewichtstoename, lagere nuchtere bloedglucose en betere glucosetolerantie. Radioactieve suikerklaargevers toonden aan dat er meer suiker door de distale darm werd opgenomen en in het darmlumen werd uitgespoeld. Een vergelijkbaar beeld ontstond in diabetische muismodellen behandeld met prostratine: ze kwamen minder aan, verwerkten suikerbelastingen beter en schakelden meer glucose naar het darmscysteem om, allemaal zonder veranderingen in insulineniveaus, voedselinname of darmbarrière-integriteit. In weefselsneden was GLUT1 zichtbaar aan zowel de bloedzijdige als de darmszijdige kanten van de cellen, precies gepositioneerd om suiker uit de circulatie te halen en in de darm te duwen.
Wat dit kan betekenen voor toekomstige diabeteszorg
Voor niet-specialisten is de kernboodschap dat de darm kan worden omgevormd tot een gecontroleerde uitlaat voor overtollige bloedglucose. Door een specifiek enzym in darmcellen—atypische PKC—te activeren konden de onderzoekers cellen ertoe aanzetten meer GLUT1-transporters naar hun oppervlak te verplaatsen en zich als een omkeerbare afvoer te gedragen: suiker uit het bloed trekken en een deel ervan terug in de darm lozen. Bij muizen verbeterde deze darmaangedreven glucoselozing de bloedglucose en beperkte gewichtstoename zonder overmatige stimulatie van insuline, verandering van eetlust of beschadiging van de darm. Hoewel prostratine en verwante verbindingen nog geen goedgekeurde diabetesmiddelen zijn, wijst dit werk op de aPKC–GLUT1-route als een veelbelovend target voor toekomstige geneesmiddelen die gedeeltelijk de metabolische voordelen van gastric bypass zouden kunnen nabootsen zonder operatie.
Bronvermelding: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Trefwoorden: intestinale glucose-excretie, type 2 diabetes, GLUT1-transporter, atypische proteïnekinase C, prostratine